Losmapimod
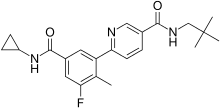 | |
| Rättslig status | |
|---|---|
| Rättslig status | |
| Identifierare | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard | 100.158.124 |
| Kemiska och fysikaliska data | |
| Formel | C22H26FN3O2 _ _ _ _ _ _ _ _ |
| Molar massa | 383,467 g·mol -1 |
| 3D-modell ( JSmol ) | |
| |
| |
|
| |
Losmapimod ( GW856553X ) är ett prövningsläkemedel som utvecklas av Fulcrum Therapeutics för behandling av facioscapulohumeral muskeldystrofi (FSHD); en klinisk fas III-prövning väntar på godkännande. Losmapimod hämmar selektivt enzymerna p38α/β mitogenaktiverade proteinkinaser (MAPK), som är modulatorer av DUX4 -uttryck och mediatorer av inflammation .
Potentiell behandling för FSHD
Fulcrum Therapeutics, ett Massachusetts-baserat bioteknikföretag, identifierade p38α/β MAPK-hämmare som potenta suppressorer av DUX4-uttryck, vars avsuppression accepteras som orsaken till FSHD. Bland p38α/β MAPK-hämmare valde Fulcrum losmapimod som sin föredragna utvecklingskandidat på grund av dess "substantiella och attraktiva prekliniska och kliniska data" från tidigare GlaxoSmithKline (GSK) kliniska prövningar.
När Fulcrum upptäckte den potentiella nyttan av p38 MAPK-hämning vid behandling av FSHD, kom en forskargrupp från Saint Louis University (SLU) oberoende till samma slutsats. SLU-forskargruppen fann att p38α- och p38β-isoformer oberoende bidrar till DUX4-uttryck, vilket indikerar potentiell vinst i att utforska isoformspecifik (p38α eller p38β) hämning för att balansera terapeutiska effekter med biverkningar.
En teoretisk begränsning av losmapimod är att p38-kinashämning kan försämra myogenesen, den motsatta effekten av vad som önskas. Facio Therapies, ett holländskt läkemedelsföretag med en egen läkemedelskandidat för FSHD, meddelade att de hade eliminerat p38 kinashämmare (inklusive losmapimod) som en utvecklingskandidat eftersom p38 kinashämmare resulterade i försämrad myotubbildning på deras läkemedelsutvecklingsplattform. Andra har faktiskt funnit att p38a-upphävande försämrar myotubbildning. Fulcrum fann emellertid att p38-kinashämning inte försämrade myotubfusion vid nivåer tillräckliga för DUX4-reduktion.
Fulcrum utveckling tidslinje
- Mars 2022: Fulcrum tillkännagav plan för en klinisk fas III-prövning för behandling av FSHD, kallad REACH. Till skillnad från den tidigare testversionen kommer den primära slutpunkten att vara tillgänglig arbetsyta .
- Juni 2021: Resultaten av en randomiserad kontrollerad klinisk fas IIb-studie, kallad ReDUX4, visade statistiskt signifikant försämring av muskelfunktionsförsämring, även om biomarkörerna var oförändrade. Ytterligare rättegångar väntar.
- Mars 2021: Fulcrum tillkännagav avbrytande av LOSVID på grund av utmaningar med inskrivningen och den snabbt utvecklande miljön för behandling av covid-19 .
- Juni 2020: Fulcrum meddelade att de ansöker till FDA om att inleda en klinisk fas III-prövning, LOSVID, för losmapimod vid behandling av COVID-19. Nya bevis tyder på att p38 MAPK-hämning kan vara terapeutisk, möjligen genom att dämpa det överdrivna inflammatoriska svaret efter SARS-CoV-2- infektion.
- Januari 2020: Fulcrum meddelade att han fått status som särläkemedel för losmapimod.
- Oktober 2019: Fulcrum tillkännagav preliminära resultat av sin kliniska fas 1-studie av losmapimod. Oral dosering av losmapimod visade ihållande läkemedelskoncentrationer i muskelvävnad som i prekliniska in vitro-studier hade visat sig vara effektiva för att minska DUX4-nivåerna.
- April 2019: Fulcrum förvärvade från GSK de globala rättigheterna till losmapimod.
Historiska undersökningar
Losmapimod upptäcktes och utvecklades utan framgång av GSK för att behandla flera medicinska tillstånd. Trots att det inte lyckades bevisa effekt, visade GSK kliniska prövningar att losmapimod i allmänhet tolereras väl av mer än 3 500 försökspersoner.
GSK undersökte losmapimod som ett terapeutiskt medel för patienter efter hjärtinfarkt (hjärtinfarkt). Trots kliniska fas II-prövningar visade den kliniska fas IIIA-studien (LATITUDE) inte signifikant förbättrade kliniska resultat. I oktober 2015 meddelade GSK att de avbryter den planerade fas IIIB-studien, men skulle "utvärdera alla alternativ för framtida utveckling."
GSK undersökte losmapimod som ett läkemedel för KOL, men flera kliniska fas II-prövningar visade inte att losmapimod förbättrar träningstolerans, lungfunktion, arteriell inflammation, endotelfunktion eller frekvensen av KOL-exacerbationer hos personer med KOL. GSK avslutade utvecklingen av losmapimod för KOL 2016.
GSK undersökte losmapimod som ett terapeutiskt medel för allvarlig depressiv sjukdom (MDD) på grundval av att depression var korrelerad med förhöjda proinflammatoriska cytokiner. Fas II kliniska studier misslyckades med att visa en signifikant förbättring av depressionssymtom och biomarkörer.