Synaptisk taggning
Synaptisk märkning , eller den synaptiska märkningshypotesen, föreslogs först 1997 av Uwe Frey och Richard G. Morris ; den försöker förklara hur neural signalering vid en viss synaps skapar ett mål för efterföljande plasticitetsrelaterad produkthandel ( PRP) som är avgörande för ihållande LTP och LTD . Även om taggarnas molekylära identitet förblir okänd, har det fastställts att de bildas som ett resultat av hög- eller lågfrekvent stimulering , interagerar med inkommande PRP:er och har en begränsad livslängd.
Ytterligare undersökningar har föreslagit att plasticitetsrelaterade produkter inkluderar mRNA och proteiner från både soma och dendritiska axeln som måste fångas upp av molekyler i dendritiska ryggraden för att uppnå ihållande LTP och LTD. Denna idé artikulerades i den synaptiska tag-and-capture-hypotesen. Sammantaget utvecklar synaptisk taggning den molekylära grunden för hur L-LTP genereras och leder till minnesbildning .
Historia
Frey, en forskare vid Leibniz Institute for Neurobiology , och Morris, en forskare vid University of Edinburgh , lade grunden för den synaptiska taggningshypotesen, och sa:
"Vi föreslår att LTP initierar skapandet av en kortvarig proteinsyntesoberoende 'synaptisk tag' vid den potentierade synapsen som binder det eller de relevanta proteinerna för att etablera sen LTP. Till stöd för denna idé visar vi nu att svaga tetanisk stimulering, som vanligtvis endast leder till tidig LTP, eller upprepad stelkramp i närvaro av proteinsyntesinhibitorer, resulterar var och en i proteinsyntesberoende sen LTP, förutsatt att upprepad stelkramp redan har tillämpats vid en annan ingång till samma population av neuroner . Den synaptiska taggen sönderfaller på mindre än tre timmar. Dessa fynd tyder på att långvarigheten av LTP beror inte bara på lokala händelser under dess induktion, utan också på neurons tidigare aktivitet."
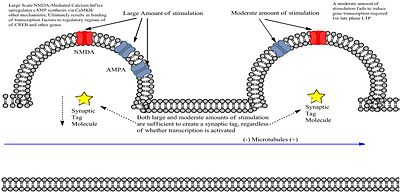
L-LTP-inducerande stimulans inducerar två oberoende processer inklusive en dendritisk biologisk tagg som identifierar synapsen som stimulerad och en genomisk kaskad som producerar nya mRNA och proteiner (plasticitetsprodukter). Även om svag stimulering också taggar synapser, producerar den inte kaskaden. Proteiner som produceras i kaskaden är karakteristiskt promiskuösa, eftersom de kommer att fästa vid alla nyligen taggade synapser. Men som Frey och Morris upptäckte är taggen tillfällig och kommer att försvinna om inget protein presenterar sig för infångning. Därför måste taggen och proteinproduktionen överlappa varandra om L-LTP ska induceras av högfrekvent stimulering .
Experimentet utfört av Frey och Morris involverade stimulering av två olika uppsättningar av Schaffer kollaterala fibrer som synapserade på samma population av CA1 -celler. De registrerade sedan fält- EPSP associerat med varje stimulus på antingen S1- eller S2-vägar för att producera E-LTP och L-LTP på olika synapser inom samma neuron , baserat på stimulansens intensitet. Resultaten visade 1) att E-LTP producerad av svag stimulering kunde omvandlas till L-LTP om en stark S2-stimulus levererades före eller efter och 2) att förmågan att omvandla E-LTP till L-LTP minskade när intervallet mellan två stimulanser ökade, vilket skapade tidsmässigt beroende. När de blockerade proteinsyntesen före leverans av stark S2-stimulering förhindrades omvandlingen till L-LTP, vilket visade vikten av att översätta mRNA som produceras av den genomiska kaskaden.
Efterföljande forskning har identifierat ytterligare en egenskap hos synaptisk taggning som involverar associationer mellan sen LTP och LTD. Detta fenomen identifierades först av Sajikumar och Frey 2004 och kallas nu för "korstaggning". Det involverar sen-associativa interaktioner mellan LTP och LTD inducerade i uppsättningar av oberoende synaptiska ingångar : sen-LTP inducerad i en uppsättning synaptiska ingångar kan omvandla tidig-LTD till sen-LTD i en annan uppsättning av ingångar. Den motsatta effekten uppstår också: tidig LTP inducerad i den första synapsen kan omvandlas till sen LTP om den följs av en sen LTD-inducerande stimulans i en oberoende synaps. Detta fenomen ses eftersom syntesen av icke-specifika plasticitetsrelaterade proteiner (PRP) av sen-LTP eller -LTD i den första synapsen är tillräcklig för att transformera tidig-LTD/LTP till sen-LTD/LTP i den andra synapsen efter att synaptiska taggar har blivit uppsättning.
Blitzer och hans forskargrupp föreslog en modifiering av teorin 2005, och angav att proteinerna som fångas av den synaptiska taggen faktiskt är lokala proteiner som översätts från mRNA som finns i dendriterna. Detta betyder att mRNA inte är en produkt av genomisk kaskad initierad av stark stimulans, utan snarare levereras som ett resultat av kontinuerlig basal transkription . De föreslog att även svagt stimulerade synapser som var taggade kan acceptera proteiner som produceras från en stark stimulering i närheten trots att de saknar den genomiska kaskaden.
mRNA-trafik till dendritiska ryggraden och cytoskelettet
Synaptisk taggning/tag-och-fångsteori adresserar potentiellt det betydande problemet med att förklara hur mRNA, proteiner och andra molekyler specifikt kan trafikeras till vissa dendritiska ryggraden under LTP i sen fas. Det har länge varit känt att den sena fasen av LTP beror på proteinsyntes inom den särskilda dendritiska ryggraden, vilket bevisats genom att injicera anisomycin i en dendritisk ryggrad och observera den resulterande frånvaron av sen LTP. För att uppnå translation inom den dendritiska ryggraden måste neuroner syntetisera mRNA:t i kärnan, paketera det i ett ribonukleoproteinkomplex , initiera transport, förhindra translation under transport och slutligen leverera RNP-komplexet till lämplig dendritiska ryggraden. Dessa processer spänner över ett antal discipliner och synaptisk taggning/tag-och-fånga kan inte förklara dem alla; ändå spelar synaptisk taggning sannolikt en viktig roll för att styra mRNA-handel till den lämpliga dendritiska ryggraden och signalera att mRNA-RNP-komplexet dissocierar och kommer in i dendritiska ryggraden.
En cells identitet och identiteterna för subcellulära strukturer bestäms till stor del av RNA- transkript. Med tanke på denna premiss följer det att cellulär transkription, trafficking och translation av mRNA genomgår modifiering vid ett antal olika tillfällen. Med början med transkription modifieras mRNA-molekyler potentiellt via alternativ splitsning av exoner och introner . De alternativa splitsningsmekanismerna tillåter celler att producera en mångsidig uppsättning proteiner från en enda gen i genomet. Den senaste utvecklingen inom nästa generations sekvensering har möjliggjort större förståelse för den mångfald som eukaryota celler uppnår genom splitsningsvarianter.
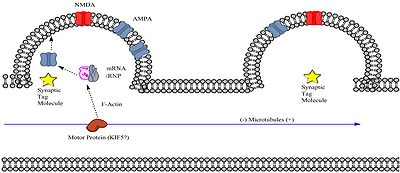
Transkriberat mRNA måste nå den avsedda dendritiska ryggraden för att ryggraden ska kunna uttrycka L-LTP. Neuroner kan transportera mRNA till specifika dendritiska ryggraden i en förpackning tillsammans med ett transport-ribonukleoprotein (RNP)-komplex; transport-RNP-komplexet är en undertyp av en RNA-granul. Granuler som innehåller två proteiner av känd betydelse för synaptisk plasticitet, CaMKII (Calmodulin-beroende Kinase II) och den omedelbara tidiga genen Arc, har identifierats för att associera med en typ av motorproteinet kinesin, KIF5. Dessutom finns det bevis för att polyadenylerat mRNA associerar med mikrotubuli i däggdjursneuroner, åtminstone in vitro. Eftersom mRNA-transkript genomgår polyadenylering innan de exporteras från kärnan, tyder detta på att mRNA som är väsentligt för senfas-LTP kan färdas längs mikrotubulierna i det dendritiska skaftet innan det når den dendritiska ryggraden.
När RNA/RNP-komplexet anländer via motorprotein till ett område i närheten av den specifika dendritiska ryggraden, måste det på något sätt "fångas" av en process i den dendritiska ryggraden. Denna process involverar sannolikt den synaptiska taggen som skapas av synaptisk stimulering med tillräcklig styrka. Synaptisk taggning kan resultera i infångning av RNA/RNP-komplexet via valfritt antal möjliga mekanismer som:
- Den synaptiska taggen utlöser transient mikrotubuli in i dendritiska ryggraden. Ny forskning har visat att mikrotubuli tillfälligt kan komma in i dendritiska ryggraden på ett aktivitetsberoende sätt. []
- Den synaptiska taggen utlöser lastens dissociation från motorprotein och leder den på något sätt till dynamiskt bildade mikrofilament
Lokal proteinsyntes
Sedan 1980-talet har det blivit mer och mer tydligt att dendriterna innehåller ribosomer , proteiner och RNA-komponenter för att uppnå lokal och autonom proteintranslation. Många mRNA som visat sig vara lokaliserade i dendriterna kodar för proteiner som är kända för att vara involverade i LTP, inklusive AMPA-receptor och CaMKII-subenheter, och cytoskelettrelaterade proteiner MAP2 och Arc .
Forskare gav bevis på lokal syntes genom att undersöka fördelningen av Arc-mRNA efter selektiv stimulering av vissa synapser i en hippocampuscell. De fann att Arc-mRNA var lokaliserat vid de aktiverade synapserna, och Arc-protein uppträdde där samtidigt. Detta tyder på att mRNA:t translaterades lokalt.
Dessa mRNA-transkript translateras på ett cap-beroende sätt, vilket betyder att de använder en "cap"-förankringspunkt för att underlätta ribosomfästning till den 5'-otranslaterade regionen. Medlemmar av eIF4-gruppen (eukaryot initieringsfaktor 4) rekryterar ribosomala subenheter till mRNA-terminalen, och sammansättning av eIF4F-initieringskomplexet är ett mål för translationskontroll: fosforylering av eIF4F exponerar locket för snabb omladdning, vilket påskyndar det hastighetsbegränsande steget för translation. Det föreslås att eIF4F-komplexbildning regleras under LTP för att öka lokal translation. Dessutom destabiliserar överdrivet eIF4F-komplex LTP.
Forskare har identifierat sekvenser inom mRNA som bestämmer dess slutdestination - kallade lokaliseringselement (LEs), postnummer och målinriktningselement (TEs). Dessa känns igen av RNA-bindande proteiner, av vilka några potentiella kandidater är MARTA och ZBP1. De känner igen TE:erna, och denna interaktion resulterar i bildning av ribonukleotidproteinkomplex (RNP), som färdas längs cytoskelettfilament till ryggraden med hjälp av motorproteiner. Dendritiska TE har identifierats i den oöversatta regionen av flera mRNA, som MAP2 och alphaCaMKII.
Möjliga tagmodeller
Synaptisk taggning kommer sannolikt att involvera förvärvet av molekylära underhållsmekanismer genom en synaps som sedan skulle möjliggöra bevarandet av synaptiska förändringar. Det finns flera föreslagna processer genom vilka synaptisk taggning fungerar. En modell föreslår att taggen möjliggör lokal proteinsyntes vid den specificerade synapsen som sedan leder till modifieringar i synaptisk styrka. Ett exempel på denna föreslagna mekanism involverar förankringen av PKMzeta -mRNA till den taggade synapsen. Detta ankare skulle sedan begränsa aktiviteten av translaterad PKMzeta, ett viktigt plasticitetsrelaterat protein, till denna plats. En annan modell föreslår att kortsiktiga synaptiska förändringar som induceras av stimulansen själva är taggen; efterföljande levererade eller översatta proteinprodukter verkar för att stärka denna förändring. Till exempel stabiliseras avlägsnandet av AMPA-receptorer på grund av lågfrekvent stimulering som leder till LTD av en ny proteinprodukt som skulle vara inaktiv vid synapser där internalisering inte hade skett. Taggen kan också vara ett latent minnesspår, som en annan modell föreslår. Aktiviteten hos proteiner skulle då krävas för att minnesspåret skulle leda till ihållande förändringar i synaptisk styrka. Enligt denna modell är förändringar inducerade av det latenta minnesspåret, såsom tillväxten av nya filipodier, själva taggen. Dessa taggar kräver proteinprodukter för stabilisering, synapsbildning och synapsstabilisering. Slutligen föreslår en annan modell att de erforderliga molekylära produkterna leds in i lämpliga dendritiska grenarna och sedan hittar de specifika synapserna under effektmodifiering, genom att följa Ca++ mikrokoncentrationsgradienter genom spänningsstyrda Ca++-kanaler.
Beteendetaggning
Medan konceptet med den synaptiska taggningshypotesen huvudsakligen härrörde från experiment som tillämpade stimulering på synapser, kan en liknande modell etableras med tanke på inlärningsprocessen i en bredare - beteendemässig - mening. Fabricio Ballarini och kollegor utvecklade denna beteendetaggningsmodell genom att testa rumslig objektigenkänning, kontextuell konditionering och betingad smakaversion hos råttor med svag träning. Den tillämpade träningen resulterar normalt endast i förändringar av korttidsminnet. Men de parade ihop denna svaga träning med en separat, godtycklig beteendehändelse som antas inducera proteinsyntes. När de två beteendehändelserna kopplades ihop inom en viss tidsram var den svaga träningen tillräcklig för att framkalla uppgiftsrelaterade förändringar i långtidsminnet. Forskarna trodde att den svaga träningen leder till en "inlärningstagg". Under den efterföljande uppgiften resulterade klyvningen av proteiner i bildandet av långtidsminne för denna tagg. Den beteendemässiga taggningsmodellen motsvarar den synaptiska taggningsmodellen. En svag stimulering etablerar E-LTP som kan fungera som taggen som används för att omvandla den svaga potentieringen till den starkare, mer ihållande L-LTP, när högintensiv stimulering väl appliceras.