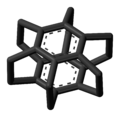
Superphane

|
|||
|
|
|||
| Namn | |||
|---|---|---|---|
| Andra namn [2.2.2.2.2.2](1,2,3,4,5,6)cyklofan
|
|||
| Identifierare | |||
|
3D-modell ( JSmol )
|
|||
| ChemSpider | |||
|
PubChem CID
|
|||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Egenskaper | |||
| C24H24 _ _ _ | |||
| Molar massa | 312,456 g·mol -1 | ||
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|||
Superphane är en 6-faldigt bryggad cyklofan med alla arenpositioner i bensendimeren upptagna av etylendistanser. Föreningen har varit av visst vetenskapligt intresse som modell för att testa aromaticitet och syntetiserades första gången av Virgil Boekelheide 1979. Superphane är basföreningen för en stor grupp av derivat med strukturella variationer. Analogerna med 2 till 5 bryggor är också kända föreningar. Bensenringarna har ersatts av andra aromatiska enheter, såsom de baserade på ferrocen eller stabiliserad cyklobutadien . Ett flertal derivat är kända med variationer i typen och längden på bryggenheterna.
Syntes
Den första syntesen av superphane själv av Boekelheide involverade att bilda par av överbryggande enheter. Vid varje steg pyrolyseras två o- klormetyltoluenstrukturer för att bilda o - xylylener , antingen direkt eller via bensocyklobutenintermediärer . Vid ytterligare pyrolys genomgår dessa var och en elektrocyklisk ringöppning för att bilda o - xylylener . Dessa strukturer var inte isolerade - de reagerar omedelbart via [4+4] cykloadditionsreaktioner för att bilda två intilliggande broar mellan de aromatiska ringarna.
Processen startade från 2,4,5-trimetylbensylklorid 1 , som pyrolyserades vid 700 °C för att ge bensocyklobuten 2 och pyrolyserades vidare till cyklooktan- dimeren 3 . Riecheformylering gav 4 (efter separation från andra regioisomerer), aldehydreduktion med användning av natriumborhydrid gav diol 5 och sedan klorering med användning av tionylklorid ) gav diklorid 6 . En annan pyrolys gav tetrabryggad cyklofan 7 , en annan formyleringsreaktion gav dialdehyd 8 , en annan reduktions-/kloreringssekvens gav diklorid 9 och en slutlig pyrolys gav superfan 10 som hårda vita kristaller med smältpunkt 325–327 °C.
Andra syntetiska vägar publicerades av Hopf (1983) och en annan av Boekelheide (1984).
Struktur och egenskaper
Röntgenanalys visar D 6h molekylär symmetri med de aromatiska planen separerade med 262 pm . Sp 2 - sp 3 kol-kolbindningarna är ur plan med bensenringarna med 20°. Stamenergin uppskattas till 20 kcal/mol . Proton-NMR visar bara en topp vid 2,98 ppm och kol-NMR två vid 32 ppm och 144 ppm.