Pentosfosfatväg
Pentosfosfatvägen (även kallad fosfoglukonatvägen och hexosmonofosfatshunten och HMP - shunten ) är en metabolisk väg parallell med glykolys . Det genererar NADPH och pentoser (5- kolsocker ) samt ribos 5-fosfat , en prekursor för syntesen av nukleotider . Medan pentosfosfatvägen involverar oxidation av glukos , är dess primära roll anabol snarare än katabolisk . Vägen är särskilt viktig i röda blodkroppar (erytrocyter).
Det finns två distinkta faser i vägen. Den första är den oxidativa fasen, i vilken NADPH genereras, och den andra är den icke-oxidativa syntesen av 5-kolsocker. För de flesta organismer sker pentosfosfatvägen i cytosolen ; i växter sker de flesta stegen i plastider .
Liksom glykolys verkar pentosfosfatvägen ha ett mycket gammalt evolutionärt ursprung. Reaktionerna av denna väg är mestadels enzymkatalyserade i moderna celler, men de förekommer också icke-enzymatiskt under förhållanden som replikerar de i det arkeiska havet och katalyseras av metalljoner , särskilt järnjoner (Fe(II)). Detta tyder på att ursprunget till vägen kan gå tillbaka till den prebiotiska världen.
Resultat
De primära resultaten av vägen är:
- Generering av reducerande ekvivalenter, i form av NADPH, som används i reduktiva biosyntesreaktioner inom celler (t.ex. fettsyrasyntes) .
- Produktion av ribos 5-fosfat (R5P), som används vid syntes av nukleotider och nukleinsyror.
- Produktion av erytros 4-fosfat (E4P) som används vid syntes av aromatiska aminosyror .
Aromatiska aminosyror är i sin tur prekursorer för många biosyntetiska vägar, inklusive ligninet i trä. [ citat behövs ]
Pentosocker i kosten som härrör från nedbrytningen av nukleinsyror kan metaboliseras genom pentosfosfatvägen, och kolskeletten från kostkolhydrater kan omvandlas till glykolytiska/glukoneogena mellanprodukter.
Hos däggdjur förekommer PPP uteslutande i cytoplasman. Hos människor har den visat sig vara mest aktiv i levern, bröstkörtlarna och binjurebarken. PPP - reducerande är ett av de tre huvudsakliga sätten som kroppen skapar molekyler med kraft och står för cirka 60 % av NADPH produktionen hos människor. [ citat behövs ]
En av användningarna av NADPH i cellen är att förhindra oxidativ stress . Det minskar glutation via glutationreduktas , som omvandlar reaktivt H 2 O 2 till H 2 O genom glutationperoxidas . Om den saknas, skulle H 2 O 2 omvandlas till fria hydroxylradikaler genom Fenton-kemi , som kan attackera cellen. Erytrocyter, till exempel, genererar en stor mängd NADPH genom pentosfosfatvägen för att användas i reduktionen av glutation.
Väteperoxid genereras också för fagocyter i en process som ofta kallas en respiratorisk explosion .
Faser
Oxidativ fas
reduceras två molekyler av NADP + till NADPH , med hjälp av energin från omvandlingen av glukos-6-fosfat till ribulos-5-fosfat .
Hela uppsättningen av reaktioner kan sammanfattas enligt följande:
| Reaktanter | Produkter | Enzym | Beskrivning |
| Glukos 6-fosfat + NADP+ | → 6-fosfoglukono-5-lakton + NADPH | glukos 6-fosfatdehydrogenas | Dehydrering . Hydroxylen på kol 1 av glukos 6-fosfat förvandlas till en karbonyl, vilket genererar en lakton, och i processen genereras NADPH . |
| - lakton + H2O | → 6-fosfoglukonat + H + | 6-fosfoglukonolaktonas | Hydrolys |
| 6-fosfoglukonat + NADP + | → ribulos 5-fosfat + NADPH + CO 2 | 6-fosfoglukonatdehydrogenas | Oxidativ dekarboxylering . NADP + är elektronacceptorn, som genererar ytterligare en molekyl av NADPH , en CO 2 , och ribulos 5-fosfat . |
Den övergripande reaktionen för denna process är:
- Glukos 6-fosfat + 2 NADP + + H 2 O → ribulos 5-fosfat + 2 NADPH + 2 H + + CO 2
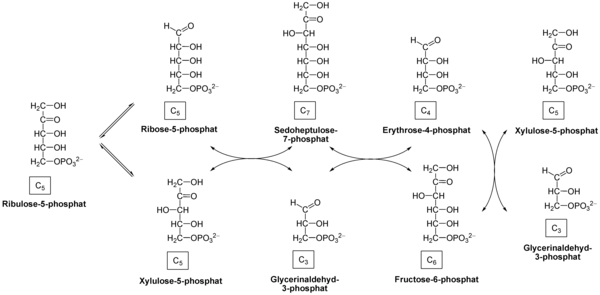
Icke-oxidativ fas
Netto reaktion: 3 ribulos-5-fosfat → 1 ribos-5-fosfat + 2 xylulos-5-fosfat → 2 fruktos-6-fosfat + glyceraldehyd-3-fosfat
förordning
Glukos-6-fosfatdehydrogenas är det hastighetskontrollerande enzymet för denna väg [ citat behövs ] . Det allosteriskt av NADP + och hämmas starkt av NADPH . Förhållandet NADPH:NADP + är det primära regleringssättet för enzymet och är normalt cirka 100:1 i levercytosol [ citat behövs ] . Detta gör cytosolen till en mycket reducerande miljö. En NADPH-användande väg bildar NADP + , vilket stimulerar glukos-6-fosfatdehydrogenas att producera mer NADPH. Detta steg hämmas också av acetyl CoA . [ citat behövs ]
G6PD -aktivitet regleras också post-translationellt av cytoplasmatiskt deacetylas SIRT2 . SIRT2-medierad deacetylering och aktivering av G6PD stimulerar oxidativ gren av PPP för att tillföra cytosolisk NADPH för att motverka oxidativ skada eller stödja de novo lipogenes .
Erytrocyter
Flera brister i aktivitetsnivån (ej funktion) av glukos-6-fosfatdehydrogenas har observerats vara associerade med resistens mot malariaparasiten Plasmodium falciparum bland individer av medelhavs- och afrikansk härkomst. Grunden för denna resistens kan vara en försvagning av det röda blodkroppsmembranet (erytrocyten är värdcellen för parasiten) så att den inte kan upprätthålla den parasitära livscykeln tillräckligt länge för produktiv tillväxt.
Se även
- G6PD-brist - En ärftlig sjukdom som stör pentosfosfatvägen
- RNA
- Tiaminbrist
- Frank Dickens FRS
- ^ Alfarouk, Khalid O.; Ahmed, Samrein BM; Elliott, Robert L.; Benoit, Amanda; Alqahtani, Saad S.; Ibrahim, Muntaser E.; Bashir, Adil HH; Alhoufie, Sari TS; Elhassan, Gamal O.; Wales, Christian C.; Schwartz, Laurent H.; Ali, Heyam S.; Ahmed, Ahmed; Forde, Patrick F.; Devesa, Jesus; Cardone, Rosa A.; Fais, Stefano; Harguindey, Salvador; Reshkin, Stephan J. (2020). "Pentosfosfatvägens dynamik i cancer och dess beroende av intracellulärt pH" . Metaboliter . 10 (7): 285. doi : 10.3390/metabo10070285 . PMC 7407102 . PMID 32664469 .
- ^ Alfarouk, Khalid O.; Ahmed, Samrein BM; Elliott, Robert L.; Benoit, Amanda; Alqahtani, Saad S.; Ibrahim, Muntaser E.; Bashir, Adil HH; Alhoufie, Sari TS; Elhassan, Gamal O.; Wales, Christian C.; Schwartz, Laurent H.; Ali, Heyam S.; Ahmed, Ahmed; Forde, Patrick F.; Devesa, Jesus; Cardone, Rosa A.; Fais, Stefano; Harguindey, Salvador; Reshkin, Stephan J. (2020). "Pentosfosfatvägens dynamik i cancer och dess beroende av intracellulärt pH" . Metaboliter . 10 (7): 285. doi : 10.3390/metabo10070285 . PMC 7407102 . PMID 32664469 .
- ^ Kruger, Nicholas J; von Schaewen, Antje (juni 2003). "Den oxidativa pentosfosfatvägen: struktur och organisation". Aktuell åsikt i växtbiologi . 6 (3): 236–246. doi : 10.1016/S1369-5266(03)00039-6 . PMID 12753973 .
- ^ Keller, Markus A.; Turchyn, Alexandra V.; Ralser, Markus (25 april 2014). "Icke-enzymatisk glykolys och pentosfosfatväg-liknande reaktioner i ett rimligt arkeiskt hav" . Molekylär systembiologi . 10 (4): 725. doi : 10.1002/msb.20145228 . PMC 4023395 . PMID 24771084 .
- ^ Immunologi vid MCG 1/cytotox
- ^ Voet Donald ; Voet Judith G (2011). Biochemistry (4:e upplagan). sid. 894. ISBN 978-0470-57095-1 .
- ^ Wang YP, Zhou LS, Zhao YZ, Wang SW, Chen LL, Liu LX, Ling ZQ, Hu FJ, Sun YP, Zhang JY, Yang C, Yang Y, Xiong Y, Guan KL, Ye D (juni 2014). "Reglering av G6PD-acetylering av SIRT2 och KAT9 modulerar NADPH-homeostas och cellöverlevnad under oxidativ stress" . EMBO Journal . 33 (12): 1304–20. doi : 10.1002/embj.201387224 . PMC 4194121 . PMID 24769394 .
- ^ Xu SN, Wang TS, Li X, Wang YP (sep 2016). "SIRT2 aktiverar G6PD för att öka NADPH-produktionen och främja leukemicellsproliferation" . Sci Rep . 6 : 32734. Bibcode : 2016NatSR...632734X . doi : 10.1038/srep32734 . PMC 5009355 . PMID 27586085 .
- ^ Cappadoro M, Giribaldi G, O'Brien E, et al. (oktober 1998). "Tidig fagocytos av glukos-6-fosfatdehydrogenas (G6PD)-bristiga erytrocyter parasiterade av Plasmodium falciparum kan förklara malariaskydd vid G6PD-brist. " Blod . 92 (7): 2527–34. doi : 10.1182/blod.V92.7.2527 . PMID 9746794 .
externa länkar
- Den kemiska logiken bakom pentosfosfatvägen
- Pentos+fosfat+väg vid US National Library of Medicine Medical Subject Headings (MeSH)
- Pentosfosfatväg Karta – Homo sapiens