Nogalamycin

|
|
| Identifierare | |
|---|---|
|
3D-modell ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.162.283 |
|
PubChem CID
|
|
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Egenskaper | |
| C39H49NO 16 _ _ _ _ | |
| Molar massa | 787,80 g/mol |
| Faror | |
| Arbetsmiljö och hälsa (OHS/OSH): | |
|
Huvudsakliga faror
|
kardiotoxisk |
| Besläktade föreningar | |
|
Besläktade föreningar
|
menogaril |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
Nogalamycin är ett antracyklinantibiotikum som produceras av jordbakterien Streptomyces nogalater . Det har antitumöregenskaper men det är också mycket kardiotoxiskt. Den mindre kardiotoxiska semisyntetiska analogen menogaril utvecklades på 1970-talet. För närvarande används inte nogalamycin och menogaril kliniskt.
Biosyntes
Antracyklinbiosyntes involverar konstruktionen av en aglykonkärna (med en typ II polyketidsyntas ) till vilken en eller flera sockerrester är fästa. Nogalamycin består av tre komponenter:
- nogalamycinon (svart), aglykonkärnan
- nogalos (magenta)
- nogalamin (grön)
Varje komponent byggs separat och ligeras sedan samman av två glykosyltransferaser. Alla maskineri associerade med biosyntesen av nogalamycin är belägna inom samma biosyntetiska genkluster av S. nogalater .
Nogalamycinonbiosyntes
Den biosyntetiska vägen mot aglykonkärnan av nogalamycin har bestämts genom en kombination av bioinformatisk analys och kloning av enskilda komponenter i den biosyntetiska vägen. Biosyntesvägen liknar den för aklavinon (aglykonkärnan i de flesta antracykliner, inklusive doxorubicin ), den enda skillnaden är att den första acylgruppen som laddas in i PKS är ett acetat snarare än ett propionat. Följande gener är involverade i biosyntesen av nogalamycinonens kärna:
- sno a1 (ketosyntas-α)
- sno a2 (ketosyntas-β kedjelängdsfaktor)
- sno a3 (acylbärarprotein)
- sno aD (ketoreduktas)
- sno aE (aromatas)
- sno aM (cyklas)
- sno aB (oxygenas)
- sno aC (metyltransferas)
- sno aL (cyklas)
- sno aF (ketoreduktas)
Nogalamin och nogalos biosyntes
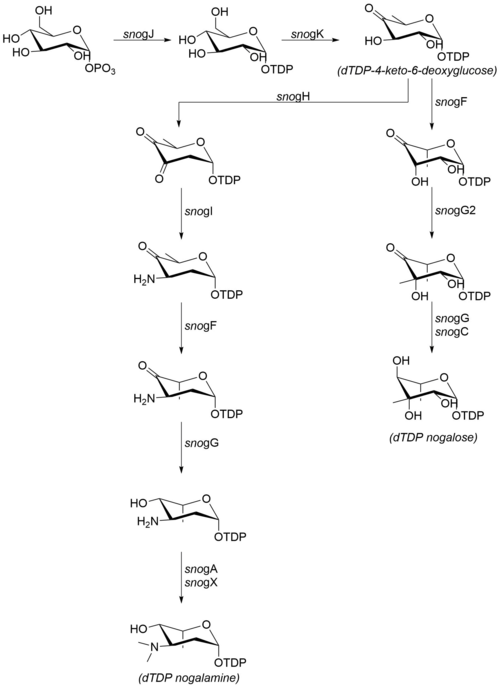
Sockerdelarna som är bundna till nogalamycinon produceras av glukos-1-fosfat . Även om stegen efter dTDP-4-keto-6-deoxiglukos inte har bekräftats in vitro , antyder den höga graden av sekvenslikhet med homologa enzymer från andra organismer att mekanismen fortsätter enligt detaljerna till höger. Följande enzymer är involverade i biosyntesen av nogalamin och nogalos:
- sno gJ (dTDP-glukossyntas)
- sno gK (4,6-dehydratas)
- sno gF (3,5-epimeras)
- sno gH (2,3-dehydratas)
- sno gN (okänd)
- sno gI (aminotransferas)
- sno gG (ketoreduktas)
- sno gC (ketoreduktas)
- sno gA (N-metyltransferas)
- sno gX (N-metyltransferas)
- sno gG2 (C-metyltransferas)
Observera att även om mycket av litteraturen hänvisar till den slutliga, permetylerade kolhydratdelen som "nogalos", tyder nyare data på att nogalosdelen på nogalamycin metyleras efter att nogalamycinonkärnan har glykosylerats.
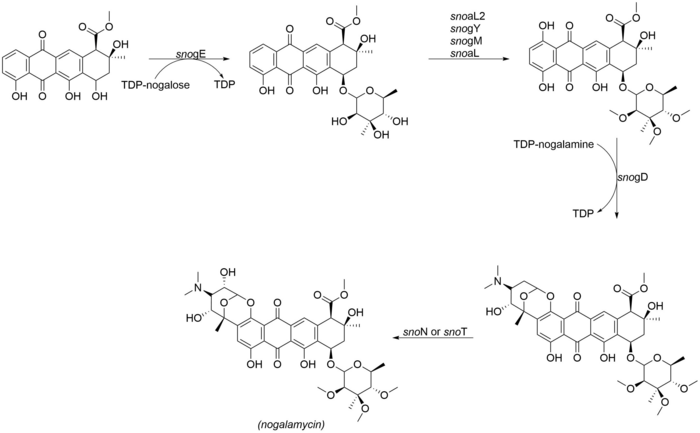
Nogalamycinonglykosylering och anpassning
Den mest anmärkningsvärda aspekten av strukturen av nogalamycin är den dubbla bindningen av nogalamin både genom O -glykosylering och även genom en kol-kol-bindning vid C2-positionen av nogalamycinonkärnan. Följande enzymer är involverade i de sista skräddarsysstegen av nogalamycin. Sno N och sno T är gener i nogalamycin-genklustret som sannolikt kommer att katalysera den slutliga hydroxyleringen:
- sno gE (glykosyltransferas)
- sno aL2 (hydroxylas)
- sno gY (O-metyltransferas)
- sno gM (förmodat O-metyltransferas)
- sno gL (förmodat O-metyltransferas)
- sno gD (glykosyltransferas)
- sno N/T