Hjärtmuskel
 | |
 | |
| Hjärtmuskeldetaljer | |
|---|---|
| _ | |
| Del av | Hjärtväggen _ |
| Identifierare | |
| latin | Textus muscularis striatus cardiacus |
| Maska | D009206 |
| TA98 | A12.1.06.001 |
| TA2 | 3950 |
| FMA | 9462 |
| Anatomisk terminologi | |
Hjärtmuskel (även kallad hjärtmuskel, myokardium, cardiomyocytes och cardiac myocytes ) är en av tre typer av ryggradsdjurs muskelvävnader , med de andra två är skelettmuskulatur och glatt muskulatur . Det är en ofrivillig, tvärstrimmig muskel som utgör huvudvävnaden i hjärtväggen . Hjärtmuskeln (myokardiet) bildar ett tjockt mellanlager mellan det yttre lagret av hjärtväggen ( hjärtsäcken ) och det inre lagret ( endokardiet ), med blod som tillförs via kranskärlscirkulationen . Den består av individuella hjärtmuskelceller sammanfogade av interkalerade skivor och omslutna av kollagenfibrer och andra ämnen som bildar den extracellulära matrisen .
Hjärtmuskeln drar ihop sig på ett liknande sätt som skelettmuskulaturen , men med några viktiga skillnader. Elektrisk stimulering i form av en hjärtaktionspotential utlöser frisättningen av kalcium från cellens inre kalciumförråd, det sarkoplasmatiska retikulumet . Ökningen av kalcium gör att cellens myofilament glider förbi varandra i en process som kallas excitation-kontraktionskoppling . Sjukdomar i hjärtmuskeln som kallas kardiomyopatier är av stor betydelse. Dessa inkluderar ischemiska tillstånd orsakade av en begränsad blodtillförsel till muskeln såsom angina och hjärtinfarkt .
Strukturera
Grov anatomi
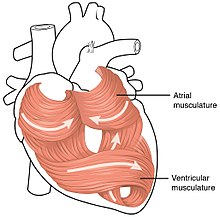
Hjärtmuskelvävnad eller myokardium utgör huvuddelen av hjärtat. Hjärtväggen är en struktur i tre lager med ett tjockt lager av myokard inklämt mellan det inre endokardiet och det yttre epikardium (även känt som det viscerala perikardiet). Det inre endokardiet kantar hjärtkamrarna, täcker hjärtklaffarna och förenar sig med endotelet som kantar blodkärlen som ansluter till hjärtat. På den yttre sidan av myokardiet finns epikardium som utgör en del av perikardsäcken som omger, skyddar och smörjer hjärtat.
Inom hjärtmuskeln finns flera ark av hjärtmuskelceller eller kardiomyocyter. De muskelark som lindas runt vänster kammare närmast endokardiet är orienterade vinkelrätt mot dem som är närmast epikardium. När dessa ark drar ihop sig på ett koordinerat sätt tillåter de ventrikeln att klämmas åt i flera riktningar samtidigt - longitudinellt (blir kortare från spets till bas), radiellt (blir smalare från sida till sida) och med en vridningsrörelse (liknande att vrida ut en fuktig trasa) för att pressa ut största möjliga mängd blod ur hjärtat med varje hjärtslag.
Att dra ihop hjärtmuskeln använder mycket energi och kräver därför ett konstant blodflöde för att ge syre och näringsämnen. Blod förs till myokardiet av kranskärlen . Dessa kommer från aortaroten och ligger på hjärtats yttre eller epikardiella yta. Blodet dräneras sedan bort av kranskärlen till höger förmak .
Mikroanatomi
Hjärtmuskelceller även kallade kardiomyocyter är de kontraktila myocyterna i hjärtmuskeln. Cellerna är omgivna av en extracellulär matris som produceras av stödjande fibroblastceller . Specialiserade modifierade kardiomyocyter, kända som pacemakerceller , ställer in rytmen för hjärtsammandragningarna. Pacemakercellerna är endast svagt kontraktila utan sarkomerer och är kopplade till närliggande kontraktila celler via gap junctions . De är belägna i den sinoatriala noden (den primära pacemakern) placerad på väggen i det högra förmaket, nära ingången till den övre hålvenen . Andra pacemakerceller finns i den atrioventrikulära noden (sekundär pacemaker).
Pacemakerceller bär de impulser som är ansvariga för hjärtats slag. De är fördelade i hela hjärtat och ansvarar för flera funktioner. spontant kunna generera och skicka ut elektriska impulser . De måste också kunna ta emot och svara på elektriska impulser från hjärnan. Slutligen måste de kunna överföra elektriska impulser från cell till cell. Pacemakerceller i den sinoatriala noden och atrioventrikulära noden är mindre och leder i en relativt långsam hastighet mellan cellerna. Specialiserade ledande celler i bunten av His och Purkinje-fibrerna är större i diameter och leder signaler i snabb takt.
Purkinje-fibrerna leder snabbt elektriska signaler; kranskärl för att föra näringsämnen till muskelcellerna, och vener och ett kapillärnätverk för att ta bort slaggprodukter.
Hjärtmuskelceller är de sammandragande cellerna som låter hjärtat pumpa. Varje kardiomyocyt behöver dra ihop sig i samordning med dess närliggande celler - känd som ett funktionellt syncytium - som arbetar för att effektivt pumpa blod från hjärtat, och om denna koordination går sönder då – trots att enskilda celler drar ihop sig – kanske hjärtat inte pumpar alls, som t.ex. kan förekomma under onormal hjärtrytm som t.ex. ventrikelflimmer .
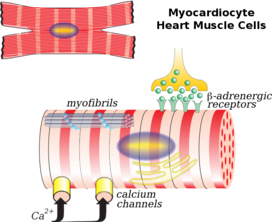
Sett genom ett mikroskop är hjärtmuskelcellerna ungefär rektangulära och mäter 100–150 μm gånger 30–40 μm. Individuella hjärtmuskelceller är sammanfogade i sina ändar av interkalerade skivor för att bilda långa fibrer. Varje cell innehåller myofibriller , specialiserade proteinsammandragande fibrer av aktin och myosin som glider förbi varandra. Dessa är organiserade i sarkomerer , de grundläggande kontraktila enheterna i muskelceller. Den regelbundna organiseringen av myofibriller till sarkomerer ger hjärtmuskelceller ett randigt eller tvärstrimmigt utseende när de tittas på genom ett mikroskop, liknande skelettmuskler. Dessa ränder orsakas av ljusare I-band som huvudsakligen består av aktin och mörkare A-band som huvudsakligen består av myosin.
Kardiomyocyter innehåller T-tubuli , påsar av cellmembran som löper från cellytan till cellens inre som hjälper till att förbättra kontraktionseffektiviteten. Majoriteten av dessa celler innehåller bara en kärna (vissa kan ha två centrala kärnor), till skillnad från skelettmuskelceller som innehåller många kärnor . Hjärtmuskelceller innehåller många mitokondrier som ger den energi som behövs för cellen i form av adenosintrifosfat (ATP), vilket gör dem mycket motståndskraftiga mot trötthet.
T-tubuli
T-tubuli är mikroskopiska rör som löper från cellytan till djupt inuti cellen. De är kontinuerliga med cellmembranet, är sammansatta av samma fosfolipiddubbelskikt och är öppna vid cellytan mot den extracellulära vätskan som omger cellen. T-tubuli i hjärtmuskeln är större och bredare än de i skelettmuskulaturen , men färre till antalet. I mitten av cellen går de samman och löper in i och längs cellen som ett tväraxiellt nätverk. Inuti cellen ligger de nära cellens inre kalciumförråd, det sarkoplasmatiska retikulumet . Här parar sig en enda tubuli med en del av det sarkoplasmatiska retikulumet som kallas en terminal cisterna i en kombination som kallas en diad .
Funktionerna hos T-tubuli inkluderar att snabbt överföra elektriska impulser som kallas aktionspotentialer från cellytan till cellens kärna och hjälper till att reglera koncentrationen av kalcium i cellen i en process som kallas excitation-kontraktionskoppling . De är också involverade i mekano-elektrisk återkoppling, vilket framgår av cellsammandragningsinducerad T-tubulärt innehållsutbyte (advektionsassisterad diffusion), vilket bekräftades av konfokala och 3D elektrontomografiobservationer.
Interkalerade skivor

Hjärtsyncytium är ett nätverk av kardiomyocyter sammankopplade med interkalerade skivor som möjliggör snabb överföring av elektriska impulser genom nätverket , vilket gör att syncytium kan agera i en koordinerad sammandragning av myokardiet. Det finns ett förmakssyncytium och ett ventrikulärt syncytium som är förbundna med hjärtanslutningsfibrer. Det elektriska motståndet genom interkalerade skivor är mycket lågt, vilket möjliggör fri diffusion av joner. Lättheten för jonrörelse längs hjärtmuskelfibrernas axlar är sådan att aktionspotentialer kan förflytta sig från en hjärtmuskelcell till nästa, med endast ett litet motstånd. Varje syncytium lyder allt eller inget-lagen .
Interkalerade skivor är komplexa vidhäftande strukturer som förbinder de enskilda kardiomyocyterna med ett elektrokemiskt syncytium (i motsats till skelettmuskeln, som blir ett flercelligt syncytium under embryonal utveckling ). Diskarna ansvarar främst för kraftöverföring under muskelkontraktion. Interkalerade skivor består av tre olika typer av cell-cell-övergångar: aktinfilamentförankringsfascian adherens junctions , desmosomer för mellanliggande filamentförankring och gap junctions . De tillåter aktionspotentialer att spridas mellan hjärtceller genom att tillåta passage av joner mellan celler, vilket ger depolarisering av hjärtmuskeln. De tre typerna av korsningar fungerar tillsammans som en enda area composita .
Under ljusmikroskopi ser interkalerade skivor ut som tunna, typiskt mörkfärgande linjer som delar intilliggande hjärtmuskelceller. De inskjutna skivorna löper vinkelrätt mot muskelfibrernas riktning. Under elektronmikroskopi verkar en interkalerad skivas väg mer komplex. Vid låg förstoring kan detta uppträda som en invecklad elektrontät struktur som ligger över platsen för den mörka Z-linjen. Vid hög förstoring verkar den interkalerade skivans väg ännu mer invecklad, med både längsgående och tvärgående områden som visas i längsgående snitt.
Fibroblaster
Hjärtfibroblaster är vitala stödjande celler i hjärtmuskeln. De kan inte ge kraftfulla sammandragningar som kardiomyocyter , utan är istället till stor del ansvariga för att skapa och underhålla den extracellulära matrisen som omger kardiomyocyterna. Fibroblaster spelar en avgörande roll för att svara på skada, såsom en hjärtinfarkt . Efter skada kan fibroblaster aktiveras och förvandlas till myofibroblaster – celler som uppvisar beteende någonstans mellan en fibroblast (genererar extracellulär matris) och en glatt muskelcell (förmåga att dra ihop sig). I denna egenskap kan fibroblaster reparera en skada genom att skapa kollagen medan de försiktigt drar ihop sig för att dra ihop kanterna på det skadade området.
Fibroblaster är mindre men fler än kardiomyocyter, och flera fibroblaster kan fästas på en kardiomyocyt samtidigt. När de är fästa till en kardiomyocyt kan de påverka de elektriska strömmarna som passerar över muskelcellens ytmembran, och i sammanhanget hänvisas till som elektriskt kopplade, som ursprungligen visades in vitro på 1960-talet, och slutligen bekräftades i inhemsk hjärtvävnad med hjälp av optogenetiska tekniker. Andra potentiella roller för fibroblaster inkluderar elektrisk isolering av hjärtledningssystemet och förmågan att transformera till andra celltyper inklusive kardiomyocyter och adipocyter .
Extracellulär matris
Den extracellulära matrisen (ECM) omger kardiomyocyten och fibroblasterna. ECM består av proteiner inklusive kollagen och elastin tillsammans med polysackarider (sockerkedjor) som kallas glykosaminoglykaner . Tillsammans ger dessa ämnen stöd och styrka till muskelcellerna, skapar elasticitet i hjärtmuskeln och håller muskelcellerna hydrerade genom att binda vattenmolekyler.
Matrisen i omedelbar kontakt med muskelcellerna kallas basalmembranet, huvudsakligen sammansatt av typ IV kollagen och laminin . Kardiomyocyter är kopplade till basalmembranet via specialiserade glykoproteiner som kallas integriner .
Utveckling
Människor föds med ett visst antal hjärtmuskelceller, eller kardiomyocyter, som ökar i storlek när hjärtat växer sig större under barndomens utveckling. Bevis tyder på att kardiomyocyter långsamt vänds under åldrandet, men mindre än 50 % av de kardiomyocyter som finns vid födseln ersätts under en normal livslängd. Tillväxten av individuella kardiomyocyter sker inte bara under normal hjärtutveckling, den sker också som svar på omfattande träning ( atletiskt hjärtsyndrom ), hjärtsjukdom eller hjärtmuskelskada som efter en hjärtinfarkt. En frisk vuxen kardiomyocyt har en cylindrisk form som är cirka 100 μm lång och 10–25 μm i diameter. Kardiomyocythypertrofi uppstår genom sarkomerogenes, skapandet av nya sarkomerenheter i cellen. Under hjärtvolymöverbelastning växer kardiomyocyter genom excentrisk hypertrofi. Kardiomyocyterna sträcker sig på längden men har samma diameter, vilket resulterar i ventrikulär dilatation. Under hjärttrycksöverbelastning växer kardiomyocyter genom koncentrisk hypertrofi. Kardiomyocyterna blir större i diameter men har samma längd, vilket resulterar i att hjärtväggen förtjockas.
Fysiologi
Hjärtmuskelns fysiologi har många likheter med skelettmuskulaturen . Den primära funktionen för båda muskeltyperna är att dra ihop sig, och i båda fallen börjar en sammandragning med ett karakteristiskt flöde av joner över cellmembranet, känt som en aktionspotential . Hjärtverkanspotentialen utlöser därefter muskelkontraktion genom att öka koncentrationen av kalcium i cytosolen .
Hjärtcykel
Hjärtcykeln är det mänskliga hjärtats prestanda från början av ett hjärtslag till början av nästa. Den består av två perioder: en under vilken hjärtmuskeln slappnar av och fylls på med blod, kallad diastole , efter en period av kraftig sammandragning och pumpning av blod, kallad systole . Efter tömning slappnar hjärtat omedelbart av och expanderar för att ta emot ytterligare ett tillflöde av blod som återvänder från lungorna och andra system i kroppen, innan det återigen drar ihop sig för att pumpa blod till lungorna och dessa system. Ett normalt fungerande hjärta måste expanderas helt innan det effektivt kan pumpa igen.
Vilofasen anses vara polariserad. Vilopotentialen under denna fas av takten separerar jonerna som natrium, kalium och kalcium . Myokardceller har egenskapen att automatisera eller spontant depolarisera . Detta är det direkta resultatet av ett membran som tillåter natriumjoner att långsamt komma in i cellen tills tröskeln för depolarisering nås. Kalciumjoner följer efter och förlänger depolariseringen ytterligare. När kalcium slutar röra sig inåt, rör sig kaliumjoner långsamt ut för att producera repolarisering. Den mycket långsamma repolariseringen av CMC-membranet är ansvarig för den långa refraktära perioden.
Mekanismen genom vilken kalciumkoncentrationerna i cytosolen stiger skiljer sig dock mellan skelett- och hjärtmuskel. I hjärtmuskeln består aktionspotentialen av ett inåtflöde av både natrium- och kalciumjoner. Flödet av natriumjoner är snabbt men mycket kortlivat, medan flödet av kalcium upprätthålls och ger platåfasen som är karakteristisk för hjärtmuskelns aktionspotentialer. Det jämförelsevis lilla flödet av kalcium genom kalciumkanalerna av L-typ utlöser en mycket större frisättning av kalcium från det sarkoplasmatiska retikulumet i ett fenomen som kallas kalciuminducerad kalciumfrisättning . Däremot i skelettmuskulaturen flödar minimalt med kalcium in i cellen under aktionspotential och istället är det sarkoplasmatiska retikulumet i dessa celler direkt kopplat till ytmembranet. Denna skillnad kan illustreras av observationen att hjärtmuskelfibrer kräver kalcium för att finnas i lösningen som omger cellen för att dra ihop sig, medan skelettmuskelfibrer kommer att dra ihop sig utan extracellulärt kalcium.
Under sammandragning av en hjärtmuskelcell glider de långa proteinmyofilamenten orienterade längs med cellens längd över varandra i det som kallas glidtrådsteorin . Det finns två typer av myofilament, tjocka filament som består av proteinet myosin och tunna filament som består av proteinerna aktin , troponin och tropomyosin . När de tjocka och tunna filamenten glider förbi varandra blir cellen kortare och fetare. I en mekanism som kallas cross-bridge cycling binder kalciumjoner till proteinet troponin, som tillsammans med tropomyosin sedan avslöjar viktiga bindningsställen på aktin. Myosin, i det tjocka filamentet, kan sedan binda till aktin och dra de tjocka filamenten längs de tunna filamenten. När koncentrationen av kalcium i cellen faller täcker troponin och tropomyosin återigen bindningsställena på aktin, vilket får cellen att slappna av.
Regeneration
Det var allmänt ansett att hjärtmuskelceller inte kunde regenereras. Detta motsägs dock av en rapport som publicerades 2009. Olaf Bergmann och hans kollegor vid Karolinska Institutet i Stockholm testade hjärtmuskelprover från personer födda före 1955 som hade väldigt lite hjärtmuskler runt hjärtat, många visade med funktionsnedsättning från denna abnormitet . Genom att använda DNA-prover från många hjärtan uppskattade forskarna att en 4-åring förnyar cirka 20 % av hjärtmuskelcellerna per år, och cirka 69 procent av hjärtmuskelcellerna hos en 50-åring genererades efter att han eller hon var född.
Ett sätt att regenerering av kardiomyocyter sker är genom delning av redan existerande kardiomyocyter under den normala åldrandeprocessen.
På 2000-talet rapporterades upptäckten av endogena hjärtstamceller från vuxna, och studier publicerades som hävdade att olika stamcellslinjer, inklusive benmärgsstamceller kunde differentiera till kardiomyocyter, och kunde användas för att behandla hjärtsvikt . Andra lag kunde dock inte replikera dessa fynd, och många av de ursprungliga studierna drogs senare tillbaka för vetenskapligt bedrägeri.
Skillnader mellan atria och ventriklar
Hjärtmuskeln bildar både hjärtats förmak och ventriklar. Även om denna muskelvävnad är mycket lik mellan hjärtkamrarna, finns det vissa skillnader. Myokardiet som finns i ventriklarna är tjockt för att möjliggöra kraftfulla sammandragningar, medan myokardiet i förmaken är mycket tunnare. De individuella myocyterna som utgör myokardiet skiljer sig också åt mellan hjärtkamrarna. Ventrikulära kardiomyocyter är längre och bredare, med ett tätare nätverk av T-tubuli . Även om de grundläggande mekanismerna för kalciumhantering är likartade mellan ventrikulära och atriella kardiomyocyter, är kalciumtransienten mindre och sönderfaller snabbare i atriella myocyter, med en motsvarande ökning av kalciumbuffrande kapacitet . Komplementet av jonkanaler skiljer sig mellan kamrarna, vilket leder till längre aktionspotentialvaraktigheter och effektiva refraktärperioder i ventriklarna. Vissa jonströmmar som IK (UR) är mycket specifika för förmakskardiomyocyter, vilket gör dem till ett potentiellt mål för behandlingar för förmaksflimmer .
Klinisk signifikans
Sjukdomar som påverkar hjärtmuskeln, kända som kardiomyopatier , är den vanligaste dödsorsaken i utvecklade länder . Det vanligaste tillståndet är kranskärlssjukdom , där blodtillförseln till hjärtat minskar . Kransartärerna blir smalare av bildandet av aterosklerotiska plack . Om dessa förträngningar blir tillräckligt allvarliga för att delvis begränsa blodflödet, kan syndromet angina pectoris uppstå. Detta orsakar vanligtvis bröstsmärtor under ansträngning som lindras av vila. Om en kransartär plötsligt blir mycket förträngd eller helt blockerad, vilket avbryter eller kraftigt minskar blodflödet genom kärlet, uppstår en hjärtinfarkt eller hjärtinfarkt. Om blockeringen inte lindras omedelbart genom medicinering , perkutan kranskärlsintervention eller operation , kan en hjärtmuskelregion bli permanent ärrad och skadad. En specifik kardiomyopati kan orsaka att hjärtmuskeln blir onormalt tjock ( hypertrofisk kardiomyopati ), onormalt stor ( dilaterad kardiomyopati ) eller onormalt stel ( restriktiv kardiomyopati ). Vissa av dessa tillstånd orsakas av genetiska mutationer och kan ärftas.
Hjärtmuskeln kan också skadas trots normal blodtillförsel. Hjärtmuskeln kan bli inflammerad i ett tillstånd som kallas myokardit , oftast orsakat av en virusinfektion men ibland orsakat av kroppens eget immunsystem . Hjärtmuskler kan också skadas av droger som alkohol, långvarigt högt blodtryck eller högt blodtryck , eller ihållande onormal hjärtslag . Många av dessa tillstånd, om de är tillräckligt allvarliga, kan skada hjärtat så mycket att hjärtats pumpfunktion minskar. Om hjärtat inte längre kan pumpa tillräckligt med blod för att tillgodose kroppens behov, beskrivs detta som hjärtsvikt .
Betydande skada på hjärtmuskelcellerna kallas myocytolys , vilket anses vara en typ av cellulär nekros definierad som antingen koagulativ eller kollikvativ.