Enolas
| fosfopyruvathydratas | |||||||||
|---|---|---|---|---|---|---|---|---|---|
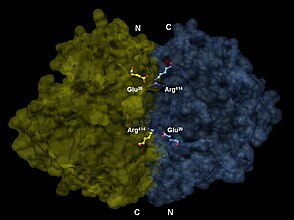
 Jäst enolasdimer.
| |||||||||
| Identifierare | |||||||||
| EG nr. | 4.2.1.11 | ||||||||
| CAS-nr. | 9014-08-8 | ||||||||
| Databaser | |||||||||
| IntEnz | IntEnz-vy | ||||||||
| BRENDA | BRENDA inträde | ||||||||
| ExPASy | NiceZyme-vy | ||||||||
| KEGG | KEGG inträde | ||||||||
| MetaCyc | Metabolisk väg | ||||||||
| PRIAM | profil | ||||||||
| PDB- strukturer | RCSB PDB PDBe PDB summa | ||||||||
| Genontologi | AmiGO / QuickGO | ||||||||
| |||||||||
| Enolas, N-terminal domän | |||||||||
|---|---|---|---|---|---|---|---|---|---|
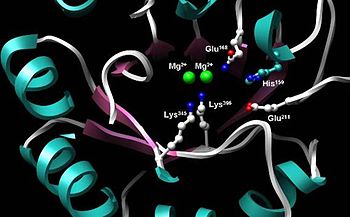
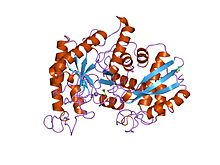 röntgenstruktur och katalytisk mekanism för hummerenolas
| |||||||||
| Identifierare | |||||||||
| Symbol | Enolase_N | ||||||||
| Pfam | PF03952 | ||||||||
| Pfam klan | CL0227 | ||||||||
| InterPro | IPR020811 | ||||||||
| PROSITE | PDOC00148 | ||||||||
| SCOP2 | 1els / SCOPe / SUPFAM | ||||||||
| |||||||||
| Enolas | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
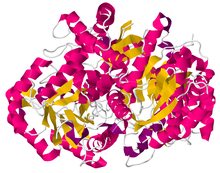 Kristallstruktur av dimert beta humant enolas ENO3 .
| |||||||||||
| Identifierare | |||||||||||
| Symbol | Enolas | ||||||||||
| Pfam | PF00113 | ||||||||||
| InterPro | IPR000941 | ||||||||||
| PROSITE | PDOC00148 | ||||||||||
| |||||||||||
Fosfopyruvathydratas , vanligtvis känt som enolas , är ett metalloenzym ( EC 4.2.1.11 ) som katalyserar omvandlingen av 2-fosfoglycerat (2-PG) till fosfoenolpyruvat (PEP), det nionde och näst sista steget av glykolys . Den kemiska reaktionen är:
- 2-fosfo- D -glycerat fosfoenolpyruvat + H 2 O
Fosfopyruvathydratas tillhör familjen lyaser , speciellt hydrolyaserna, som klyver kol-syrebindningar. Det systematiska namnet på detta enzym är 2-fosfo- D -glycerathydrolyas (fosfoenolpyruvatbildande) .
Reaktionen är reversibel, beroende på miljökoncentrationer av substrat. Det optimala pH-värdet för det mänskliga enzymet är 6,5. Enolas finns i alla vävnader och organismer som kan glykolyseras eller fermenteras . Enzymet upptäcktes av Lohmann och Meyerhof 1934 och har sedan dess isolerats från en mängd olika källor inklusive mänskliga muskler och erytrocyter . Hos människor brist på ENO1 kopplad till ärftlig hemolytisk anemi , medan ENO3-brist är kopplad till glykogenlagringssjukdom typ XIII.
Isozymer
Hos människor finns det tre subenheter av enolas, α , β och γ , var och en kodad av en separat gen som kan kombineras för att bilda fem olika isoenzymer : αα, αβ, αγ, ββ och γγ. Tre av dessa isoenzymer (alla homodimerer) finns vanligare i vuxna mänskliga celler än de andra:
- αα eller icke-neuronalt enolas (NNE). Även känd som enolas 1 . Finns i en mängd olika vävnader, inklusive lever, hjärna, njure, mjälte, fett. Det finns på någon nivå i alla normala mänskliga celler.
- ββ eller muskelspecifikt enolas (MSE). Även känd som enolas 3 . Detta enzym är till stor del begränsat till muskler där det finns i mycket höga nivåer i muskler.
- γγ eller neuronspecifikt enolas (NSE). Även känd som enolas 2 . Uttryckt i mycket höga nivåer i neuroner och neurala vävnader, där det kan stå för så mycket som 3% av det totala lösliga proteinet. Det uttrycks vid mycket lägre nivåer i de flesta däggdjursceller.
När de är närvarande i samma cell bildar olika isozymer lätt heterodimerer. [ citat behövs ]
Strukturera
Enolas är en medlem av den stora superfamiljen enolas . Den har en molekylvikt på 82 000-100 000 Dalton beroende på isoformen. I humant alfa-enolas är de två subenheterna antiparallella i orienteringen så att Glu 20 i en subenhet bildar en jonbindning med Arg 414 i den andra subenheten. Varje underenhet har två distinkta domäner. Den mindre N-terminala domänen består av tre α-helixar och fyra β-sheets . Den större C-terminala domänen börjar med två β-sheets följt av två α-helixar och slutar med en cylinder som består av alternerande β-sheets och α-helixar arrangerade så att β-beta-arken omges av α-helixarna. Enzymets kompakta, globulära struktur är ett resultat av betydande hydrofoba interaktioner mellan dessa två domäner.
Enolas är ett mycket konserverat enzym med fem rester på det aktiva stället som är särskilt viktiga för aktiviteten. Jämfört med vildtypsenolas har ett mutantenolas som skiljer sig vid antingen Glu 168 , Glu 211 , Lys 345 eller Lys 396 -resten en aktivitetsnivå som minskas med en faktor 105. Dessutom lämnar förändringar som påverkar His 159 mutant med endast 0,01 % av sin katalytiska aktivitet. En integrerad del av enolas är två Mg 2+ kofaktorer i det aktiva stället, som tjänar till att stabilisera negativa laddningar i substratet.
På senare tid har månskensfunktioner hos flera enolaser, såsom interaktion med plasminogen, väckt intresse för enzymernas katalytiska loopar och deras strukturella mångfald.
Mekanism
Med användning av isotopiska sönder föreslås den övergripande mekanismen för att omvandla 2-PG till PEP vara en E1cB-elimineringsreaktion som involverar en karbanjonintermediär. Följande detaljerade mekanism är baserad på studier av kristallstruktur och kinetik . När substratet, 2-fosfoglycerat, binder till α-enolas, koordinerar dess karboxylgrupp med två magnesiumjon-kofaktorer i det aktiva stället. Detta stabiliserar den negativa laddningen på det deprotonerade syret samtidigt som surheten hos alfavätet ökar. Enolases Lys 345 deprotonerar alfavätet, och den resulterande negativa laddningen stabiliseras genom resonans till karboxylatsyren och av magnesiumjonkofaktorerna. Efter skapandet av karbanjonmellanprodukten elimineras hydroxiden på C3 som vatten med hjälp av Glu 211 och PEP bildas.
Dessutom inträffar konformationsförändringar inom enzymet som underlättar katalys. I humant a-enolas roteras substratet till position vid bindning till enzymet på grund av interaktioner med de två katalytiska magnesiumjonerna, Gln167 och Lys396 . Rörelser av slingorna Ser 36 till His 43 , Ser 158 till Gly 162 och Asp 255 till Asn 256 tillåter Ser 39 att koordinera med Mg2 + och stänga av det aktiva stället. Förutom koordination med de katalytiska magnesiumjonerna, sänks pKa för substratets alfaväte också på grund av protonering av fosforylgruppen av His 159 och dess närhet till Arg 374 . Arg 374 får också Lys 345 i det aktiva stället att deprotoneras, vilket primerar Lys 345 för dess roll i mekanismen.
Diagnostiska användningsområden
I de senaste medicinska experimenten har enolaskoncentrationer tagits prov i ett försök att diagnostisera vissa tillstånd och deras svårighetsgrad. Till exempel, högre koncentrationer av enolas i cerebrospinalvätskan var starkare korrelerad till låggradigt astrocytom än andra testade enzymer ( aldolas , pyruvatkinas , kreatinkinas och laktatdehydrogenas ). Samma studie visade att den snabbaste takten av tumörtillväxt inträffade hos patienter med de högsta nivåerna av CSF-enolas. Ökade nivåer av enolas har också identifierats hos patienter som nyligen har drabbats av en hjärtinfarkt eller cerebrovaskulär olycka . Det har dragits slutsatsen att nivåer av CSF-neuronspecifikt enolas, serum -NSE och kreatinkinas (typ BB) är indikativa vid den prognostiska bedömningen av hjärtstoppsoffer. Andra studier har fokuserat på det prognostiska värdet av NSE-värden hos cerebrovaskulära olycksoffer.
Autoantikroppar mot alfa-enolas är associerade med reumatoid artrit och det sällsynta syndromet som kallas Hashimotos encefalopati .
Inhibitorer
Småmolekylära inhibitorer av enolas har syntetiserats som kemiska prober (substrat-analoger) av enzymets katalytiska mekanism och på senare tid har de undersökts som potentiella behandlingar för cancer och infektionssjukdomar. De flesta inhibitorer har metallkelaterande egenskaper och binder till enzym genom interaktioner med den strukturella magnesiumatomen Mg(A). Den mest potenta av dessa är fosfonoacetohydroxamat, som i sin oprotonerade form har pM-affinitet för enzymet. Den har strukturell likhet med den förmodade katalytiska mellanprodukten, mellan PEP och 2-PG. Försök har gjorts att använda denna hämmare som ett antitrypanosomläkemedel, och på senare tid, som ett anticancermedel, specifikt vid glioblastom som är enolasbrist på grund av homozygot deletion av ENO1 -genen som en del av 1p36-tumörsuppressorn locus ( syntetisk dödlighet ). En naturlig produkt fosfonatantibiotikum , SF2312 ( CAS 107729-45-3), som är aktiv mot grampositiva och negativa bakterier, särskilt under anaeroba förhållanden, är en högpotenshämmare av Enolase 4zcw som binder på liknande sätt som foshphonoacetohydroxamate 4za0 . SF2312 hämmar enolasaktivitet i både eukaryotiskt och prokaryot ursprung, vilket återspeglar den starka evolutionära bevarandet av enolas och det gamla ursprunget till glykolysvägen. SF2312 är en kiral molekyl med endast 3S-enantiomeren som visar Enolashämmande aktivitet och biologisk aktivitet mot bakterier. På senare tid har ett derivat av SF2312, kallat HEX, och en prodrug därav, POMHEX, visat sig utöva antineoplastisk aktivitet mot ENO1-deleterat gliom i en preklinisk intrakraniell ortotopisk musmodell. Ett allosteriskt bindemedel, ENOblock, beskrevs initialt som en hämmare av enolas, men visade sig senare inte hämma enzymet, utan snarare störa den enzymatiska analysen av enolas in vitro. ENOblock visade sig förändra den cellulära lokaliseringen av enolas, vilket påverkar dess sekundära, icke-glykolytiska funktioner, såsom transkriptionsreglering. Efterföljande analys med användning av en kommersiell analys visade också att ENOblock kan hämma enolasaktivitet i biologiska sammanhang, såsom celler och djurvävnader. Metylglyoxal har också beskrivits som en hämmare av humant enolas.
Enolashämmare har undersökts prekliniskt för behandling av olika mikrobiella patogener, såväl som inom precisionsonkologi för tumörer med 1p36 homozygota deletioner, som saknar ENO1.
Fluor är en känd konkurrent till enolasens substrat 2-PG. Fluor kan ett komplex med magnesium och fosfat, som binder i det aktiva stället i stället för 2-PG. En studie fann att fluor kunde hämma bakteriellt enolas in vitro . Fluoridanjonens enolashämmande aktivitet kan bidra till fluortandkrämens anti-kavitetseffekt genom att begränsa produktionen av mjölksyra (en glykolysprodukt som kräver enolas). [ läkarintyg behövs ]
Vidare läsning
- Holt A, Wold F (december 1961). "Isoleringen och karakteriseringen av kaninmuskelenolas" . Journal of Biological Chemistry . 236 (12): 3227–3231. doi : 10.1016/S0021-9258(18)94000-7 . PMID 13908561 .
- Boyer, PD, Lardy, H. och Myrback, K. (Eds.), The Enzymes, 2nd ed., vol. 5, Academic Press, New York, 1961, sid. 471-494.
- Westhead EW, Mclain G (augusti 1964). "En rening av brygger- och bagerijästanolas som ger en enda aktiv komponent" . Journal of Biological Chemistry . 239 (8): 2464–2468. doi : 10.1016/S0021-9258(18)93875-5 . PMID 14235523 .
externa länkar
- Enolas vid US National Library of Medicine Medical Subject Headings (MeSH)