Androgen deprivationsterapi
| Androgen deprivationsterapi | |
|---|---|
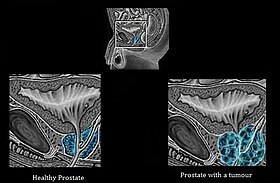 Skillnader mellan en frisk prostata och en prostata med en tumör
| |
| Andra namn | Androgen suppression terapi |
| Specialitet | onkologi |
Androgen deprivation therapy ( ADT ), även kallad androgen suppression therapy , är en antihormonbehandling vars huvudsakliga användning är vid behandling av prostatacancer . Prostatacancerceller kräver vanligtvis androgenhormoner, såsom testosteron , för att växa. ADT minskar nivåerna av androgenhormoner, med droger eller kirurgi , för att förhindra att prostatacancercellerna växer. De farmaceutiska metoderna inkluderar antiandrogener och kemisk kastrering .
Flera studier har dragit slutsatsen att ADT har visat nytta hos patienter med metastaserande sjukdom, och som ett komplement till strålbehandling hos patienter med lokalt avancerad sjukdom, såväl som hos de med ogynnsam medelrisk eller högrisk lokaliserad sjukdom. Hos patienter med lågriskprostatacancer har dock ADT inte visat någon överlevnadsfördel och betydande skada, såsom impotens, diabetes och benförlust.
Behandlingen kan också eliminera cancerceller genom att inducera androgenbrist-inducerad senescens . Att sänka androgennivåerna eller hindra dem från att komma in i prostatacancerceller får ofta prostatacancer att krympa eller växa långsammare under en tid. Denna behandling måste dock kombineras med strålbehandling (RT) eftersom ADT i sig inte utrotar cancern ; det minskar bara dess aggressivitet.
Typer
Metod baserad på kirurgi
- Orkiektomi (kirurgisk kastration)
- Den består av att ta bort testiklarna , det organ där androgener syntetiseras, från cancerpatienten. Det är den mest radikala behandlingen för att stoppa produktionen av androgener. Dessutom är det den enklaste och billigaste. Den största nackdelen är att kirurgisk kastration är en permanent metod.
Metoder baserade på droger
- Syntesen av testosteron förmedlas av en kedja av processer som startar i hjärnan. När kroppen upptäcker en låg nivå av testosteron, hypotalamus att producera LHRH . LHRH aktiverar syntesen av LH (luteiniserande hormon) i hypofysen. LH inducerar testosteronsyntes i testiklarna. Det finns två olika läkemedel, LHRH-agonister och antagonister, som båda sänker mängden testosteron som tillverkas av testiklarna. De verkar genom att hämma bildandet av LH i hypofysen. LHRH-agonisterna producerar en plötslig ökning av nivåerna av testosteron följt av en enorm sjunkande process som kallas flare , medan LHRH-antagonister direkt minskar mängden testosteron. LHRH-agonister och -antagonister som används i androgendeprivationsterapi inkluderar leuprorelin (leuprolid) , goserelin , triptorelin , histrelin , buserelin och degarelix .
- Dessa läkemedel injiceras under huden och uppnår samma resultat som kirurgisk kastration . Kemisk kastrering kan vara att föredra framför kirurgisk kastration [ citat behövs ] eftersom det håller testiklarna intakta.
- Antiandrogenterapi Binjurarna
- upptäcktes som ett annat centrum för androgenproduktion även efter en kastreringsprocess . Därför utvecklades en kompletterande behandling som använder antiandrogener för att blockera kroppens förmåga att använda alla androgener. Prostataceller innehåller en androgenreceptor (AR), som när den stimuleras av androgener som testosteron främjar tillväxt och upprätthåller prostata-differentiering. Dessa pro-tillväxt-signaler kan dock vara problematiska när de uppstår i en cancercell. Antiandrogener kan komma in i celler och förhindra bindningen av testosteron till receptorproteinerna, på grund av deras högre affinitet för androgenreceptorn.
- De huvudsakliga antiandrogenerna är cyproteronacetat , flutamid , nilutamid , bicalutamid och enzalutamid , som alla administreras i oral pillerform.
- Nya antiandrogener som är inriktade på testosteronsyntes ( abirateronacetat och seviteronel ) eller AR-kärntranslokation ( enzalutamid , apalutamid och darolutamid ), såväl som kombinerade terapier ( galeteron ) har nyligen utvecklats och kan fungera för att bättre målinrikta androgenkänsliga celler i kombination med ADT. Men även dessa kan ha negativa negativa roller i utvecklingen av CRPC .
Effekter på mäns sexualitet
Normal manlig sexualitet verkar bero på mycket specifika och komplicerade hormonella mönster som inte är helt förstådda. En studie tyder på att ADT kan förändra den hormonbalans som är nödvändig för manlig sexuell aktivitet. När män åldras minskar testosteronnivåerna med cirka 1 % per år efter 30 års ålder; det är dock viktigt att avgöra om lågt testosteron beror på normalt åldrande, eller på en sjukdom, såsom hypogonadism. Testosteron spelar en betydande roll i sexuell funktion; därför kan naturligt sjunkande nivåer av testosteron leda till minskning av normal sexuell funktion. Ytterligare minskningar av serumtestosteron kan ha en negativ inverkan på normal sexuell funktion, vilket leder till försämrad livskvalitet.
Erektil dysfunktion är inte ovanligt efter radikal prostatektomi och män som genomgår ADT utöver detta kommer sannolikt att visa ytterligare nedgång i sin förmåga att delta i penetrerande samlag, såväl som sin önskan att göra det. En studie som tittar på skillnaderna mellan att använda GnRH-A (och androgenhämmare) eller en orkiektomi rapporterar skillnader i sexuellt intresse, upplevelsen av erektioner och prevalensen av att delta i sexuell aktivitet. Män som inte rapporterade något sexuellt intresse ökade från 27,6 % till 63,6 % efter orkiektomi och från 31,7 % till 58,0 % efter GnRH-A; män som inte upplevde några erektioner ökade från 35,0 % till 78,6 %; och män som inte rapporterade att de ägnade sig åt sexuell aktivitet ökade från 47,9 % till 82,8 % efter orkiektomi och 45,0 % till 80,2 %. Denna studie tyder på att GnRH-A och orkiektomi hade liknande effekter på sexuell funktion. En ond cirkel där sänkta testosteronnivåer leder till minskad sexuell aktivitet, vilket i sin tur gör att både fria och totala testosteronnivåer sjunker ytterligare. Detta visar vikten av androgener för att upprätthålla sexuella strukturer och funktioner.
Skadliga effekter
Även om inriktning på androgenaxeln har klara terapeutiska fördelar, är dess effektivitet tillfällig, eftersom prostatatumörceller anpassar sig för att överleva och växa. Avlägsnandet av androgener har visat sig aktivera epitelial-mesenkymal övergång (EMT), neuroendokrin transdifferentiering (NEtD) och cancerstamcellsliknande genprogram.
- EMT har etablerat roller för att främja biologiska fenotyper associerade med tumörprogression (migration/invasion, tumörcellsöverlevnad, cancerstamcellsliknande egenskaper, motståndskraft mot strålning och kemoterapi) i flera mänskliga cancertyper.
- NEtD i prostatacancer är associerad med resistens mot terapi, viscerala metastaser och aggressiv sjukdom.
- Cancerstamcellsfenotyper är associerade med sjukdomsåterfall, metastaser och cellöverlevnad i cirkulation som cirkulerande tumörceller .
Således tillhandahåller aktivering av dessa program via hämning av androgenaxeln en mekanism genom vilken tumörceller kan anpassa sig för att främja sjukdomsåterfall och -progression.
Orkiektomi, LHRH-analoger och LHRH-antagonister kan alla orsaka liknande biverkningar, på grund av förändringar i nivåerna av könshormoner (testosteron).
Ett program har utvecklats för patienter och deras partner för att känna igen och hantera de mer betungande biverkningarna av androgenbristbehandling. Ett program är uppbyggt kring 2014 års bok "Androgen Deprivation Therapy: An Essential Guide for Prostate Cancer Patients and Their Loved Ones", som godkänns av Canadian Urological Association.
Nyligen genomförda studier har visat att ADT kan öka risken för Alzheimers sjukdom eller demens. Den ökade risken kan vara associerad med varaktigheten av ADT. Medan vissa studier rapporterar en nedgång i vissa områden av kognitiv funktion såsom rumsliga förmågor , uppmärksamhet och verbalt minne i samband med ADT, är bevis som helhet motsägelsefulla. Användbara förebyggande insatser kan inkludera social interaktion , fysisk träning och en " medelhavsdiet ", bland annat. Det finns ytterligare en liten risk för hjärtarytmier.
