Spanska sjukan forskning
|
|
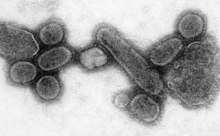
| Influensa A-virus subtyp H1N1 | |
|---|---|
| En elektronmikrofotografi av viruset som orsakade 1918 års influensa. | |
| Virusklassificering | |
| (orankad): | Virus |
| Rike : | Riboviria |
| Rike: | Orthornavirae |
| Provins: | Negarnaviricota |
| Klass: | Insthoviricetes |
| Beställa: | Articulavirales |
| Familj: | Orthomyxoviridae |
| Släkte: | Alfainfluensavirus |
| Arter: | |
| Serotyp: |
Influensa A-virus subtyp H1N1
|
| Provtagna stammar | |
|
|
Spanska sjukan forskning rör studier om orsakerna och egenskaperna hos den spanska sjukan , en mängd olika influensa som 1918 var ansvarig för den värsta influensapandemin i modern historia. Många teorier om uppkomsten och utvecklingen av den spanska sjukan fanns kvar i litteraturen, men det var inte förrän 2005, när olika prover av lungvävnad återfanns från amerikanska soldater från första världskriget och från en inupiatisk kvinna begravd i permafrost i en massgrav i Brevig Mission, Alaska , att betydande genetisk forskning möjliggjordes.
Virusets ursprung
Det finns två rådande teorier som vanligtvis postuleras. En teori av genetisk Alfred virus W. Crosby är att virusstammen har sitt ursprung i Fort Riley , Kansas , genom två genetiska mekanismer - drift och antigenisk förändring - i hos fjäderfä och svin som fortet föd upp för lokal konsumtion. Även om initiala data från en nyligen genomförd rekonstruktion av viruset antydde att det hoppade direkt från fåglar till människor , utan att resa genom svin, har detta sedan dess betvivlats. En forskare publicerad 2004 hävdade att sjukdomen hittades i Haskell County, Kansas , redan i januari 1918. Ett liknande och ännu mer dödligt virus hade setts tidigare i brittiska läger i Frankrike och i Aldershot.
Tidigare utredningsarbete publicerat år 2000 av ett team ledd av den brittiske virologen John Oxford från St Bartholomew's Hospital och Royal London Hospital , antydde att en brittisk brittisk truppuppläggningsläger i Étaples , Frankrike, var i centrum för 1918 års influensapandemi eller vid åtminstone ett betydande prekursorvirus till det. Det hade inträffat en mystisk luftvägsinfektion vid militärbasen under vintern 1915–1916.
Upptäckt av virala genom


1995 undrade Jeffery Taubenberger från US Armed Forces Institute of Pathology ( AFIP) om det kunde vara möjligt att återvinna viruset från 1918 års influensapandemi från offrens torkade och fixerade vävnader. Han och hans kollegor testade 10 objektglas av vävnadsprov och 2 kom ut positiva. Taubenberger, Ann H. Reid och Thomas G. Fanning kunde amplifiera korta segment av den virala nukleinsyran med användning av polymeraskedjereaktion (PCR) . Resultaten publicerades i tidskriften Science i mars 1997.
Den 20 augusti 1997 tog Johan Hultin prover av 1918 års influensa från det frusna liket av en infödd Alaskan kvinna som begravts i nästan åtta decennier i permafrost nära Brevig Mission, Alaska . Han tog med proverna till ett team i Rockville, Maryland, ledd av Jeffery Taubenberger från US Armed Forces Institute of Pathology (AFIP). Brevig Mission förlorade cirka 85 % av sin befolkning till 1918 års influensa i november 1918. Ett av de fyra återvunna proverna innehöll livsdugligt genetiskt material från viruset. Detta prov gav forskarna en förstahandsmöjlighet att studera viruset, som inaktiverades med guanidiniumtiocyanat före transport. Detta prov och andra som hittades i AFIP-arkiv gjorde det möjligt för forskare att fullständigt analysera de kritiska genstrukturerna för 1918-viruset.
- "Vi har nu identifierat tre fall: Brevig Mission -fallet och två arkivfall som representerar de enda kända källorna till genetiskt material från 1918 års influensavirus", säger Taubenberger, chef för AFIP:s avdelning för molekylär patologi och huvudutredare för projektet.
De arkiverade obduktionsproverna hade tagits från WWI-arméns meniga Roscoe Vaughan och James Downs.
Den 6 februari 2004 av tidskriften Science rapporterade att två forskarlag, ett ledd av Sir John Skehel, chef för National Institute for Medical Research i London , ett annat av professor Ian Wilson från The Scripps Research Institute i San Diego , hade lyckats syntetisera hemagglutininproteinet som var ansvarigt för influensautbrottet 1918. De gjorde detta genom att sätta ihop DNA från ett lungprov från en inuitkvinna begravd i Alaskas tundra och ett antal bevarade prover från amerikanska soldater från första världskriget . Teamen hade analyserat genens struktur och upptäckt hur subtila förändringar av formen på en proteinmolekyl hade tillåtit den att flytta från fåglar till människor med sådana förödande effekter.
meddelade Tumpey och andra forskare vid Centers for Disease Control and Prevention (CDC) i Atlanta , Georgia, och Mount Sinai School of Medicine i New York , att den (~13 kbp) genetiska sekvensen av 1918 års influensa stam, en undertyp av fågelstam H1N1 , hade rekonstruerats med hjälp av historiska vävnadsprover och en liten del av RNA:t från en modern stam.
Egenskaper hos virus
Influensavirus har en relativt hög mutationshastighet som är karakteristisk för RNA-virus . H5N1 - viruset har muterats till en mängd olika typer med olika patogena profiler; vissa patogena för en art men inte andra, vissa patogena för flera arter. Förmågan hos olika influensastammar att visa artselektivitet beror till stor del på variation i hemagglutiningenerna. Genetiska mutationer i hemagglutiningenen som orsakar enstaka aminosyrasubstitutioner kan väsentligt förändra förmågan hos virala hemagglutininproteiner att binda till receptorer på värdcellernas yta. Sådana mutationer i aviärt H5N1-virus kan förändra virusstammar från att vara ineffektiva när det gäller att infektera mänskliga celler till att vara lika effektiva för att orsaka mänskliga infektioner som vanligare typer av humana influensavirus.
I juli 2004 rapporterade forskare under ledning av H. Deng från Harbin Veterinary Research Institute , Harbin , Kina, och Robert Webster från St. Jude Children's Research Hospital , Memphis, Tennessee , resultat av experiment där möss hade exponerats för 21 isolat av bekräftade H5N1-stammar erhållna från ankor i Kina mellan 1999 och 2002. De fann "ett tydligt tidsmönster av progressivt ökande patogenicitet." Resultat som rapporterades av Webster i juli 2005 avslöjar ytterligare progression mot patogenicitet hos möss och längre virusutsöndring från ankor.
I december 2008 visade forskning av Yoshihiro Kawaoka från University of Wisconsin närvaron av de tre specifika generna (benämnda PA, PB1 och PB2) och ett nukleoprotein som härrörde från H1N1 1918 influensaprover var tillräckligt för att utlösa liknande symtom i djurförsök.
Forskning om viral patogenes
Ny forskning av Taubenberger et al. har föreslagit att 1918 års virus, liksom H5N1, kunde ha uppstått direkt från ett fågelinfluensavirus. Men forskare vid University of Virginia och Australian National University har föreslagit att det kan finnas en alternativ tolkning av de data som används i Taubenberger et al. papper. Taubenberger et al. svarade på dessa brev och försvarade deras ursprungliga tolkning.
Annan forskning av Tumpey och kollegor som rekonstruerade H1N1 -viruset från 1918 kom till slutsatsen att det framför allt var polymerasgenerna och HA- och NA-generna som orsakade den extrema virulensen av detta virus. Den 18 januari 2007, Kobasa et al. rapporterade att infekterade apor ( Macaca fascicularis ) uppvisade klassiska symtom från pandemin 1918 och dog av en cytokinstorm .
Sekvenserna för polymerasproteinerna (PA, PB1 och PB2) från 1918-viruset och efterföljande humana virus skiljer sig endast med 10 aminosyror från fågelinfluensavirus. Virus med 7 av de 10 aminosyrorna på de mänskliga influensaplatserna har redan identifierats i H5N1 som för närvarande cirkulerar . Detta har fått vissa forskare att föreslå att andra mutationer kan komma till ytan och göra H5N1-viruset kapabelt att överföras från människa till människa.
En annan viktig faktor är förändringen av HA-proteinet till en bindningspreferens för alfa-2,6- sialinsyra (den huvudsakliga formen som finns i mänskliga luftvägar). I fågelvirus binder HA-proteinet företrädesvis till alfa-2,3 sialinsyra, som är huvudformen i tarmkanalen. Det har visats att endast en enda aminosyraförändring kan resultera i förändringen av denna bindningspreferens. Sammantaget kan bara en handfull mutationer behöva äga rum för att fågelinfluensan H5N1 ska bli ett pandemiskt virus som det från 1918. Det är dock viktigt att notera att sannolikheten för mutation inte indikerar sannolikheten för utvecklingen av ett sådant virus. stam, eftersom några av de nödvändiga mutationerna kan begränsas genom att stabilisera selektion .
Blodplasma som en effektiv behandling
I händelse av en annan pandemi har amerikanska militärforskare föreslagit att man ska återanvända en behandling från den dödliga pandemin 1918 för att dämpa effekterna av influensa: Vissa militärläkare injicerade svårt drabbade patienter med blod eller blodplasma från människor som hade återhämtat sig från influensa. Data som samlats in under den tiden tyder på att blodinjektionsbehandlingen minskade dödligheten med så mycket som 50 procent.
Marinforskare har lanserat ett test för att se om 1918 års behandling kommer att fungera mot dödlig asiatisk fågelinfluensa. Resultaten hittills har varit ofullständiga. Human H5N1 -plasma kan vara en effektiv, aktuell och allmänt tillgänglig behandling för nästa influensapandemi. En ny internationell studie som använder moderna datainsamlingsmetoder skulle vara en svår, långsam process. Med hänvisning till den månader långa väntan på ett vaccin för nästa pandemi, anser många influensaexperter att 1918 års metod är något att överväga.
I den världsomspännande influensapandemin 1918 , "provade läkare allt de visste, allt de någonsin hört talas om, från den uråldriga konsten att blöda patienter, till administrering av syre, till att utveckla nya vacciner och sera (främst mot vad vi nu kallar Hemophilus influenzae - en namnet kommer från det faktum att det ursprungligen ansågs vara det etiologiska medlet – och flera typer av pneumokocker). Endast en terapeutisk åtgärd visade någon antydan till framgång: Transfusion av blod från återhämtade patienter till nya offer."
Se även
- Influensaforskning
- Mark Sykes – uppgrävning av ett brittiskt influensaoffer i Storbritannien
- Yoshihiro Kawaoka – konstruerade och återskapade ett virus för att studera hur det fungerar och hur influensan naturligt muterar
- Kirsty Duncan - ledde misslyckad expedition för att hitta influensavirus i permafrost vid Longyearbyen , Svalbard, Norge