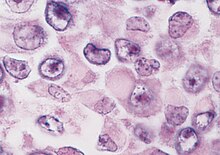
Malign rhabdoid tumör
| Malign rhabdoid tumör | |
|---|---|
| Specialitet |
Onkologi |
Malign rhabdoidtumör (MRT) är en mycket aggressiv form av tumör som ursprungligen beskrevs som en variant av Wilms tumör, som i första hand är en njurtumör som främst förekommer hos barn.
MRT beskrevs först som en variant av Wilms tumör i njuren 1978. MRT är en sällsynt och mycket malign neoplasm hos barn . Rabdoida tumörer utanför njuren rapporterades senare i många vävnader inklusive levern, mjukvävnaden och det centrala nervsystemet . Flera fall av primär intrakraniell MRT har rapporterats sedan dess erkännande som en separat enhet 1978. Termen rhabdoid användes på grund av dess likhet med rabdomyosarkom under ljusmikroskopet. Den exakta patogenesen av MRT är okänd.
Lillhjärnan är den vanligaste platsen för primär intracerebral MRT (dvs atypisk teratoid rhabdoidtumör ) . Biggs et al. var de första som rapporterade en primär intrakraniell MRT runt 1987.
Även om ursprungscellen inte är känd, har cytogenetiska studier föreslagit en gemensam genetisk grund för rhabdoida tumörer oavsett lokalisering med vanliga avvikelser i kromosom 22 .
Genetik
Det har rapporterats fall av ett barn som har både atypiska teratoida rhabdoida tumörer i hjärnan och rhabdoida tumörer i njuren. Weeks and associates rapporterade om 111 renala rhabdoidfall varav 13,5% också hade en malignitet i centrala nervsystemet. Det har antagits att en könslinje-INI-mutation kan predisponera ett barn för dessa tumörer. Det har förekommit några referenser i litteraturen som anspelar på en ny diagnos som kallas rhabdoid predispositionssyndrom relaterat till genen hSNF5/INI1 .
Dessa tumörer har associerats med mutationer i den SWI/SNF-relaterade matrisassocierade aktinberoende regulatorn av kromatinunderfamilj B-medlem 1 ( SMARCB1 ) belägen på den långa armen av kromosom 22 (22q11) och transkriptionsaktivatorn BRG1/ATP-beroende kromatin remodeler ( SMARCA4 ) lokaliserad på den korta armen av kromosom 19 (19p13.2).
Rabdoida tumörer i njure och hjärna
Betydande debatt har fokuserats på huruvida atypiska teratoida rhabdoida tumörer är samma som rhabdoida tumörer i njuren (dvs bara extrarenala MRT). [ citat behövs ]
Erkännande av att både atypiska CNS-teratoida/rhabdoida tumörer och MRTs har deletioner av INI1-genen i kromosom 22 indikerar att rhabdoida tumörer i njure och hjärna är identiska eller närbesläktade enheter, även om CNS-varianten tenderar att ha sina mutationer på Taxon [medicinsk citat ] behövs ] 9 och MRT på andra ställen. Denna observation är inte förvånande eftersom rhabdoida tumörer på båda platserna har liknande histologiska, kliniska och demografiska egenskaper. Dessutom har 10-15 % av patienterna med MRT synkrona eller metakrona hjärntumörer, av vilka många är andra primära maligna rhabdoida tumörer. Denna likhet utesluter sammansatta rhabdoida tumörer, som förekommer främst hos vuxna. [ citat behövs ]
Diagnos
Den histologiska diagnosen av maligna rabdoida tumörer beror på identifiering av karakteristiska rhabdoidceller - stora celler med excentriskt placerade kärnor och riklig, eosinofil cytoplasma. Histologin kan dock vara heterogen och diagnosen MRT kan ofta vara svår. Felklassificeringar kan förekomma.
I MRT fungerar INI1-genen (SMARCB1) på kromosom 22q som en klassisk tumörsuppressorgen. Inaktivering av INI1 kan ske via deletion, mutation eller förvärvad UPD.
I en nyligen genomförd studie identifierade singelnukleotidpolymorfism array karyotyping deletioner eller LOH på 22q i 49/51 rhabdoida tumörer. Av dessa var 14 kopieneutral LOH (eller förvärvad UPD), som kan detekteras genom SNP-array-karyotyping, men inte av FISH, cytogenetik eller array-CGH. MLPA upptäckte en enda exon homozygot deletion i ett prov som var under upplösningen för SNP-matrisen. SNP array karyotyping kan användas för att skilja till exempel ett medulloblastom med en isokromosom 17q från en primär rhabdoidtumör med förlust av 22q11.2. När så anges kan molekylär analys av INI1 med användning av MLPA och direkt sekvensering sedan användas. När de tumörrelaterade förändringarna har hittats kan en analys av könscells-DNA från patienten och föräldrarna göras för att utesluta en ärftlig eller de novo könscellsmutation eller deletion av INI1, så att lämpliga riskbedömningar av återfall kan göras.
Prognos
Oavsett lokalisering är alla rhabdoida tumörer mycket aggressiva, har en dålig prognos och tenderar att förekomma hos barn under två år.
Se även
Litteratur
- Donner LR, Wainwright LM, Zhang F, Biegel JA (2007). "Mutation av INI1-genen i sammansatt rhabdoidtumör i endometrium" . Brum. Patol . 38 (6): 935–9. doi : 10.1016/j.humpath.2006.12.003 . PMC 1963314 . PMID 17376508 .
- Jeffrey S Dome, MD; D Ashley Hill, MD (8 januari 2007). "Malign rhabdoidtumör" . EMedicine från WebMD .
- Perry A, Fuller CE, Judkins AR, Dehner LP, Biegel JA (2005). "INI1-uttryck bibehålls i sammansatta rhabdoida tumörer, inklusive rhabdoida meningiom" . Mod. Patol . 18 (7): 951–8. doi : 10.1038/modpathol.3800375 . PMID 15761491 .
- Biegel JA, Fogelgren B, Wainwright LM, Zhou JY, Bevan H, Rorke LB (2000). "Germline INI1-mutation hos en patient med en atypisk teratoidtumör i centrala nervsystemet och renal rhabdoidtumör" ( abstrakt sida) . Gener Kromosomer Cancer . 28 (1): 31–7. doi : 10.1002/(SICI)1098-2264(200005)28:1<31::AID-GCC4>3.0.CO;2-Y . PMID 10738300 . S2CID 21250260 .
- Huret J, Sevenet N (2000). "Rhabdoid predisponionssyndrom" . Atlas of Genetics and Cytogenetics in Oncology and Hematology (1): 31–7. Arkiverad från originalet 2005-12-26.
- Weeks DA, Beckwith JB, Mierau GW, Luckey DW (1989). "Rhabdoid tumör i njure. En rapport med 111 fall från National Wilms' Tumor Study Pathology Center". American Journal of Surgical Pathology . 13 (6): 439–58. doi : 10.1097/00000478-198906000-00001 . PMID 2543225 . S2CID 19589843 .