ILC2
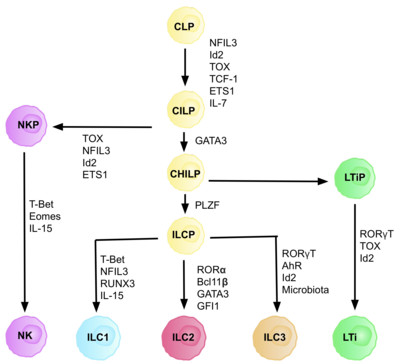
ILC2- celler eller typ 2 medfödda lymfoidceller är en typ av medfödda lymfoidceller . Ej att förväxla med ILC. De härrör från vanliga lymfoida stamceller och tillhör den lymfoida härstamningen . Dessa celler saknar antigenspecifik B- eller T-cellsreceptor på grund av bristen på rekombinationsaktiverande gen . ILC2 producerar typ 2-cytokiner (t.ex. IL-4 , IL-5 , IL-9 , IL-13 ) och är involverade i svar på helminter , allergener , vissa virus, såsom influensavirus och cancer.
Celltypen beskrevs först 2001 som icke-B/icke-T-celler, som producerade IL-5 och IL-13 som svar på IL-25 och uttryckte MHC klass II och CD11c . År 2006 identifierades en liknande cellpopulation i ett fall av helminthic infektion. Namnet "ILC2" föreslogs inte förrän 2013. De identifierades tidigare i litteraturen som naturliga hjälparceller, nuocyter eller medfödda hjälparceller 2. Man tror att ILC2s är ganska gamla celltyper med förfäderpopulationer som dyker upp i lamprey och benfiskar .
Parasitisk infektion
ILC2 spelar den avgörande rollen att utsöndra typ 2-cytokiner som svar på stora extracellulära parasiter. De uttrycker karakteristiska ytmarkörer och receptorer för kemokiner , som är involverade i distributionen av lymfoida celler till specifika organplatser. De kräver IL-7 för sin utveckling, vilket aktiverar två transkriptionsfaktorer (båda krävs av dessa celler) - RORα och GATA3 . Efter stimulering med Th2-polariserande cytokiner, som huvudsakligen utsöndras av epitel (t.ex. IL-25 , IL-33 , TSLP , prostaglandin D2 och leukotrien D4 ), börjar ILC2 producera IL-5 , IL-13 , IL-9 , IL- 4 snabbt. ILC2s är kritiska för primära svar på lokala Th2-antigener, t.ex. helminter och virus, och det är därför ILC2s finns i överflöd i vävnaderna i hud, lungor, lever och tarm. Det har observerats att ILC2 har sitt ursprung i tarmen, kommer in i lymfkärlen och sedan cirkulerar i blodomloppet så att de kan migrera till andra organ för att hjälpa till att bekämpa parasitinfektionen. Handeln är delvis sfingosin-1-fosfatberoende . Till exempel, under en Nippostrongylus brasiliensis -infektion, bidrar ILC2s till maskrensning genom att producera det essentiella cytokinet IL-13 . IL-13 som utsöndras av ILC2s främjar också migration av aktiverade lungdendritiska celler in i den dränerande lymfkörteln, vilket sedan resulterar i naiv T-cellspriming och differentiering till Th2-celler .
Luftvägsvirusinfektion
Det har observerats att ILC2 aktiveras vid luftvägsvirusinfektioner hos möss och människor. Till exempel, under influensa A-virusinfektion , som inducerar IL-33- produktion, aktiveras ILC2: er och driver luftvägarnas hyperkänslighet. Ett annat exempel är en respiratorisk syncytialvirusinfektion , där ILC2 bidrar genom att vara den huvudsakliga källan till IL-13 tidigt i infektionen, vilket leder till hyperrespons i luftvägarna och ökad slemproduktion.
Allergi, atopisk dermatit och astma
ILC2 spelar en mängd olika roller vid allergi . I första hand tillhandahåller de en källa till typ 2-cytokiner som orkestrerar det allergiska immunsvaret. De producerar en profil av signaler som svar på pro-allergena cytokiner IL-25 och IL-33 som liknar de som produceras som svar på helminthic infektion. Deras bidrag till denna signalering verkar vara jämförbart med T-cellers. Som svar på allergenexponering i lungorna producerar ILC2s IL-13, ett nödvändigt cytokin i patogenesen av allergiska reaktioner. Detta svar verkar vara oberoende av T- och B-celler. Vidare har allergiska reaktioner som liknar astmaliknande symtom inducerats hos möss som saknar T- och B-celler med hjälp av IL-33. Det har också visat sig att ILC2 finns i högre koncentrationer i vävnader där allergiska symtom förekommer, såsom i näspolyper hos patienter med kronisk rhinosinusit och huden från patienter med atopisk dermatit .
Barriärfunktion
ILC2s är kända för att anrikas i fettassocierade lymfoidkluster (FALC) i mesenterierna . IL-5 som utsöndras av ILC2s är väsentlig tillväxtfaktor för B1 B-celler och därför viktig i produktionen av IgA -antikroppar. Förutom typ 2-cytokinerna kan ILC2s också producera IL-6 , vilket inducerar antikroppsproduktion av B-celler, fungerar som en tillväxtfaktor för plasmablaster och bidrar till reglering av T-follikulära hjälparceller.
ILC2 är också kända för att finnas i FALC i pleurahålan . Efter att ha stimulerats via IL-33 under en infektion börjar de utsöndra IL-5, vilket leder till en aktivering av B1 B-celler och produktion av IgM -antikroppar. ILC2 är den dominerande populationen av ILC i lungorna. Genom att producera IL-13 kan de initiera sammandragning av glatt muskulatur och slemsekretion , men även bägarcellshyperplasi om IL-13 överuttrycks. Dessutom hjälper ILC2s lungsårläkning efter influensainfektion genom att utsöndra amfiregulin . Förutom lungor kan ILC2-populationer också hittas i mänskliga näs- och tonsillvävnader .
Fettvävnad homeostas
ILC2s är avgörande för att upprätthålla homeostas i mager och frisk fettvävnad. ILC2s som finns i visceral fettvävnad producerar IL-5-, IL-13- och metionin-enkefalinpeptider efter långvarig exponering för IL-33 . IL-5 som utsöndras av ILC2s i fettvävnad är avgörande för rekrytering och underhåll av eosinofiler . Vidare stöder produktion av IL-13 och IL-4 av ILC2 och eosinofiler upprätthållandet av alternativt aktiverade M2-makrofager och glukoshomeostas.
Forskning identifierade dysregulerade svar av ILC2s i fettvävnad som en faktor i utvecklingen av fetma hos möss eftersom ILC2s också spelar en viktig roll i energihomeostas. Metionin-enkefalinpeptider producerade av ILC2s verkar direkt på adipocyter för att uppreglera UCP1 och främja uppkomsten av beige adipocyter i vit fettvävnad. Beige och brun fettvävnad är specialiserade på termogenes . Processen att beiga leder till ökad energiförbrukning och minskat fettinnehåll.