Fraktionering av kolisotoper i syrehaltig fotosyntes
Fotosyntes omvandlar koldioxid till kolhydrater via flera metabola vägar som ger energi till en organism och företrädesvis reagerar med vissa stabila isotoper av kol . Den selektiva anrikningen av en stabil isotop över en annan skapar distinkta isotopfraktioneringar som kan mätas och korreleras bland syrehaltiga fototrofer . Graden av kolisotopfraktionering påverkas av flera faktorer, inklusive organismens metabolism, anatomi, tillväxthastighet och miljöförhållanden. Att förstå dessa variationer i kolfraktionering mellan arter är användbart för biogeokemiska studier, inklusive rekonstruktion av paleoekologi , växtutveckling och karakterisering av näringskedjor .

Oxygenisk fotosyntes är en metabolisk väg som underlättas av autotrofer , inklusive växter, alger och cyanobakterier. Denna väg omvandlar oorganisk koldioxid från atmosfären eller vattenmiljön till kolhydrater , med hjälp av vatten och energi från ljus, och frigör sedan molekylärt syre som en produkt. Organiskt kol innehåller mindre av den stabila isotopen Carbon-13 , eller 13 C, i förhållande till det ursprungliga oorganiska kolet från atmosfären eller vattnet eftersom fotosyntetisk kolfixering involverar flera fraktioneringsreaktioner med kinetiska isotopeffekter . Dessa reaktioner genomgår en kinetisk isotopeffekt eftersom de begränsas genom att övervinna en aktiveringsenergibarriär . Den lättare isotopen har ett högre energitillstånd i kvantbrunnen av en kemisk bindning, vilket gör att den företrädesvis kan formas till produkter. Olika organismer fixerar kol genom olika mekanismer, vilket återspeglas i de olika isotopsammansättningarna över fotosyntetiska vägar (se tabell nedan och förklaring av notationen i avsnittet "Mätning av kolisotoper"). Följande avsnitt kommer att beskriva de olika syrehaltiga fotosyntetiska vägarna och vad som bidrar till deras associerade deltavärden.
| Väg | δ 13 C (‰) |
|---|---|
| C3 | -20 till -37 |
| C4 | -12 till -16 |
| KAM | -10 till -20 |
| Växtplankton | -18 till -25 |
Kolisotopmätning
Kol på jorden förekommer naturligt i två stabila isotoper, med 98,9 % i form av 12 C och 1,1 % i 13 C . Förhållandet mellan dessa isotoper varierar i biologiska organismer på grund av metaboliska processer som selektivt använder en kolisotop framför den andra, eller "fraktionerar" kol genom kinetiska eller termodynamiska effekter. Oxygenisk fotosyntes sker i växter och mikroorganismer genom olika kemiska vägar, så olika former av organiskt material återspeglar olika förhållanden av 13 C isotoper. Att förstå dessa variationer i kolfraktionering mellan arter tillämpas i isotopgeokemi och ekologiska isotopstudier för att förstå biokemiska processer, etablera näringskedjor eller modellera kolets kretslopp genom geologisk tid.
Kolisotopfraktioneringar uttrycks genom att använda deltanotation av δ 13 C ("delta tretton C"), som rapporteras i promille ( promille , ‰). δ 13 C definieras i förhållande till Vienna Pee Dee Belemnite (VPDB, 13 C/ 12 C = 0,01118) som en etablerad referensstandard . Detta kallas ett "deltavärde" och kan beräknas från formeln nedan:
Fotosyntesreaktioner
Den kemiska vägen för oxygenisk fotosyntes fixerar kol i två steg: de ljusberoende reaktionerna och de ljusoberoende reaktionerna.
De ljusberoende reaktionerna fångar ljusenergi för att överföra elektroner från vatten och omvandla NADP + , ADP och oorganiskt fosfat till energilagringsmolekylerna NADPH och ATP . Den övergripande ekvationen för de ljusberoende reaktionerna är i allmänhet:
2 H 2 O + 2 NADP + + 3 ADP + 3 Pi + ljus → 2 NADPH + 2 H + + 3 ATP + O 2
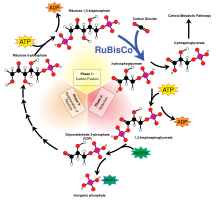
De ljusoberoende reaktionerna genomgår Calvin-Benson-cykeln , där energin från NADPH och ATP används för att omvandla koldioxid och vatten till organiska föreningar via enzymet RuBisCO . Den övergripande allmänna ekvationen för de ljusoberoende reaktionerna är följande:
3 CO2 + 9 ATP + 6 NADPH + 6 H + → C3H6O3 - fosfat + 9 ADP + 8 Pi + 6 NADP + + 3 H2O
3-kolprodukterna (C 3 H 6 O 3 -fosfat) i Calvin-cykeln omvandlas senare till glukos eller andra kolhydrater såsom stärkelse , sackaros och cellulosa .
Fraktionering via RuBisCO
Den stora fraktioneringen av 13C i fotosyntesen beror på karboxyleringsreaktionen, som utförs av enzymet ribulos-1,5-bisfosfatkarboxylasoxygenas, eller RuBisCO . RuBisCO katalyserar reaktionen mellan en femkolsmolekyl, ribulos-1,5-bisfosfat (förkortat RuBP) och CO 2 för att bilda två molekyler av 3-fosfoglycerinsyra (förkortat PGA). PGA reagerar med NADPH för att producera 3-fosfoglyceraldehyd .
Isotopfraktionering på grund av Rubisco (form I) karboxylering enbart förutspås vara en 28‰ utarmning i genomsnitt. Fraktioneringsvärdena varierar dock mellan organismer, allt från en 11‰ utarmning observerad i coccolithophorid alger till en 29‰ utarmning observerad i spenat . RuBisCO orsakar en kinetisk isotopeffekt eftersom 12 CO 2 och 13 CO 2 tävlar om samma aktiva ställe och 13 C har en väsentligt lägre reaktionshastighet.
13 C fraktioneringsmodell
Förutom de särskiljande effekterna av enzymatiska reaktioner påverkar diffusionen av CO 2 -gas till karboxyleringsstället i en växtcell också isotopfraktionering. Beroende på typ av växt (se avsnitt nedan) måste extern CO 2 transporteras genom gränsskiktet och stomata och in i det inre gasutrymmet i en växtcell, där det löses upp och diffunderar till kloroplasten. En gass diffusivitet är omvänt proportionell mot kvadratroten av dess molekylära reducerade massa (relativt till luft), vilket gör att 13 CO 2 är 4,4‰ mindre diffusiv än 12 CO 2 .
En rådande modell för fraktionering av atmosfärisk CO 2 i växter kombinerar isotopeffekterna av karboxyleringsreaktionen med isotopeffekterna från gasdiffusion in i växten i följande ekvation:
Var:
- δ 13 C- prov är organismens deltavärde för 13 C-sammansättning
- δ 13 C atm är delta-värdet för atmosfärisk CO 2 , vilket är = -7,8‰
- diskrimineringen på grund av diffusion a = 4,4‰
- karboxyleringsdiskrimineringen b = 30‰
- c a är partialtrycket för CO 2 i den yttre atmosfären, och
- c i är partialtrycket för CO 2 i de intercellulära utrymmena.
Denna modell, härledd ab initio , beskriver generellt fraktionering av kol i de flesta växter, vilket underlättar C3-kolfixering . Modifieringar har gjorts i denna modell med empiriska fynd. Flera ytterligare faktorer, som inte ingår i denna allmänna modell, kommer dock att öka eller minska 13C -fraktioneringen mellan arter. Sådana faktorer inkluderar den konkurrerande syresättningsreaktionen av RuBisCO, anatomiska och tidsmässiga anpassningar till enzymaktivitet och variationer i celltillväxt och geometri. De isotopiska fraktioneringarna av olika fotosyntetiska vägar kännetecknas unikt av dessa faktorer, som beskrivs nedan.
I C3-anläggningar
En C3-växt använder C3-kolfixering , en av de tre metaboliska fotosyntesvägarna som också inkluderar C4 och CAM (beskrivs nedan). Dessa växter kallas "C3" på grund av trekolföreningen ( 3-fosfoglycerinsyra eller 3-PGA) som produceras av CO 2 -fixeringsmekanismen i dessa växter. Denna C3-mekanism är det första steget i Calvin-Benson-cykeln, som omvandlar CO 2 och RuBP till 3-PGA .
C3-växter är den vanligaste typen av växter och trivs vanligtvis under måttlig solljusintensitet och temperaturer, CO 2 -koncentrationer över 200 ppm och rikligt med grundvatten. C3-växter växer inte bra i mycket varma eller torra områden, där C4- och CAM-växter är bättre anpassade.
Isotopfraktioneringarna i C3-kolfixering uppstår från de kombinerade effekterna av CO 2 -gasdiffusion genom växtens stomata och karboxyleringen via RuBisCO . Stomatal konduktans diskriminerar de tyngre 13 C med 4,4‰. RuBisCO-karboxylering bidrar till en större diskriminering på 27‰.
RuBisCO-enzymet katalyserar karboxyleringen av CO 2 och 5-kolsockret, RuBP , till 3-fosfoglycerat , en 3-kolförening genom följande reaktion:
Produkten 3-fosfoglycerat är utarmad i 13° C på grund av den kinetiska isotopeffekten av ovanstående reaktion. Den totala 13C -fraktioneringen för C3-fotosyntes varierar mellan -20 och -37‰.
Det breda intervallet av variationer i delta-värden som uttrycks i C3-växter moduleras av stomatalkonduktansen, eller hastigheten för CO 2 som kommer in eller vattenånga ut, de små porerna i överhuden på ett blad. δ 13 C för C3-växter beror på förhållandet mellan stomatal konduktans och fotosynteshastighet, vilket är en bra proxy för vattenanvändningseffektiviteten i bladet. C3-anläggningar med hög vattenanvändningseffektivitet tenderar att vara mindre fraktionerade i 13 C (dvs. δ 13 C är relativt mindre negativa) jämfört med C3-anläggningar med låg vattenanvändningseffektivitet.
I C4-anläggningar

C4-växter har utvecklat C4-kolfixeringsvägen för att spara vattenförlust, och är därför vanligare i varma, soliga och torra klimat. Dessa växter skiljer sig från C3-växter eftersom CO 2 initialt omvandlas till en fyrkolsmolekyl, malat , som transporteras till buntceller, frigörs tillbaka som CO 2 och först därefter går in i Calvin-cykeln. Däremot utför C3-växter direkt Calvin-cykeln i mesofyllceller, utan att använda en CO 2 -koncentrationsmetod. Malat, fyra-kolföreningen är namnet på "C4" fotosyntes. Denna väg gör det möjligt för C4-fotosyntesen att effektivt överföra CO 2 till RuBisCO-enzymet och upprätthålla höga koncentrationer av CO 2 i buntmantelceller . Dessa celler är en del av den karakteristiska kranzbladanatomin , som rumsligt separerar fotosyntetiska celltyper i ett koncentriskt arrangemang för att ackumulera CO 2 nära RuBisCO.
Dessa kemiska och anatomiska mekanismer förbättrar RuBisCOs förmåga att fixera kol snarare än att utföra dess slösaktiga oxygenasaktivitet . RuBisCO oxygenasaktiviteten, som kallas fotorespiration , gör att RuBP-substratet går förlorat till syresättning och förbrukar energi vid att göra det. Anpassningarna av C4-växter ger en fördel jämfört med C3-vägen, som förlorar effektivitet på grund av fotorespiration. Förhållandet mellan fotorespiration och fotosyntes i en växt varierar med miljöförhållandena, eftersom minskad CO 2 och förhöjda O 2 koncentrationer skulle öka effektiviteten av fotorespiration. Atmosfärisk CO 2 på jorden minskade abrupt vid en punkt för mellan 32 och 25 miljoner år sedan. Detta gav en selektiv fördel för utvecklingen av C4-vägen, vilket kan begränsa fotorespirationshastigheten trots den minskade omgivande CO 2 . Idag står C4-växter för ungefär 5 % av växtbiomassan på jorden, men ungefär 23 % av markbunden kolfixering. Typer av växter som använder C4-fotosyntes inkluderar gräs och ekonomiskt viktiga grödor, som majs , sockerrör , hirs och sorghum .
Isotopfraktionering skiljer sig mellan C4-kolfixering och C3, på grund av den rumsliga separationen i C4-växter av CO 2 -fångning (i mesofyllcellerna) och Calvin-cykeln (i buntmantelcellerna). I C4-växter omvandlas kol till bikarbonat , fixeras till oxaloacetat via enzymet fosfoenolpyruvat (PEP) karboxylas och omvandlas sedan till malat . Malatet transporteras från mesofyllet till buntceller , som är ogenomträngliga för CO 2 . Den inre CO 2 koncentreras i dessa celler när malat reoxideras och sedan dekarboxyleras tillbaka till CO 2 och pyruvat. Detta gör det möjligt för RuBisCO att utföra katalys medan intern CO 2 är tillräckligt hög för att undvika den konkurrerande fotorespirationsreaktionen. Delta-värdet i C4-vägen är -12 till -16‰ utarmat i 13 C på grund av de kombinerade effekterna av PEP-karboxylas och RuBisCO.
Den isotopiska diskrimineringen i C4-vägen varierar i förhållande till C3-vägen på grund av de ytterligare kemiska omvandlingsstegen och aktiviteten hos PEP-karboxylas. Efter diffusion in i stomata koncentrerar omvandlingen av CO 2 till bikarbonat de tyngre 13 C. Den efterföljande fixeringen via PEP-karboxylas är därmed mindre utarmad i 13 C än den från Rubisco: ca 2‰ utarmad i PEP-karboxylas, mot 29‰ i RuBisCO . Emellertid läcker en del av det isotopiskt tunga kolet som fixeras av PEP-karboxylas ut ur buntmantelcellerna. Detta begränsar det kol som är tillgängligt för RuBisCO, vilket i sin tur minskar dess fraktioneringseffekt. Detta står för att det totala deltavärdet i C4-anläggningar är -12 till -16 ‰.
I CAM-anläggningar
Växter som använder Crassulacean-syrametabolism , även känd som CAM-fotosyntes, separerar temporärt sina kemiska reaktioner mellan dag och natt. Denna strategi modulerar stomatal konduktans för att öka vattenanvändningseffektiviteten, så den är väl anpassad för torra klimat. Under natten öppnar CAM-växter stomata för att tillåta CO 2 att komma in i cellen och genomgå fixering till organiska syror som lagras i vakuoler. Detta kol frigörs till Calvin-cykeln under dagen, när stomata stängs för att förhindra vattenförlust, och ljusreaktionerna kan driva den nödvändiga ATP- och NADPH-produktionen. Denna väg skiljer sig från C4-fotosyntes eftersom CAM-växter separerar kol genom att lagra fixerad CO 2 i vesiklar på natten och sedan transportera den för användning under dagen. Således koncentrerar CAM-växter CO 2 tillfälligt för att förbättra RuBisCO-effektiviteten, medan C4-växter koncentrerar CO 2 rumsligt i buntmantelceller. Fördelningen av växter som använder CAM-fotosyntes inkluderar epifyter (t.ex. orkidéer , bromeliads ) och xerofyter (t.ex. suckulenter , kaktusar ).
I Crassulacean-syrametabolism kombinerar isotopfraktionering effekterna av C3-vägen på dagtid och C4-vägen på natten. På natten, när temperaturen och vattenförlusten är lägre, diffunderar CO 2 genom stomata och producerar malat via fosfenolpyruvatkarboxylas. Under följande dag stängs stomata, malat dekarboxyleras och CO 2 fixeras av RuBisCO. Enbart denna process liknar den för C4-växter och ger karakteristiska C4-fraktioneringsvärden på ungefär -11‰. Men på eftermiddagen kan CAM-växter öppna sina stomata och utföra C3-fotosyntes. Enbart på dagtid har CAM-växter ungefär -28‰ fraktionering, karakteristiskt för C3-växter. Dessa kombinerade effekter ger δ 13 C -värden för CAM-anläggningar i intervallet -10 till -20‰.
Förhållandet 13 C till 12 C i CAM-växter kan indikera den tidsmässiga separationen av CO 2 -fixering, vilket är omfattningen av biomassa som härrör från nattlig CO 2 -fixering i förhållande till dygns CO 2 -fixering. Denna distinktion kan göras eftersom PEP-karboxylas, enzymet som ansvarar för nettoupptag av CO 2 på natten, särskiljer 13 C mindre än RuBisCO, som är ansvarigt för CO 2 -upptag dagtid. CAM-växter som fixerar CO 2 primärt på natten skulle förutsägas visa δ 13 C -värden som mer liknar C4-växter, medan CO 2 -fixering dagtid skulle visa δ 13 C -värden mer lika C3-växter.
I växtplankton
Till skillnad från landväxter, där CO 2 -diffusionen i luft är relativt snabb och vanligtvis inte begränsar, är diffusionen av löst CO 2 i vatten betydligt långsammare och kan ofta begränsa kolfixeringen i växtplankton. Eftersom gasformig CO 2(g) löses i vattenhaltig CO 2(aq) fraktioneras den genom både kinetiska och jämviktseffekter som är temperaturberoende. I förhållande till växter kan den lösta CO 2 -källan för växtplankton anrikas i 13 C med cirka 8‰ från atmosfärisk CO 2 .
Isotopfraktionering av 13 C genom fytoplanktonfotosyntes påverkas av diffusionen av extracellulär vattenhaltig CO 2 in i cellen, den RuBisCO-beroende celltillväxthastigheten och cellgeometrin och ytan. Användningen av bikarbonat och kolkoncentreringsmekanismer i växtplankton skiljer isotopfraktioneringen från växternas fotosyntetiska vägar.
Skillnaden mellan intracellulära och extracellulära CO 2 -koncentrationer återspeglar CO 2 -behovet hos en växtplanktoncell, som är beroende av dess tillväxthastighet. Förhållandet mellan efterfrågan på kol och utbudet styr diffusionen av CO 2 in i cellen och är negativt korrelerad med storleken på kolfraktioneringen av växtplankton. Tillsammans tillåter dessa samband fraktionering mellan CO 2(aq) och växtplanktonbiomassa att användas för att uppskatta tillväxthastigheten för växtplankton.
Tillväxthastigheten ensam svarar dock inte för observerad fraktionering. Flödet av CO 2(aq) in i och ut ur en cell är ungefär proportionellt mot cellytan, och cellens kolbiomassa varierar som en funktion av cellvolymen. Växtplanktongeometri som maximerar ytarea till volym bör ha större isotopfraktionering från fotosyntes.
De biokemiska egenskaperna hos växtplankton liknar C3-växter, medan gasutbytesegenskaperna mer liknar C4-strategin. Närmare bestämt förbättrar växtplankton effektiviteten hos deras primära kolfixerande enzym, RuBisCO, med kolkoncentreringsmekanismer (CCM), precis som C4-växter ackumulerar CO 2 i buntmantelcellerna. Olika former av CCM i växtplankton inkluderar aktivt upptag av bikarbonat och CO 2 genom cellmembranet, aktiv transport av oorganiskt kol från cellmembranet till kloroplasterna och aktiv, enkelriktad omvandling av CO 2 till bikarbonat. Parametrarna som påverkar 13C δ13C - - fraktioneringen i växtplankton bidrar till värden mellan -18 till -25‰.





![{\displaystyle CO_{2}+H_{2}O+RuBP{\xrightarrow[{RuBisCO}]{}}2(3{\mbox{-}}phosphoglycerate)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/78da9dc5727089ee854e6ff699812f85c28a07e3)