Ultrakänslighet
Inom molekylärbiologi beskriver ultrasensitivitet ett utmatningssvar som är mer känsligt för stimulansförändringar än det hyperboliska Michaelis-Menten - svaret . Ultrakänslighet är en av de biokemiska växlingarna i cellcykeln och har varit inblandad i ett antal viktiga cellulära händelser, inklusive utgående G2-cellcykelstopp i Xenopus laevis oocyter, ett stadium till vilket cellen eller organismen inte skulle vilja återvända.
Ultrasensitivitet är ett cellulärt system som utlöser inträde i ett annat cellulärt tillstånd. Ultrakänslighet ger ett litet svar på den första insignalen, men en ökning av insignalen ger högre och högre utmatningsnivåer. Detta fungerar för att filtrera bort brus, eftersom små stimuli och tröskelkoncentrationer av stimulus (ingångssignal) är nödvändiga för triggern som gör att systemet kan aktiveras snabbt. Ultrakänsliga svar representeras av sigmoidala grafer, som liknar kooperativitet . Kvantifieringen av ultrakänslighet utförs ofta ungefär med Hill-ekvationen :
Där Hills koefficient (n) kan representera ett kvantitativt mått på ultrakänslig respons.
Historisk utveckling
Zero-order ultrasensitivity beskrevs först av Albert Goldbeter och Daniel Koshland, Jr 1981 i en artikel i Proceedings of the National Academy of Sciences . De visade med hjälp av matematisk modellering att modifiering av enzymer som fungerar utanför första ordningens kinetik endast krävde små förändringar i koncentrationen av effektorn för att producera större förändringar i mängden modifierat protein. Denna amplifiering gav ökad känslighet i biologisk kontroll och implicerade betydelsen av detta i många biologiska system.
Många biologiska processer är binära (ON-OFF), såsom cellödebeslut, metabola tillstånd och signalvägar. Ultrasensitivitet är en switch som hjälper beslutsfattande i sådana biologiska processer. Till exempel, i en apoptotisk process, visade en modell att en positiv återkoppling av hämning av kaspas 3 (Casp3) och Casp9 av hämmare av apoptos kan åstadkomma ultrakänslighet (bistabilitet). Denna positiva feedback samarbetar med Casp3-medierad återkopplingsklyvning av Casp9 för att generera irreversibilitet i kaspasaktivering (slå PÅ), vilket leder till cellapoptos. En annan modell visade också liknande men olika positiva återkopplingskontroller i Bcl-2-familjens proteiner i apoptotisk process.
Nyligen har Jeyeraman et al. har föreslagit att fenomenet ultrakänslighet ytterligare kan delas in i tre underregimer, åtskilda av skarpa stimuluströskelvärden: AV, AV-PÅ-AV och PÅ. Baserat på deras modell föreslog de att denna subregim av ultrakänslighet, AV-PÅ-AV, är som en switchliknande anpassning som kan åstadkommas genom att koppla N-fosforylerings-defosforyleringscykler enkelriktat, utan några explicita återkopplingsslingor.
Andra nya arbeten har betonat att inte bara topologin hos nätverk är viktig för att skapa ultrakänslighetssvar, utan att deras sammansättning (enzymer kontra transkriptionsfaktorer) starkt påverkar om de kommer att uppvisa robust ultrakänslighet. Matematisk modellering antyder för ett brett spektrum av nätverkstopologier att en kombination av enzymer och transkriptionsfaktorer tenderar att ge mer robust ultrakänslighet än den som ses i nätverk som helt består av transkriptionsfaktorer eller helt sammansatta av enzymer.
Mekanismer
Ultrakänslighet kan uppnås genom flera mekanismer:
- Flerstegsmekanismer (exempel: kooperativitet) och multisite fosforylering
- Buffertmekanismer (exempel: lockfosforyleringsställen) eller stökiometriska inhibitorer
- Förändringar i lokalisering (såsom translokation över kärnvapenhöljet)
- Mättnadsmekanismer (även känd som nollordningens ultrakänslighet)
- Positiv feedback
- Allovalens
- Icke-nollordnings ultrakänslighet i membranproteiner
- Dissipativ allosteri
Flerstegsmekanismer
Flerstegs ultrakänslighet uppstår när en enda effektor verkar på flera steg i en kaskad. Successiva kaskadsignaler kan resultera i att högre nivåer av brus introduceras i signalen som kan störa den slutliga utsignalen. Detta är särskilt relevant för stora kaskader, såsom det flagellära regulatoriska systemet där huvudregulatorsignalen sänds genom flera mellanliggande regulatorer innan transkription aktiveras. Kaskad ultrakänslighet kan minska brus och kräver därför mindre input för aktivering. Dessutom är multipla fosforyleringshändelser ett exempel på ultrakänslighet. Ny modellering har visat att flera fosforyleringsställen på membranproteiner kan tjäna till att lokalt mätta enzymaktivitet. Proteiner vid membranet är kraftigt nedsatt i rörlighet jämfört med de i cytoplasman, detta betyder att ett membranbundet enzym som verkar på ett membranprotein kommer att ta längre tid att diffundera bort. Med tillägg av multipla fosforyleringsställen på membransubstratet kan enzymet - genom en kombination av ökad lokal koncentration av enzym och ökade substrat - snabbt nå mättnad.
Buffertmekanismer
Buffertmekanismer som molekylär titrering kan generera ultrakänslighet. In vitro kan detta observeras för den enkla mekanismen:
Där den monomera formen av A är aktiv och den kan inaktiveras genom att binda B för att bilda heterodimeren AB. När koncentrationen av ( = [B] + [AB]) är mycket större än , uppvisar detta system en tröskel som bestäms av koncentrationen av . Vid koncentrationer av ( = [A] +[AB]), lägre än , fungerar B som en buffert för att frigöra A och nästan alla A kommer att hittas som AB. Men vid ekvivalenspunkten, när ≈ , kan inte längre buffra ökningen av , så en liten ökning av orsakar en stor ökning av A. Styrkan hos ultrakänsligheten hos [A] för förändringar i bestäms av / . Ultrakänslighet uppstår när detta förhållande är större än ett och ökar när förhållandet ökar. Ovanför ekvivalenspunkten och A åter linjärt relaterade. In vivo komplicerar syntesen av A och B såväl som nedbrytningen av alla tre komponenterna genereringen av ultrakänslighet. Om synteshastigheterna för A och B är lika uppvisar detta system fortfarande ultrakänslighet vid ekvivalenspunkten.
Ett exempel på en buffringsmekanism är proteinsekvestrering, som är en vanlig mekanism som finns i signalerings- och regulatoriska nätverk. 2009 konstruerade Buchler och Cross ett syntetiskt genetiskt nätverk som reglerades av proteinbindning av en transkriptionell aktivator av en dominant-negativ hämmare. De visade att detta system resulterar i ett flexibelt ultrakänsligt svar i genuttryck. Den är flexibel genom att graden av ultrakänslighet kan ändras genom att ändra expressionsnivåer av den dominant-negativa inhibitorn. Figur 1 i deras artikel illustrerar hur en aktiv transkriptionsfaktor kan sekvestreras av en inhibitor i det inaktiva komplexet AB som inte kan binda DNA. Denna typ av mekanism resulterar i ett "allt-eller-inget"-svar, eller ultraokänslighet, när koncentrationen av det regulatoriska proteinet ökar till den grad att hämmaren utarmas. Robust buffring mot ett svar existerar under denna koncentrationströskel, och när den uppnås förstärks varje liten ökning av insignalen till en stor förändring i utsignalen. [ citat behövs ]
Förändringar i lokalisering
Translokation
Signaltransduktion regleras på olika sätt och ett av sätten är translokation. Reglerad translokation genererar ultrakänslig respons på huvudsakligen tre sätt:
- Reglerad translokation ökar den lokala koncentrationen av signalproteinet. När koncentrationen av signalproteinet är tillräckligt hög för att delvis mätta enzymet som inaktiverar det, genereras ett ultrakänsligt svar.
- Translokation av flera komponenter i signalkaskaden, där stimulus (insignal) orsakar translokation av både signalprotein och dess aktivator i samma subcellulära fack och därigenom genererar ultrakänslig respons som ökar hastigheten och noggrannheten hos signalen.
- Translokation till avdelningen som innehåller stökiometriska inhibitorer.
Translokation är ett sätt att reglera signaltransduktion, och det kan generera ultrakänsliga switchliknande svar eller flerstegs-feedback-loopmekanismer. Ett switchliknande svar kommer att inträffa om translokation höjer den lokala koncentrationen av ett signalprotein. Till exempel epidermal tillväxtfaktor (EGF)-receptorer internaliseras genom klatrinoberoende endocytos (CIE) och/eller klatrinberoende endocytos (CDE) på ligandkoncentrationsberoende sätt. Fördelningen av receptorer i de två vägarna visade sig vara EGF-koncentrationsberoende. I närvaro av låga koncentrationer av EGF internaliserades receptorn uteslutande via CDE, medan vid höga koncentrationer var receptorer lika fördelade mellan CDE och CIE.
Mättnadsmekanismer (nollordningens ultrakänslighet)
Nollordningens ultrakänslighet sker under mättande förhållanden. Tänk till exempel på ett enzymsteg med kinas, fosfatas och substrat. Steady state-nivåer av det fosforylerade substratet har ett ultrakänsligt svar när det finns tillräckligt med substrat för att mätta alla tillgängliga kinaser och fosfataser. Under dessa förhållanden kan små förändringar i förhållandet mellan kinas och fosfatasaktivitet dramatiskt förändra antalet fosforylerade substrat (För en graf som illustrerar detta beteende, se ). Denna förbättring av känsligheten hos steady state-fosforylerat substrat till Km, eller förhållandet mellan kinas och fosfatasaktivitet, kallas noll-ordningen för att skilja det från första ordningens beteende som beskrivs av Michaelis-Menten-dynamiken, där steady state-koncentrationen svarar i en mer gradvis sätt än det switchliknande beteende som uppvisas i ultrakänslighet.
Med hjälp av notationen från Goldbeter & Koshland, låt W vara ett visst substratprotein och låt W' vara en kovalent modifierad version av W. Omvandlingen av W till W' katalyseras av något enzym E 1 {\displaystyle {\ce och den omvända omvandlingen av W' till W katalyseras av ett andra enzym enligt följande ekvationer:
Koncentrationerna av alla nödvändiga komponenter (såsom ATP) antas vara konstanta och representerade i de kinetiska konstanterna. Med hjälp av de kemiska ekvationerna ovan är reaktionshastighetsekvationerna för varje komponent:
Den totala koncentrationen av varje komponent ges av:
Nollordningsmekanismen antar att eller . Systemet är med andra ord i ett Michaelis-Menten steady state, vilket med en bra approximation betyder och är konstanta. Från dessa kinetiska uttryck kan man lösa för vid ett stabilt tillstånd som definierar och
där och
När plottas mot molförhållandet och kan det ses att W till W ' omvandlingen sker över en mycket mindre förändring i -förhållandet än vad den skulle göra under första ordningens (icke-mättande) förhållanden, vilket är ett tecken på ultrakänslighet.
Positiv feedback
Positiva återkopplingsslingor kan orsaka ultrakänsliga svar. Ett exempel på detta ses i transkriptionen av vissa eukaryota gener där icke-samverkande transkriptionsfaktorbindning förändrar positiva återkopplingsslingor av histonmodifiering som resulterar i en ultrakänslig aktivering av transkription. Bindningen av en transkriptionsfaktor rekryterar histonacetyltransferaser och metyltransferaser. Acetyleringen och metyleringen av histoner rekryterar fler acetyltransferaser och metyltransferaser som resulterar i en positiv återkopplingsslinga. I slutändan resulterar detta i aktivering av transkription.
Dessutom kan positiv feedback inducera bistabilitet i Cyclin B1 - av de två regulatorerna Wee1 och Cdc25C, vilket leder till cellens beslut att begå mitos. Systemet kan inte vara stabilt på mellanliggande nivåer av Cyclin B1, och övergången mellan de två stabila tillstånden är abrupt när ökande nivåer av Cyclin B1 växlar systemet från låg till hög aktivitet. Uppvisar hysteres , för olika nivåer av Cyclin B1 varierar växlarna från låg till hög och hög till låg. Emellertid är uppkomsten av ett bistabilt system starkt påverkad av känsligheten hos dess återkopplingsslingor. Det har visats i Xenopus -äggextrakt att Cdc25C-hyperfosforylering är en mycket ultrakänslig funktion av Cdk-aktivitet, som visar ett högt värde på Hill-koefficienten (ca 11) och defosforyleringssteget för Ser 287 i Cdc25C (också involverat i Cdc25C-aktivering) är ännu mer ultrakänslig och visar en Hill-koefficient på cirka 32.
Allovalens
En föreslagen mekanism för ultrakänslighet, kallad allovalens, antyder att aktivitet "härrör från en hög lokal koncentration av interaktionsställen som rör sig oberoende av varandra" Allovalens föreslogs först när den troddes inträffa i den väg där Sic1 bryts ned för att Cdk1 -Clb ( cykliner av B-typ ) för att tillåta inträde i mitos. Sic1 måste fosforyleras flera gånger för att kännas igen och nedbrytas av Cdc4 i SCF-komplexet . Eftersom Cdc4 bara har ett igenkänningsställe för dessa fosforylerade rester föreslogs att när mängden fosforylering ökar, ökar det exponentiellt sannolikheten för att Sic1 känns igen och bryts ned av Cdc4. Denna typ av interaktion ansågs vara relativt immun mot förlust av en plats och lätt inställd på varje given tröskel genom att justera egenskaperna för individuella platser. Antaganden för allovalensmekanismen baserades på en generell matematisk modell som beskriver interaktionen mellan en polyvalent störd ligand och ett enda receptorställe. Det visade sig senare att ultrakänsligheten i Cdk1-nivåer genom nedbrytning av Sic1 faktiskt beror på en positiv återkopplingsslinga.
Icke-nollordnings ultrakänslighet i membranproteiner
Modellering av Dushek et al. föreslår en möjlig mekanism för ultrakänslighet utanför nollordningen. När det gäller membranbundna enzymer som verkar på membranbundna substrat med flera enzymatiska ställen (såsom tyrosin-fosforylerade receptorer som T-cellsreceptorn), kunde ultrakänsliga svar ses, avgörande beroende på tre faktorer: 1) begränsad diffusion i membranet, 2) flera bindningsställen på substratet och 3) kort enzymatisk inaktivering efter katalys.
Under dessa speciella förhållanden, även om enzymet kan vara i överskott av substratet (första ordningens regim), är enzymet effektivt lokalt mättat med substrat på grund av de multipla bindningsställena, vilket leder till switchliknande svar. Denna mekanism för ultrakänslighet är oberoende av enzymkoncentration, men signalen förstärks avsevärt beroende på antalet bindningsställen på substratet. Båda villkorade faktorerna (begränsad diffusion och inaktivering) är fysiologiskt rimliga, men har ännu inte bekräftats experimentellt. Dusheks modellering fann ökande Hill-kooperativitet med fler substratställen (fosforyleringsställen) och med större steriskt/diffusionshinder mellan enzym och substrat. Denna mekanism för ultrakänslighet baserad på lokal enzymmättnad härrör delvis från passiva egenskaper hos långsam membrandiffusion och kan därför vara allmänt tillämplig.
Dissipativ allosteri
Den bakteriella flagellmotorn har föreslagits att följa en dissipativ allosterisk modell, där ultrakänslighet kommer som en kombination av proteinbindningsaffinitet och energibidrag från protonens drivkraft (se Flagellarmotorer och kemotaxi nedan).
Inverkan av uppströms och nedströms komponenter på modulens ultrakänslighet
I en levande cell är ultrakänsliga moduler inbäddade i ett större nätverk med uppströms och nedströms komponenter. Dessa komponenter kan begränsa intervallet av ingångar som modulen kommer att ta emot såväl som intervallet av modulens utgångar som nätverket kommer att kunna upptäcka. Altszyler et al. (2014) studerade hur den effektiva ultrakänsligheten hos ett modulärt system påverkas av dessa restriktioner. De fann för vissa ultrakänsliga motiv att begränsningar av dynamiskt omfång som åläggs av nedströmskomponenter kan ge effektiva känsligheter som är mycket större än den för originalmodulen när de betraktas isolerat.
Hill Koefficient
Ultrakänsligt beteende representeras vanligtvis av en sigmoidal kurva, eftersom små förändringar i stimulus kan utlösa stora förändringar i svaret . En sådan relation är Hill-ekvationen :
där är Hill-koefficienten som kvantifierar brantheten hos den sigmoidala stimulus-responskurvan och det är därför en känslighetsparameter. Det används ofta för att bedöma samverkan i ett system. En Hill-koefficient som är större än en indikerar positiv kooperativitet och systemet uppvisar således ultrakänslighet. System med en Hill-koefficient på 1 är icke-samarbetsvilliga och följer den klassiska Michaelis-Menten-kinetiken. Enzymer som uppvisar icke-samverkande aktivitet representeras av hyperboliska stimulus/svarskurvor, jämfört med sigmoida kurvor för kooperativa (ultrakänsliga) enzymer. Vid mitogenaktiverat proteinkinas (MAPK)-signalering (se exempel nedan) stöds signaleringens ultrakänslighet av den sigmoida stimulus/svarskurvan som är jämförbar med ett enzym med en Hill-koefficient på 4,0-5,0. Detta är ännu mer ultrakänsligt för den kooperativa bindningsaktiviteten av hemoglobin, som har en Hill-koefficient på 2,8.
Beräkning
Ur driftssynpunkt kan Hill-koefficienten beräknas som:
- .
där och är de ingångsvärden som behövs för att producera 10% respektive 90% av det maximala svaret.
Svarskoefficient
Globalt känslighetsmått som Hill-koefficient karakteriserar inte de s-formade kurvornas lokala beteenden. Istället fångas dessa egenskaper väl av svarskoefficientmåttet definierat som:
Länk mellan Hill Coefficient och Response Coefficient
Altszyler et al. (2017) har visat att dessa ultrakänslighetsmått kan kopplas samman med följande ekvation:
där betecknade medelvärdet för variabeln x över området [a,b].
Ultrakänslighet i funktionssammansättning
Betrakta två kopplade ultrakänsliga moduler, bortse från effekterna av sekvestrering av molekylära komponenter mellan skikt. I det här fallet är uttrycket för systemets dos-responskurva, , ett resultat av den matematiska sammansättningen av funktionerna, , som beskriver input/output-förhållandet för isolerade moduler :
Brown et al. (1997) har visat att den lokala ultrakänsligheten hos de olika lagren kombineras multiplikativt:
- .
I samband med detta resultat har Ferrell et al. (1997) visade, för moduler av Hill-typ, att den totala kaskadens globala ultrakänslighet måste vara mindre än eller lika med produkten av de globala ultrakänslighetsuppskattningarna av varje kaskads lager,
- ,
där och är Hill-koefficienten för modul 1 respektive 2.
Altszyler et al. (2017) har visat att kaskadens globala ultrakänslighet kan beräknas analytiskt:
där och avgränsade Hill-ingångens arbetsområde för det sammansatta systemet, dvs ingångsvärdena för i-lagret så att det sista lagret ( motsvarande i detta fall) nådde 10% och 90% av sin maximala uteffektnivå. Det följde denna ekvation att systemets Hill-koefficient kunde skrivas som produkten av två faktorer, och , som karakteriserade lokala genomsnittliga känsligheter över den relevanta ingångsregionen för varje lager: med i detta fall.
För det mer allmänna fallet med en kaskad av -moduler, kan Hill-koefficienten uttryckas som:
- ,
Supramultiplikativitet
Flera författare har rapporterat förekomsten av supramultiplikativt beteende i signaleringskaskader (dvs. ultrakänsligheten för kombinationen av skikt är högre än produkten av individuella ultrakänsligheter), men i många fall förblev det ultimata ursprunget för supramultiplikativitet svårfångat. Altszyler et al. (2017) ramverk föreslog naturligtvis ett generellt scenario där supramultiplikativt beteende kunde äga rum. Detta kan inträffa när, för en given modul, motsvarande Hills ingångsarbetsområde var beläget i en ingångsregion med lokala ultrakänsligheter högre än den globala ultrakänsligheten för respektive dos-responskurva.
Roll i cellulära processer
MAP Kinase Signaling Cascade
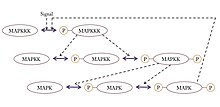
Ett allestädes närvarande signaleringsmotiv som uppvisar ultrakänslighet är MAPK ( mitogen-aktiverat proteinkinas )-kaskaden, som kan ta en graderad insignal och producera en switchliknande utdata, såsom gentranskription eller cellcykelprogression . I detta vanliga motiv aktiveras MAPK av ett tidigare kinas i kaskaden, kallat MAPK-kinas eller MAPKK. På liknande sätt aktiveras MAPKK av MAPKK-kinas, eller MAPKKK. Dessa kinaser fosforyleras sekventiellt när MAPKKK aktiveras, vanligtvis via en signal som tas emot av ett membranbundet receptorprotein. MAPKKK aktiverar MAPKK och MAPKK aktiverar MAPK. Ultrakänslighet uppstår i detta system på grund av flera funktioner:
- MAPK och MAPKK kräver båda två separata fosforyleringshändelser för att aktiveras.
- Omkastningen av MAPK- fosforylering av specifika fosfataser kräver en ökande koncentration av aktiveringssignaler från varje tidigare kinas för att uppnå en utmatning av samma storlek.
- MAPKK har en koncentration över K Μ för dess specifika fosfatas och MAPK har en koncentration över K Μ för MAPKK.
Förutom MAPK-kaskaden har ultrasensitivitet även rapporterats vid muskelglykolys, vid fosforylering av isocitratdehydrogenas och vid aktivering av det kalmodulinberoende proteinkinas II (CAMKII).
En ultrakänslig switch har konstruerats genom att kombinera ett enkelt linjärt signalprotein (N-WASP) med en till fem SH3 -interaktionsmoduler som har autoinhiberande och kooperativa egenskaper. Tillägg av en enda SH3-modul skapade en switch som aktiverades på ett linjärt sätt av exogen SH3-bindande peptid. Ett ökande antal domäner ökade ultrakänsligheten. En konstruktion med tre SH3-moduler aktiverades med en skenbar Hill-koefficient på 2,7 och en konstruktion med fem SH3-moduler aktiverades med en skenbar Hill-koefficient på 3,9.
Translokation
Under G2-fasen av cellcykeln gör Cdk1 och cyklin B1 ett komplex och bildar mognadsfrämjande faktor (MPF). Komplexet ackumuleras i kärnan på grund av fosforylering av cyklin B1 på flera ställen, vilket hämmar kärnexport av komplexet. Fosforylering av Thr19- och Tyr15-rester av Cdk1 av Wee1 och MYT1 håller komplexet inaktivt och hämmar inträde i mitos, medan defosforylering av Cdk1 av CDC25C -fosfatas vid Thr19- och Tyr15-rester aktiverar komplexet som är nödvändigt för att komma in i mitos. Cdc25C-fosfatas finns i cytoplasman och i sen G2-fas translokeras det in i kärnan genom signalering såsom PIK1, PIK3. Den reglerade translokationen och ackumuleringen av de multipla erforderliga signalkaskadkomponenterna, MPF och dess aktivator Cdc25, i kärnan genererar effektiv aktivering av MPF och producerar switchliknande, ultrakänsligt inträde i mitos.
Figuren visar olika möjliga mekanismer för hur ökad reglering av lokaliseringen av signaleringskomponenter genom stimulus (insignal) förskjuter utsignalen från michaelsk respons till ultrakänslig respons. När stimulans endast reglerar hämning av Cdk1-cyklinB1 kärnexport, är resultatet Michaelian-svar, Fig (a). Men om stimulansen kan reglera lokalisering av flera komponenter i signalkaskaden, dvs hämning av Cdk1-cyklinB1 kärnexport och translokation av Cdc25C till kärna, då är resultatet ultrakänsligt svar, Fig (b). När fler komponenter i signalkaskaden regleras och lokaliseras av stimulansen - dvs hämning av Cdk1-cyklinB1 kärnexport, translokation av Cdc25C till kärnan och aktivering av Cdc25C - blir utsignalen mer och mer ultrakänslig, Fig (c) .
Buffring (decoy)
Under mitos är mitotisk spindelorientering avgörande för att bestämma platsen för klyvningsfårning och position för dotterceller för efterföljande cellödebestämning . Denna orientering uppnås genom polariserande kortikala faktorer och snabb inriktning av spindeln med polaritetsaxeln. Hos fruktflugor har tre kortikala faktorer visat sig reglera spindelns position: heterotrimer G-protein α subenhet (Gαi), Partner of Inscuteable (Pins) och Mushroom body defect (Mud). Gαi lokaliserar sig vid apikala cortex för att rekrytera Pins. Vid bindning till GDP-bunden Gai aktiveras Pins och rekryterar Mud för att uppnå polariserad fördelning av kortikala faktorer. N-terminala tetratricopeptide repeats (TPR) i Pins är den bindande regionen för Mud, men autoinhiberas av inneboende C-terminala GoLoco-domäner (GLs) i frånvaro av Gai. Aktivering av Pins genom Gai-bindning till GLs är mycket ultrakänslig och uppnås genom följande lockbetemekanism: GLs 1 och 2 fungerar som lockdomäner, som konkurrerar med den regulatoriska domänen, GL3, om Gai-ingångar. Denna intramolekylära lockbetemekanism tillåter Pins att fastställa sin tröskel och branthet som svar på distinkt Gai-koncentration. Vid låga Gai-ingångar är lockbets-GL:erna 1 och 2 företrädesvis bundna. Vid mellanliggande Gai-koncentration är lockbetena nästan mättade och GL3 börjar befolkas. Vid högre Gai-koncentration är lockbetena helt mättade och Gai binder till GL3, vilket leder till Pins-aktivering. Ultrakänslighet hos Pins som svar på Gαi säkerställer att Pins endast aktiveras vid den apikala cortex där Gai-koncentrationen är över tröskeln, vilket möjliggör maximal lerrekrytering. [ citat behövs ]
Växlingsbeteende för GTPaser
GTPaser är enzymer som kan binda och hydrolysera guanosintrifosfat (GTP). Små GTPaser, som Ran och Ras, kan existera i antingen en GTP-bunden form (aktiv) eller en GDP-bunden form (inaktiv), och omvandlingen mellan dessa två former ger dem ett switchliknande beteende. Som sådan är små GTPaser involverade i flera cellulära händelser, inklusive nukleär translokation och signalering. Övergången mellan de aktiva och inaktiva tillstånden underlättas av guanin-nukleotidutbytesfaktorer (GEF) och GTPas-aktiverande proteiner (GAP).
Beräkningsstudier av växlingsbeteendet hos GTPaser har avslöjat att GTPase-GAP-GEF-systemet uppvisar ultrakänslighet. I sin studie har Lipshtat et al. simulerade effekterna av nivåerna av GEF- och GAP-aktivering på Rap-aktiveringssignaleringsnätverket som svar på signaler från aktiverade α2-adrenerga (α2R)-receptorer, vilket leder till nedbrytning av den aktiverade Rap GAP. De fann att växlingsbeteendet för Rap-aktivering var ultrakänsligt för förändringar i koncentrationen (dvs amplituden) och varaktigheten av α2R-signalen, vilket gav Hill-koefficienter på nH=2,9 respektive nH=1,7 (en Hill-koefficient större än nH=1) är karakteristiskt för ultrakänslighet). Författarna bekräftade detta experimentellt genom att behandla neuroblaster med HU-210, som aktiverar RAP genom nedbrytning av Rap GAP. Ultrakänslighet observerades både på ett dosberoende sätt (nH=5±0,2), genom att behandla celler med olika HU-210-koncentrationer under en bestämd tid och på ett varaktighetsberoende sätt (nH=8,6±0,8), genom att behandla celler med en fast HU-210-koncentration under varierande tider. [ citat behövs ]
Genom att ytterligare studera systemet fastställde författarna att (graden av lyhördhet och ultrakänslighet) var starkt beroende av två parametrar: det initiala förhållandet av kGAP/kGEF, där k:erna inkluderar både koncentrationen av aktiv GAP eller GEF och deras motsvarande kinetiska hastigheter; och signalpåverkan, som är produkten av nedbrytningshastigheten för aktiverad GAP och antingen signalamplituden eller signalvaraktigheten. Parametern kGAP/kGEF påverkar brantheten i övergången från GTPase-switchens två tillstånd, med högre värden (~10) som leder till ultrakänslighet. Signalpåverkan påverkar kopplingspunkten. Därför, genom att beroende på förhållandet mellan koncentrationer snarare än på individuella koncentrationer, kan systemets switchliknande beteende också visas utanför nollordningens regim. [ citat behövs ]
Ultrakänslighet och neuronal potential
Ihållande stimulering vid den neuronala synapsen kan leda till markant olika utfall för den postsynaptiska neuronen. Förlängd svag signalering kan resultera i långtidsdepression (LTD), där aktivering av den postsynaptiska neuronen kräver en starkare signal än innan LTD initierades. Däremot långsiktig potentiering (LTP) när den postsynaptiska neuronen utsätts för en stark stimulans, och detta resulterar i förstärkning av den neurala synapsen (dvs mindre signal från signalsubstansen krävs för aktivering).
I CA1-regionen av hippocampus medieras beslutet mellan LTD och LTP enbart av nivån av intracellulär vid den postsynaptiska dendritiska ryggraden . Låga nivåer av (som resulterar från stimulering på låg nivå) aktiverar proteinet fosfatas calcineurin , vilket inducerar LTD. Högre nivåer av resulterar i aktivering av /kalmodulinberoende proteinkinas II (CaMKII), vilket leder till LTP. Skillnaden i Ca 2+ koncentration som krävs för att en cell ska genomgå LTP är endast marginellt högre än för LTD, och eftersom neuroner visar bistabilitet (antingen LTP eller LTD) efter ihållande stimulering, tyder detta på att en eller flera komponenter i systemet svarar i en switchliknande eller ultrakänsligt sätt. Bradshaw et al. visade att CaMKII (LTP-induceraren) svarar på intracellulära kalciumnivåer på ett ultrakänsligt sätt, med <10% aktivitet vid 1,0 uM och ~90% aktivitet vid 1,5 uM, vilket resulterar i en Hill-koefficient på ~8. Ytterligare experiment visade att denna ultrakänslighet medierades av samverkande bindning av CaMKII av två molekyler av kalmodulin (CaM), och autofosforylering av aktiverad CaMKII vilket ledde till en positiv återkopplingsslinga.
På detta sätt kan intracellulärt kalcium inducera en graderad, icke-ultrakänslig aktivering av kalcineurin vid låga nivåer, vilket leder till LTD, medan den ultrakänsliga aktiveringen av CaMKII resulterar i en tröskel för intracellulär kalciumnivå som genererar en positiv återkopplingsslinga som förstärker signalen och leder till det motsatta cellulära resultatet: LTP. Således underlättar bindning av ett enda substrat till flera enzymer med olika känslighet ett bistabilt beslut för cellen att genomgå LTD eller LTP. [ citat behövs ]
Ultrakänslighet i utveckling
Det har föreslagits att noll-ordningens ultrakänslighet kan generera trösklar under utveckling som möjliggör omvandling av en graderad morfogeninmatning till ett binärt switchliknande svar. Melen et al. (2005) har hittat bevis för ett sådant system i mönstringen av Drosophila embryonala ventral ektoderm . I detta system omvandlas den graderade mitogenaktiverade proteinkinasaktiviteten (MAPK) till en binär utmatning, allt-eller-ingen-nedbrytningen av Yan-transkriptionsrepressorn. De fann att MAPK-fosforylering av Yan är både väsentlig och tillräcklig för Yans nedbrytning. I enlighet med noll-ordningens ultrakänslighet förlängde en ökning av Yan-protein den tid som krävdes för nedbrytning men hade ingen effekt på gränsen för Yan-nedbrytning i utvecklande embryon. Deras resultat överensstämmer med en situation där en stor pool av Yan antingen blir helt försämrad eller underhålls. Det speciella svaret för varje cell beror på om hastigheten för reversibel Yan-fosforylering av MAPK är större eller mindre än defosforylering. Således kan en liten ökning av MAPK-fosforylering göra att det är den dominerande processen i cellen och leda till fullständig nedbrytning av Yan.
Flerstegs-feedback-slingmekanism leder också till ultrakänslighet
Flerstegs återkopplingsmekanism leder också till ultrakänslighet. Det finns papper som introducerar att konstruktion av syntetiska återkopplingsslingor med användning av jästparning med mitogenaktiverat protein (MAP) kinasväg som ett modellsystem.
I jästparningsväg: alfa-faktor aktiverar receptorn, Ste2 och Ste4 och aktiverad Ste4 rekryterar Ste5-komplexet till membranet, vilket tillåter PAK-liknande kinas Ste20 (membranlokaliserat) att aktivera MAPKKK Ste11. Ste11 och nedströms kinaser, Ste7 (MAPKK) och Fus3 (MAPK), kolokaliseras på ställningen och aktivering av kaskad leder till transkriptionsprogram. De använde vägmodulatorer utanför kärnkaskaden, Ste50 främjar aktivering av Ste11 av Ste20; Msg5 (negativ, röd) är MAPK-fosfatas som deaktiverar Fus3 (Fig.2A).
Vad de byggde var en krets med förbättrat ultrakänsligt switchbeteende genom att konstitutivt uttrycka en negativ modulator, Msg5 som är en av MAPK-fosfatas och inducerbart uttrycka en positiv modulator, Ste50 som är vägmodulatorer utanför kärnkaskad (Fig.2B). Framgången med denna rekryteringsbaserade ingenjörsstrategi tyder på att det kan vara möjligt att omprogrammera cellulära svar med hög precision.
Flagellarmotorer och kemotaxi
Rotationsriktningen för E. coli styrs av flagellmotoromkopplaren . En ring av 34 FliM-proteiner runt rotorn binder CheY, vars fosforyleringstillstånd avgör om motorn roterar medurs eller moturs. Den snabba omkopplingsmekanismen tillskrivs ett ultrakänsligt svar, som har en Hill-koefficient på ~10. Detta system har föreslagits att följa en dissipativ allosterisk modell, där rotationsväxling är ett resultat av både CheY-bindning och energiförbrukning från protonmotorkraften, som också driver flagellarrotationen.
Utveckling av en syntetisk ultrakänslig signalväg
Nyligen har det visat sig att en Michaelian signalväg kan omvandlas till en ultrakänslig signalväg genom införandet av två positiva återkopplingsslingor. I detta syntetbiologiska tillvägagångssätt började Palani och Sarkar med en linjär, graderad svarsväg, en väg som visade en proportionell ökning av utsignalen i förhållande till mängden signalinmatning, över ett visst intervall av ingångar. Denna enkla väg bestod av en membranreceptor, ett kinas och en transkriptionsfaktor. Vid aktivering fosforylerar membranreceptorn kinaset, som flyttar in i kärnan och fosforylerar transkriptionsfaktorn, vilket sätter på genuttryck. För att omvandla detta graderade svarssystem till en ultrakänslig eller switchliknande signalväg skapade utredarna två positiva återkopplingsslingor. I det konstruerade systemet resulterade aktivering av membranreceptorn i ökat uttryck av både själva receptorn och transkriptionsfaktorn. Detta åstadkoms genom att placera en promotor som är specifik för denna transkriptionsfaktor uppströms om båda generna. Författarna kunde visa att den syntetiska vägen visade hög ultrakänslighet och bistabilitet.
Nyligen genomförd beräkningsanalys av effekterna av ett signalproteins koncentration på närvaron av ett ultrakänsligt svar har kommit till kompletterande slutsatser om inverkan av ett signalproteins koncentration på omvandlingen av ett graderat svar till ett ultrakänsligt. Istället för att fokusera på generering av signalproteiner genom positiv feedback, fokuserade studien istället på hur dynamiken i ett signalproteins utträde ur systemet påverkar svaret. Soyer, Kuwahara och Csika´sz-Nagy utformade en signalväg som består av ett protein (P) som har två möjliga tillstånd (omodifierat P eller modifierat P*) och som kan modifieras av en inkommande stimulus E. Dessutom, medan den omodifierade formen , P, tillåts komma in i eller lämna systemet, P* får endast lämna (dvs. den genereras inte någon annanstans). Efter att ha varierat parametrarna för detta system upptäckte forskarna att modifieringen av P till P* kan växla mellan ett graderat svar och ett ultrakänsligt svar via modifieringen av utgångshastigheterna för P och P* i förhållande till varandra. Övergången från ett ultrakänsligt svar till E och ett graderat svar på E genererades när de två hastigheterna gick från mycket lika till mycket olika, oberoende av kinetiken för omvandlingen från P till P* i sig. Detta fynd antyder åtminstone två saker: 1) det förenklade antagandet att nivåerna av signalmolekyler förblir konstanta i ett system kan allvarligt begränsa förståelsen av ultrakänslighetens komplexitet; och 2) det kan vara möjligt att inducera eller hämma ultrakänslighet artificiellt genom att reglera hastigheterna för in- och utträde av signalmolekyler som upptar ett system av intresse.
Begränsningar i modularitet
Det har visat sig att integrationen av en given syntetisk ultrakänslig modul med uppströms- och nedströmskomponenter ofta förändrar dess informationsbearbetningsförmåga. Dessa effekter måste beaktas i designprocessen.








![{\displaystyle {\begin{array}{rcrcr}\\W+E_{1}&{\ce {<=>[a_1][d_1]}}&WE_{1}&{\ce {->[k_1]}}&W'+E_{1}\\{}\\W'+E_{2}&{\ce {<=>[a_2][d_2]}}&W'E_{2}&{\ce {->[k_2]}}&W+E_{2}\\{}\end{array}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b99db825c4ff803840dbb716ddf91cf25350aee2)
![{\displaystyle {\frac {d[W]}{dt}}=-a_{1}[W][E_{1}]+d_{1}[WE_{1}]+k_{2}[W'E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8d94c07c264d2a743d2af4229c9cb395795430cf)
![{\displaystyle {\frac {d[WE_{1}]}{dt}}=a_{1}[W][E_{1}]-(d_{1}+k_{1})[WE_{1}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/240963c6e424e624af0df0c5fd9c408b2bf0dabc)
![{\displaystyle {\frac {d[W']}{dt}}=-a_{2}[W'][E_{2}]+d_{2}[W'E_{2}]+k1[WE_{1}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/26666a5dd399063d4c38813fb9853fd95de8e985)
![{\displaystyle {\frac {d[W'E_{2}]}{dt}}=a_{2}[W'][E_{2}]-(d_{2}+k_{2})[W'E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5f2755c33130ae77257089cc6cd8edbda76ee4be)
![{\displaystyle [W_{T}]=[W]+[W']+[WE_{1}]+[W'E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/74f4c088eb41138b9bed456fffb71fb5a51bf293)
![{\displaystyle [E_{1T}]=[E_{1}]+[WE_{1}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/00df8b30b56b0b703a1f4bb53c2d70cdb4e63ac1)
![{\displaystyle [E_{2T}]=[E_{2}]+[W'E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aa4d15730374a3959d60d78b8506d2ef6be59377)
![{\displaystyle [W_{T}]\gg [E_{1}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f2b067fc15f94fb3ac4fcab8cf8c72a85f2a7126)
![{\displaystyle [E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c800f8bc3fbf23eb2b33e87f84459309ac58a636)
![{\displaystyle [WE_{1}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b17c8921bcdc4458ca5b2d4f792d05479279d34d)
![{\displaystyle [W'E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4756360ea10e8a76069a18341737bfa9397a91ee)

![{\displaystyle W=[W]/[W_{T}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b6f8bd24362ea433b22305591115664c6e6c7b4c)


![{\displaystyle k_{1}[WE_{1}]=k_{2}[W'E_{2}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4e4e37afe68c067a0ee4e3fd0b8a055212e94edd)
![{\displaystyle V_{1}=k_{1}[E_{1T}],}](https://wikimedia.org/api/rest_v1/media/math/render/svg/763a5a97e5c465ea9bf779d5b3e41035a40e1528)
![{\displaystyle V_{2}=k_{2}[E_{2T}],}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3a2d41808c31348290dd5cfba0c3d1516326f1aa)
![{\displaystyle K_{1}={\frac {d_{1}+k_{1}}{a_{1}[W_{T}]}}={\frac {K_{M1}}{[W_{T}]}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bc8f2d2a0612bbf57fd2e27774ec3fde531dc387)
![{\displaystyle K_{2}={\frac {d_{2}+k_{2}}{a_{2}[W_{T}]}}={\frac {K_{M2}}{[W_{T}]}}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/82a9c2ed5487c0e38272fb390ac0ada579811ee1)


![[L]](https://wikimedia.org/api/rest_v1/media/math/render/svg/c1eba88cad4b17de726ed2c779b29eecdf5819a2)

![{\displaystyle \theta ={\frac {[L]^{n}}{K_{d}+[L]^{n}}}={\frac {[L]^{n}}{(K_{A})^{n}+[L]^{n}}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ff9d9d9370beac68a7957b42a48f719478d612ed)





















![{\displaystyle [X10_{i},X90_{i}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2a6a9f701cc2d5bd5754f6206af5ce8e2b644e8f)