Posttraumatiskt anfall
Posttraumatiska anfall ( PTS ) är anfall som är resultatet av traumatisk hjärnskada (TBI), hjärnskada orsakad av fysiskt trauma . PTS kan vara en riskfaktor för posttraumatisk epilepsi (PTE), men en person som har ett anfall eller anfall på grund av traumatisk hjärnskada behöver inte nödvändigtvis ha PTE, som är en form av epilepsi , ett kroniskt tillstånd där anfall uppstår upprepade gånger. Men "PTS" och "PTE" kan användas omväxlande i medicinsk litteratur.
Kramper är vanligtvis en indikation på en svårare TBI. Anfall som inträffar kort efter att en person fått en hjärnskada kan ytterligare skada den redan sårbara hjärnan. De kan minska mängden syre tillgängligt för hjärnan, orsaka att excitatoriska signalsubstanser frigörs i överskott, öka hjärnans metaboliska behov och höja trycket i det intrakraniella utrymmet , vilket ytterligare bidrar till skada. Således får personer som drabbas av allvarliga huvudtrauma antikonvulsiva mediciner som en försiktighetsåtgärd mot anfall.
Cirka 5–7 % av personer som är inlagda på sjukhus med TBI har minst ett anfall. PTS är mer benägna att uppstå vid svårare skador och vissa typer av skador ökar risken ytterligare. Risken för att en person ska utveckla PTS blir successivt lägre med tiden efter skadan. TBI-överlevande kan dock fortfarande vara i riskzonen över 15 år efter skadan. Barn och äldre vuxna löper en högre risk för PTS.
Klassificering
I mitten av 1970-talet klassificerades PTS först av Bryan Jennett i tidiga och sena anfall , de som inträffade under den första veckan av skadan respektive de som inträffade efter en vecka. Även om gränsen på sju dagar för tidiga anfall används i stor utsträckning, är den godtycklig; anfall som inträffar efter den första veckan men inom den första månaden av skadan kan dela egenskaper med tidiga anfall. Vissa studier använder en 30-dagars cut-off för tidiga anfall istället. Senare blev det accepterat att ytterligare dela upp anfallen i omedelbar PTS , anfall som inträffade inom 24 timmar efter skadan; tidig PTS, med anfall mellan en dag och en vecka efter trauma; och sen PTS, anfall mer än en vecka efter trauma. Vissa anser att sen PTS är synonymt med posttraumatisk epilepsi .
Tidig PTS uppträder åtminstone en gång hos cirka 4 eller 5 % av personer som är inlagda på sjukhus med TBI, och sen PTS inträffar någon gång hos 5 % av dem. Av de anfall som inträffar inom den första veckan av traumat inträffar ungefär hälften inom det första dygnet. Hos barn är det mer sannolikt att tidiga anfall inträffar inom en timme och en dag efter skada än hos vuxna. Av de anfall som inträffar inom de första fyra veckorna av huvudtrauma inträffar cirka 10 % efter den första veckan. Sena anfall inträffar i högsta grad under de första veckorna efter skadan. Cirka 40 % av sena anfall börjar inom sex månader efter skadan och 50 % börjar inom ett år.
Särskilt hos barn och personer med svår TBI är det livshotande tillståndet med ihållande anfall som kallas status epilepticus en risk vid tidiga anfall; 10 till 20 % av PTS utvecklas till tillståndet. I en studie utvecklade 22 % av barn under 5 år statusanfall, medan 11 % av hela TBI-populationen som studerades gjorde det. Statusanfall tidigt efter en TBI kan öka chanserna att en person kommer att utveckla oprovocerade anfall senare.
Patofysiologi
Det är inte helt förstått vilka fysiologiska mekanismer som orsakar anfall efter skada, men tidiga anfall tros ha andra bakomliggande processer än sena. Omedelbara och tidiga anfall tros vara en direkt reaktion på skadan, medan sena anfall tros bero på skador på hjärnbarken genom mekanismer som excitotoxicitet och järn från blod. Omedelbara anfall som inträffar inom två sekunder efter skadan uppstår troligen eftersom kraften från skadan stimulerar hjärnvävnad som har en låg tröskel för anfall när den stimuleras. Tidiga PTS anses vara provocerade anfall, eftersom de härrör från de direkta effekterna av huvudtraumat och därmed inte anses vara egentlig epilepsi, medan sena anfall anses tyda på bestående förändringar i hjärnans struktur och antyda epilepsi. Tidiga anfall kan orsakas av faktorer som cerebralt ödem , intrakraniell blödning , cerebral kontusion eller rivsår . Faktorer som kan resultera i anfall som inträffar inom två veckor efter en förolämpning inkluderar närvaron av blod i hjärnan; förändringar i blod-hjärnbarriären ; överdriven frisättning av excitatoriska neurotransmittorer såsom glutamat ; skador på vävnader orsakade av fria radikaler ; och förändringar i hur celler producerar energi. Sena anfall tros vara resultatet av epileptogenes , där neurala nätverk omstruktureras på ett sätt som ökar sannolikheten för att de kommer att bli upphetsade, vilket leder till anfall.
Diagnos
Medicinsk personal syftar till att avgöra om ett anfall orsakas av en förändring i patientens biokemi, såsom hyponatremi . Neurologiska undersökningar och tester för att mäta nivåer av serumelektrolyter utförs .
Inte alla anfall som uppstår efter trauma är PTS; de kan bero på en anfallsstörning som redan fanns, som till och med kan ha orsakat traumat. Dessutom ska posttraumatiska anfall inte förväxlas med hjärnskakning, som kan omedelbart följa efter en hjärnskakning men som faktiskt inte är anfall och inte är en prediktiv faktor för epilepsi.
Neuroimaging används för att styra behandlingen. Ofta utförs MRT hos alla patienter med PTS, men den mindre känsliga men mer lättillgängliga CT-skanningen kan också användas.
Förebyggande
Strax efter TBI får människor antikonvulsiva mediciner, eftersom anfall som inträffar tidigt efter trauma kan öka hjärnskadorna genom hypoxi , överdriven frisättning av excitatoriska neurotransmittorer , ökade metaboliska krav och ökat tryck i det intrakraniella utrymmet. Läkemedel som används för att förhindra anfall inkluderar valproat , fenytoin och fenobarbital . Det rekommenderas att behandling med anfallsmedicin påbörjas så snart som möjligt efter TBI. Förebyggande av tidiga anfall skiljer sig från det för sena anfall, eftersom syftet med de förra är att förhindra skador orsakade av anfallen, medan syftet med det senare är att förhindra epileptogenes. Starka bevis från kliniska prövningar tyder på att antiepileptika som ges inom en dag efter skada förhindrar anfall inom den första veckan efter skadan, men inte efter. Till exempel fann en genomgång av medicinsk litteratur 2003 att fenytoin var förebyggande mot tidig, men förmodligen inte sen PTS. Hos barn kan antikonvulsiva medel vara ineffektiva för både tidiga och sena anfall. Av okända anledningar är profylaktisk användning av antiepileptika under en lång period förknippad med en ökad risk för anfall. Av dessa skäl rekommenderas antiepileptika allmänt under en kort tid efter huvudtrauma för att förhindra omedelbara och tidiga, men inte sena, anfall. Ingen behandling är allmänt accepterad för att förhindra utvecklingen av epilepsi. Däremot kan mediciner ges för att undertrycka fler anfall om sena anfall inträffar.
Behandling
Anfall som är ett resultat av TBI är ofta svåra att behandla. Antiepileptika som kan ges intravenöst kort efter skada inkluderar fenytoin, natriumvalproat , karbamazepin och fenobarbital. Antiepileptika förhindrar inte alla anfall hos alla, men fenytoin och natriumvalproat stoppar vanligtvis anfall som pågår.
Prognos
PTS är förknippat med en generellt god prognos. Det är okänt exakt hur lång tid efter en TBI en person löper högre risk för anfall än resten av befolkningen, men uppskattningar har föreslagit längder på 10 till över 15 år. För de flesta med TBI inträffar inte anfall efter tre månader och endast 20–25 % av personer med TBI har PTS mer än två år efter skadan. Måttlig och svår TBI innebär dock fortfarande en hög risk för PTS i upp till fem år efter skadan.
Studier har rapporterat att 25–40 % av PTS-patienterna går i remission ; senare studier utförda efter utvecklingen av mer effektiva anfallsmediciner rapporterade högre totala remissionsfrekvenser. Hos en fjärdedel av personer med anfall från ett huvudtrauma kontrollerar medicinering dem väl. En undergrupp av patienter har dock anfall trots aggressiv antiepileptikabehandling. Sannolikheten att PTS går i remission är lägre för personer som får frekventa anfall det första året efter skadan.
Risk för att utveckla PTE
Det är inte känt om PTS ökar sannolikheten för att utveckla PTE. Tidig PTS, även om den inte nödvändigtvis är epileptisk till sin natur, är associerad med en högre risk för PTE. PTS indikerar dock inte att utveckling av epilepsi säkert kommer att inträffa, och det är svårt att isolera PTS från skadans svårighetsgrad som en faktor i PTE-utvecklingen. Cirka 3 % av patienterna utan tidiga anfall utvecklar sen PTE; denna siffra är 25 % hos dem som har tidig PTS, och skillnaden är större om andra riskfaktorer för att utveckla PTE exkluderas. Anfall som inträffar omedelbart efter en kränkning anses vanligen inte ge en ökad risk för återkommande anfall, men bevis från minst en studie har föreslagit att både omedelbara och tidiga anfall kan vara riskfaktorer för sena anfall. Tidiga anfall kan vara mindre av en prediktor för PTE hos barn; medan så många som en tredjedel av vuxna med tidiga anfall utvecklar PTE, är andelen barn med tidiga PTS som får sena anfall mindre än en femtedel av barn och kan vara så låg som en tiondel. Förekomsten av sena anfall är ungefär hälften så stor som hos vuxna med jämförbara skador.
Epidemiologi

Forskning har funnit att förekomsten av PTS varierar kraftigt baserat på den studerade populationen; den kan vara så låg som 4,4 % eller så hög som 53 %. Av alla TBI-patienter som är inlagda på sjukhus har 5 till 7 % PTS. PTS förekommer i cirka 3,1 % av traumatiska hjärnskador, men skadans svårighetsgrad påverkar sannolikheten för att det inträffar.
Den viktigaste faktorn för om en person kommer att utveckla tidiga och sena anfall är omfattningen av skadan på hjärnan. En svårare hjärnskada medför också risk för att utveckla PTS under en längre tid efter händelsen. En studie fann att sannolikheten för att anfall kommer att inträffa inom 5 år efter skada är 0,5 % av lindriga traumatiska hjärnskador (definierad som ingen skallfraktur och mindre än 30 minuter av posttraumatisk amnesi, förkortat PTA, eller medvetslöshet , förkortat LOC); 1,2 % av måttliga skador (skallfraktur eller PTA eller LOC som varar mellan 30 minuter och 24 timmar); och 10,0 % av allvarliga skador (cerebral kontusion, intrakraniellt hematom eller LOC eller PTA i över 24 timmar). En annan studie fann att risken för anfall 5 år efter TBI är 1,5 % vid mild (definierad som PTA eller LOC under mindre än 30 minuter), 2,9 % vid måttlig (LOC som varar mellan 30 minuter och 1 dag) och 17,2 % vid svår TBI (cerebral kontusion, subduralt hematom eller LOC i över en dag; bild till höger).
Omedelbara anfall har en incidens på 1 till 4 %, den för tidiga anfall är 4 till 25 % och den för sena anfall är 9 till 42 %.
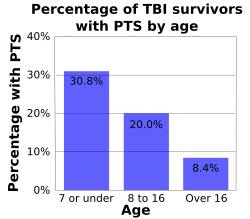
Ålder påverkar risken för PTS. När åldern ökar minskar risken för tidiga och sena anfall; en studie fann att tidig PTS inträffade hos 30,8 % av barnen 7 år eller yngre, 20 % av barnen mellan 8 och 16 år och 8,4 % av personerna som var över 16 år när de skadades (grafen till höger). Tidiga anfall förekommer upp till dubbelt så ofta hos hjärnskadade barn som de gör hos sina vuxna motsvarigheter. I en studie fick barn under fem år med triviala hjärnskador (de utan LOC, ingen PTA, ingen deprimerad skallfraktur och ingen blödning) ett tidigt anfall 17 % av tiden, medan personer över 5 år gjorde det endast 2 % av tiden. Barn under fem år får också anfall inom en timme efter skadan oftare än vad vuxna gör. En studie fann att förekomsten av tidiga anfall var högst bland spädbarn yngre än ett år och särskilt hög bland de som fick perinatal skada. Vuxna löper dock högre risk än barn för sena anfall. Personer över 65 år löper också större risk att utveckla PTS efter en skada, med en PTS-risk som är 2,5 gånger högre än deras yngre motsvarigheter.
Riskfaktorer
Chanserna att en person ska utveckla PTS påverkas av faktorer som involverar skadan och personen. De största riskerna för PTS är att ha en förändrad medvetandenivå under en utdragen tid efter skadan, svåra skador med fokala lesioner och frakturer. Den enskilt största risken för PTS är penetrerande huvudtrauma , som medför en risk på 35 till 50 % för anfall inom 15 år. Om ett metallfragment finns kvar i skallen efter skada kan risken för både tidig och sen PTS öka. Överlevande i huvudtrauma som missbrukade alkohol före skadan löper också högre risk att utveckla anfall.
Förekomsten av anfall varierar stort även bland personer med liknande skador. Det är inte känt om genetik spelar en roll i PTS-risk. Studier har haft motstridiga resultat när det gäller frågan om personer med PTS är mer benägna att ha familjemedlemmar med anfall, vilket skulle tyda på en genetisk roll vid PTS. De flesta studier har funnit att epilepsi hos familjemedlemmar inte nämnvärt ökar risken för PTS. Personer med ApoE-ε4- allelen kan också ha högre risk för sen PTS.
Risker för sen PTS inkluderar hydrocefalus , minskat blodflöde till tinningloberna i hjärnan, kontusion i hjärnan , subdurala hematom , en trasig dura mater och fokala neurologiska underskott . PTA som varar längre än 24 timmar efter skadan är en riskfaktor för både tidig och sen PTS. Upp till 86 % av personer som har ett sent posttraumatiskt anfall får ett annat inom två år.