Minigene
En minigen är ett minimalt genfragment som inkluderar en exon och de kontrollregioner som är nödvändiga för att genen ska uttrycka sig själv på samma sätt som ett vildtypsgenfragment . Detta är en minigen i sin mest grundläggande betydelse. Mer komplexa minigener kan konstrueras innehållande multipla exoner och intron(er) . Minigener ger ett värdefullt verktyg för forskare som utvärderar skarvningsmönster både in vivo och in vitro biokemiskt utvärderade experiment. Specifikt används minigener som splitsningsreportervektorer (även kallade exonfångande vektorer) och fungerar som en sond för att bestämma vilka faktorer som är viktiga för splitsningsresultat. De kan konstrueras för att testa hur både cis-regulatoriska element (RNA-effekter) och trans-regulatoriska element (associerade proteiner / splitsningsfaktorer ) påverkar genuttryck.
Historia
Minigener beskrevs först som den somatiska sammansättningen av DNA-segment och bestod av DNA-regioner som var kända för att koda för proteinet och de flankerande regioner som krävs för att uttrycka proteinet. Termen användes först i en artikel 1977 för att beskriva kloningen av två minigener som designades för att uttrycka en peptid.
RNA-skarvning upptäcktes i slutet av 1970-talet genom studiet av adenovirus som invaderar däggdjur och replikerar inuti dem. Forskare identifierade RNA-molekyler som innehöll sekvenser från icke sammanhängande delar av virusets genom. Denna upptäckt ledde till slutsatsen att det fanns regleringsmekanismer som påverkade moget RNA och de gener som det uttrycker. Att använda minigener som en splitsningsrapporteringsvektor för att utforska effekterna av RNA-splitsningsreglering följde naturligt och är fortfarande den största användningen av minigener hittills.
Typer
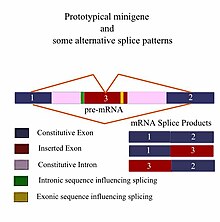
För att tillhandahålla en bra minigenmodell bör genfragmentet ha alla nödvändiga element för att säkerställa att det uppvisar samma alternativa splitsningsmönster (AS) som vildtypsgenen , dvs. längden på fragmentet måste inkludera alla uppströms och nedströms sekvenser som kan påverka dess splitsning. Därför börjar de flesta minigendesigner med en grundlig silicoanalys av kraven för experimentet innan något "vått" labbarbete utförs. Med tillkomsten av bioinformatik och utbredd användning av datorer finns det nu flera bra program för identifiering av cis-verkande kontrollregioner som påverkar splitsningsresultaten för en gen och avancerade program kan till och med överväga splitsningsresultat i olika vävnadstyper. Skillnader i minigener återspeglas vanligtvis i den slutliga storleken på fragmentet, vilket i sin tur är en återspegling av själva minigenens komplexitet. Antalet främmande DNA-element (exon och introner) som infogas i de konstitutiva exonerna och intronerna av ett givet fragment varierar med typen av experiment och den information som söks. Ett typiskt experiment kan involvera vildtypsminigener som förväntas uttrycka gener normalt i en jämförelse körd mot genetiskt modifierade allelvariationer som ersätter vildtypsgenen och har klonats in i samma flankerande sekvenser som det ursprungliga fragmentet. Dessa typer av experiment hjälper till att bestämma effekten av olika mutationer på pre-mRNA splitsning.
Konstruktion
När väl ett lämpligt genomiskt fragment har valts (steg 1), kan exonerna och intronerna av fragmentet infogas och amplifieras, tillsammans med de flankerande konstitutiva exonerna och intronerna av den ursprungliga genen, genom PCR . Primers för PCR kan väljas så att de lämnar " klibbiga ändar " vid 3'-sens och anti-sense-strängar (steg 2). Dessa "klibbiga ändar" kan lätt inkorporeras i en TOPO-vektor genom ligering i en kommersiellt tillgänglig källa som redan har ligas fäst vid inkorporeringen (steg 3). De efterföljande TOPO-vektorerna kan transfekteras in i E. coli-celler (steg 4). Efter inkubation kan totalt RNA extraheras från bakteriekolonierna och analyseras med hjälp av RT-PCR för att kvantifiera förhållandena för exon-inklusion/exclusion (steg 5). Minigenen kan transfekteras till olika celltyper med olika splitsningsfaktorer för att testa transverkande element (steg 6). De uttryckta generna eller proteinerna de kodar för kan analyseras för att utvärdera splitsningskomponenter och deras effekter via en mängd olika metoder inklusive hybridisering eller storleksuteslutningskromatografi .
Används
RNA splitsningsfel har uppskattats förekomma i en tredjedel av genetiska sjukdomar. [ citat behövs ] För att förstå patogenes och identifiera potentiella mål för terapeutisk intervention i dessa sjukdomar är det viktigt att förklara de involverade splitsningselementen. Att bestämma den kompletta uppsättningen av komponenter som är involverade i splitsning ger många utmaningar på grund av överflöd av alternativ splitsning, som förekommer i de flesta mänskliga gener, och specificiteten i vilken splitsning utförs in vivo . Splitsning utförs distinkt från celltyp till celltyp och över olika stadier av cellulär utveckling. Därför är det avgörande att alla in vitro eller bioinformatiska antaganden om splitsningsreglering bekräftas in vivo . Minigener används för att belysa cis -regulatoriska element, trans -regulatoriska element och andra regulatorer av pre-mogen RNA-splitsning in vivo . Minigener har använts för att studera en mångfald av genetiska sjukdomar på grund av det ovannämnda överflöd av alternativt splitsade gener och specificiteten och variationen som observerats vid splitsningsreglering. Följande är exempel på minigenanvändning vid olika sjukdomar. Även om det inte är en uttömmande lista, ger den en bättre förståelse för hur minigener används.
Endokrina sjukdomar
RNA-skarvningsfel kan ha drastiska effekter på hur proteiner fungerar, inklusive de hormoner som utsöndras av det endokrina systemet . Dessa effekter på hormoner har identifierats som orsaken till många endokrina störningar, inklusive sköldkörtelrelaterade patologiska tillstånd, rakitis , hyperinsulinemisk hypoglykemi och medfödd binjurehyperplasi . Ett specifikt exempel på ett skarvningsfel som orsakar en endokrin sjukdom som har studerats med minigener är en typ av tillväxthormonbrist som kallas isolerad tillväxthormonbrist (IGHD), en sjukdom som resulterar i tillväxtsvikt. IGHD typ II är en autosomal dominant form som orsakas av en mutation i den intervenerande sekvensen (IVS) intill exon 3 av genen som kodar för tillväxthormon 1, GH-1-genen. Denna muterade form av IVS3 gör att exon 3 hoppas över i mRNA-produkten. mRNA (-E3) kodar för en trunkerad form av hGH som sedan hämmar normal hGH-utsöndring. Minigener användes för att fastställa att en punktmutation i en intronsplitsningsförstärkare (ISE) inbäddad i IVS3 var skyldig till att E3 hoppades över. Dessutom fastställdes det att funktionen hos ISE påverkas av ett närliggande transponerbart AC-element , vilket avslöjar att detta speciella skarvningsfel orsakas av en transagerande faktor.
Neurodegenerativa sjukdomar
Ackumulering av tau-protein är associerat med neurodegenerativa sjukdomar inklusive Alzheimers och Parkinsons sjukdomar samt andra tauopatier . Tau-proteinisoformer skapas genom alternativ splitsning av exon 2, 3 och 10. Regleringen av tau-splitsning är specifik för utvecklingsstadiet, fysiologi och plats. Fel i tau-splitsning kan förekomma i både exoner och introner och, beroende på felet, resultera i förändringar i proteinstruktur eller funktionsförlust. Aggregering av dessa onormala tau-proteiner korrelerar direkt med patogenes och sjukdomsprogression. Minigener har använts av flera forskare för att hjälpa till att förstå de regulatoriska komponenterna som är ansvariga för mRNA-splitsning av TAU-genen.
Cancer
Cancer är en komplex, heterogen sjukdom som kan vara ärftlig eller ett resultat av miljöstimulans. Minigener används för att hjälpa onkologer att förstå rollerna pre-mRNA splitsning spelar i olika cancertyper. Av särskilt intresse är cancerspecifika genetiska mutationer som stör normala splitsningshändelser, inklusive de som påverkar spliceosomkomponenter och RNA-bindande proteiner såsom heterogena nukleära ribonukleopartiklar (hnRNP), serin /argininrika (SR) proteiner och små ribonukleoproteiner (snRNP) . Proteiner som kodas av avvikande splitsade pre-mRNA är funktionellt olika och bidrar till de karakteristiska anomalierna som uppvisas av cancerceller, inklusive deras förmåga att föröka sig, invadera och genomgå angiogenes och metastaser. Minigener hjälper forskare att identifiera genetiska mutationer i cancer som resulterar i splitsningsfel och bestämma nedströmseffekterna dessa splitsningsfel har på genuttryck. Med hjälp av kunskap erhållen från studier som använder minigener, har onkologer föreslagit tester utformade för att upptäcka produkter av onormalt genuttryck för diagnostiska ändamål. undersöks möjligheten att använda minigener som en cancerimmunterapi .
Se även
Vidare läsning
- "Alternativ pre-mRNA Splicing: Theory and Protocols", av Stefan Stamm, Chris Smith och Reinhard Lührmann ISBN 978-3527326068
- "Molecular Diagnostics, andra upplagan", av Ed. av George P. Patrinos och Whilhelm Ansorge ISBN 0123745373
- "DNA Vaccines" redigerad av Hildegun Ertl ISBN 1461349257
- "Alternativ splitsning och sjukdom (framsteg inom molekylär och subcellulär biologi)" av Philippe Jeanteur ISBN 3540344489
externa länkar
- Stefan Stamms webbsida vid University of Kentucky . Bra översikt över minigenforskning.
- Christopher Burges Lab på MIT webbplats . En bra sida för teoretisk analys av skarvning.
- UCSC Genome Browser . Stor databas för att hämta information om gener.
