Kjeldahls metod
Kjeldahlmetoden eller Kjeldahl digestion ( danskt uttal: [ˈkʰelˌtɛˀl] ) inom analytisk kemi är en metod för kvantitativ bestämning av kväve som finns i organiska ämnen plus kvävet som finns i de oorganiska föreningarna ammoniak och ammonium ( NH43 + ) . Utan modifiering, andra former av oorganiskt kväve, till exempel nitrat , ingår inte i denna mätning. Med hjälp av ett empiriskt samband mellan Kjeldahls kväveinnehåll och proteininnehåll är det en viktig metod för att analysera proteiner. Denna metod utvecklades av Johan Kjeldahl 1883.
Metod
Metoden består i att värma upp ett prov till 360–410 °C med koncentrerad svavelsyra (H 2 SO 4 ), som sönderdelar (”röter” eller ”förstör”) det organiska provet genom oxidation för att frigöra det reducerade kvävet som ammoniumsulfat . Varm koncentrerad svavelsyra oxiderar kol (som bituminöst kol) och svavel (se svavelsyras reaktioner med kol ):
- C + 2 H 2 SO 4 → CO 2 + 2 SO 2 + 2 H 2 O
- S + 2 H 2 SO 4 → 3 SO 2 + 2 H 2 O
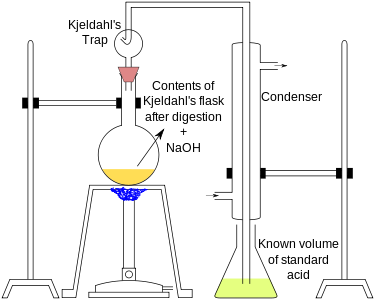
Katalysatorer som selen , Hg 2 SO 4 eller CuSO 4 tillsätts ofta för att rötningen ska gå snabbare. Na 2 SO 4 eller K 2 SO 4 tillsätts också för att öka kokpunkten för H 2 SO 4 . Matsmältningen är klar när vätskan klarnar med utsläpp av ångor. Ett destillationssystem som avbildas nedan byggs.
 |
|
Änden av kondensorn doppas i en känd volym standardsyra (dvs syra med känd koncentration). En svag syra som borsyra (H 3 BO 3 ) i överskott av ammoniak används ofta. Standardiserad HCl , H 2 SO 4 eller någon annan stark syra kan användas istället, men detta är mindre vanligt. Provlösningen destilleras sedan med en liten mängd natriumhydroxid (NaOH). NaOH kan även tillsättas med en dropptratt . NaOH reagerar på ammonium (NH 4 + ) till ammoniak (NH 3 ), som kokar bort provlösningen. Ammoniak bubblar genom standardsyralösningen och reagerar tillbaka till ammoniumsalter med den svaga eller starka syran.
Ammoniumjonkoncentrationen i den sura lösningen, och därmed mängden kväve i provet, mäts via titrering. Om borsyra (eller någon annan svag syra) användes görs direkt syra-bastitrering med en stark syra med känd koncentration. HCl eller H2SO4 kan användas . Indirekt tillbakatitrering används istället om starka syror användes för att göra standardsyralösningen: stark bas med känd koncentration (som NaOH) används för att neutralisera lösningen. I detta fall beräknas mängden ammoniak som skillnaden mellan mängden HCl och NaOH. Vid direkt titrering är det inte nödvändigt att veta den exakta mängden svag syra (t.ex. borsyra) eftersom den inte stör titreringen (det måste vara i överskott av ammoniak för att effektivt fånga in den). Således behövs en standardlösning (t.ex. HCl) i den direkta titreringen, medan två behövs (t.ex. HCl och NaOH) i backtitreringen. En av de lämpliga indikatorerna för dessa titreringsreaktioner är Tashiros indikator .
I praktiken är denna analys till stor del automatiserad; specifika katalysatorer påskyndar nedbrytningen. Ursprungligen var den valda katalysatorn kvicksilveroxid. Men även om det var mycket effektivt ledde hälsoproblem till att det ersattes av kopparsulfat. Kopparsulfat var inte lika effektivt som kvicksilveroxid och gav lägre proteinresultat. Det kompletterades snart med titandioxid, som för närvarande är den godkända katalysatorn i alla analysmetoder för protein i AOAC Internationals officiella metoder och rekommenderade metoder.
Ansökningar
Kjeldahl-metodens universalitet, precision och reproducerbarhet har gjort den till den internationellt erkända metoden för att uppskatta proteinhalten i livsmedel och det är standardmetoden mot vilken alla andra metoder bedöms. Det används också för att analysera jordar, avloppsvatten, gödningsmedel och andra material. Det ger dock inget mått på verkligt proteininnehåll, eftersom det mäter icke-proteinkväve utöver kvävet i proteiner. Detta bevisas av 2007 års sällskapsdjursincident och den kinesiska mjölkpulverskandalen 2008, då melamin , en kväverik kemikalie, sattes till råvaror för att fejka höga proteinhalter. Dessutom behövs olika korrigeringsfaktorer för att olika proteiner ska stå för olika aminosyrasekvenser. Ytterligare nackdelar, såsom behovet av att använda koncentrerad svavelsyra vid hög temperatur och den relativt långa testtiden (en timme eller mer), är ofördelaktigt att jämföra med Dumas- metoden för mätning av råproteininnehåll.
Totalt Kjeldahl-kväve
Totalt Kjeldahl-kväve eller TKN är summan av kväve bundet i organiska ämnen, kväve i ammoniak (NH 3 -N) och i ammonium (NH 4 + -N) vid kemisk analys av jord, vatten eller avloppsvatten (t.ex. avloppsrening) anläggningens avloppsvatten).
Idag är TKN en obligatorisk parameter för myndighetsrapportering vid många reningsverk och som ett sätt att övervaka anläggningens drift.
Omvandlingsfaktorer
TKN används ofta som surrogat för protein i livsmedelsprover . Omvandlingen från TKN till protein beror på vilken typ av protein som finns i provet och vilken del av proteinet som består av kvävehaltiga aminosyror , som arginin och histidin . . Utbudet av omvandlingsfaktorer är dock relativt snävt. Exempel på omvandlingsfaktorer, kända som N-faktorer, för livsmedel varierar från 6,38 för mejeriprodukter och 6,25 för kött, ägg, majs (majs) och sorghum till 5,83 för de flesta spannmål; 5,95 för ris, 5,70 för vetemjöl och 5,46 för jordnötter. I praktiken används 6,25 för nästan alla livsmedel och foder oavsett tillämplighet. Faktorn 6,25 krävs specifikt av US Nutrition Label-bestämmelser i frånvaro av en annan publicerad faktor.
| Animaliskt ursprung | Faktor | Gräsfrö | Faktor | Bönor och jordnötter | Faktor |
|---|---|---|---|---|---|
| Ägg | 6,25 | Korn | 5,83 | Castorböna | 5.30 |
| Kött | 6,25 | Majs ( majs ) | 6,25 | Jack bean | 6,25 |
| Mjölk | 6,38 | Hirsar | 5,83 | limaböna | 6,25 |
| Havre | 5,83 | Marinblå böna | 6,25 | ||
| Ris | 5,95 | Mungböna | 6,25 | ||
| råg | 5,83 | Sojaböna | 5,71 | ||
| Durra | 6,25 | Sammetsböna | 6,25 | ||
| Vete : Hel kärna | 5,83 | Jordnötter | 5,46 | ||
| Vete : kli | 6,31 | ||||
| Vete : Endosperm | 5,70 |
Känslighet
Kjeldahl-metoden är dåligt känslig i originalversionen. Andra detektionsmetoder har använts för att kvantifiera NH 4 + efter mineralisering och destillation, för att uppnå förbättrad känslighet: in-line generator av hydrid kopplad till en plasma atomemissionsspektrometer (ICP-AES-HG, 10–25 mg/L), potentiometrisk titrering (>0,1 mg kväve), zonkapillärelektrofores (1,5 µg/ml kväve) och jonkromatografi (0,5 µg/ml).
Begränsningar
Kjeldahl-metoden är inte tillämpbar på föreningar som innehåller kväve i nitro- och azogrupper och kväve som finns i ringar (t.ex. pyridin , kinolin , isokinolin ) eftersom kväve i dessa föreningar inte omvandlas till ammoniumsulfat under betingelserna för denna metod.
Se även
- Dumas metod , en annan kväveanalysmetod
- Devardas legering , ett kraftfullt reduktionsmedel för nitratanalys
- Bicinchoninsyraanalys , en kolorimetrisk analys för protein-kväve
- Förbränningsanalys en annan kol-, väte- och kväveanalysmetod
Bibliografi
- Wastewater Engineering: Treatment and Reuse , Metcalf & Eddy, McGraw-Hill Higher Education; 4:e upplagan, 1 maj 2002, ISBN 978-0071241403