Icke-oskyldig ligand
Inom kemi är en (redox) icke-oskyldig ligand en ligand i ett metallkomplex där oxidationstillståndet inte är klart. Typiskt är komplex som innehåller icke-oskyldiga ligander redoxaktiva vid milda potentialer . Konceptet antar att redoxreaktioner i metallkomplex är antingen metall- eller ligandlokaliserade, vilket är en förenkling, om än användbar.
CK Jørgensen beskrev först ligander som "oskyldiga" och "misstänkta": "Ligander är oskyldiga när de tillåter oxidationstillstånd för de centrala atomerna att definieras. Det enklaste fallet med en misstänkt ligand är NO ... "
Redoxreaktioner av komplex av oskyldiga vs icke-oskyldiga ligander
Konventionellt antas redoxreaktioner av koordinationskomplex vara metallcentrerade. Reduktionen av MnO 4 − till MnO 4 2− beskrivs av förändringen i mangans oxidationstillstånd från 7+ till 6+. Oxidliganderna ändras inte i oxidationstillstånd, de återstår 2- . Oxid är en oskyldig ligand. Ett annat exempel på konventionellt metallcentrerat redoxpar är [Co(NH3 ) 6 ] 3 + /[Co( NH3 ) 6 ] 2+ . Ammoniak är oskyldig i denna omvandling.
oskyldigt beteende hos ligander illustreras av nickel-bis(stilbenedithiolat) ( [Ni(S2C2Ph2 ) 2 ] z ) . Som alla bis(1,2-ditiolen)-komplex av n d 8 metalljoner kan tre oxidationstillstånd identifieras: z = 2-, 1- och 0. Om liganderna alltid anses vara dianjoniska (som görs i formellt oxidationstillstånd), då kräver z = 0 att nickel har ett formellt oxidationstillstånd på +IV. Det formella oxidationstillståndet för den centrala nickelatomen sträcker sig därför från +II till +IV i ovanstående transformationer (se figur). Det formella oxidationstillståndet skiljer sig emellertid från det verkliga (spektroskopiska) oxidationstillståndet baserat på den (spektroskopiska) metallens d-elektronkonfiguration. Stilben-1,2-ditiolatet beter sig som en redox icke-oskyldig ligand, och oxidationsprocesserna äger faktiskt rum vid liganderna snarare än metallen. Detta leder till bildandet av ligandradikalkomplex. Det laddningsneutrala komplexet (z =0), som uppvisar en partiell singlett-diradikal karaktär, beskrivs därför bättre som en Ni 2+ -derivat av radikalanjonen S 2 C 2 Ph 2 •− . Diamagnetismen i de två ligandradikalerna. Ett annat exempel är högre oxidationstillstånd av kopparkomplex av diamidofenylligander som stabiliseras genom intramolekylär multicentervätebindning
Typiska icke-oskyldiga ligander
- Nitrosyl (NO) binder till metaller i en av två extrema geometrier - böjd där NO behandlas som en pseudohalid (NO − ), och linjär, där NO behandlas som NO + .
- Dioxygen kan vara oskyldigt, eftersom det finns i två oxidationstillstånd, superoxid (O 2 − ) och peroxid (O 2 2− ).
Ligander med förlängd pi-delokalisering såsom porfyriner , ftalocyaniner och korroler och ligander med de generaliserade formlerna [D-CR=CR-D] n− (D = O, S, NR' och R, R' = alkyl eller aryl ) är ofta oskyldiga. Däremot är [D-CR=CR-CR=D] − som NacNac eller acac oskyldiga.
- katekolater och relaterade 1,2-dioxalener.
- ditiolener , såsom maleonitrileditiolat (se exempel på [Ni(S 2 C 2 Ph 2 ) 2 ] n− ovan).
- 1,2- diiminer såsom derivat av 1,2-diamidobensen, 2,2'-bipyridin och dimetylglyoxim . Komplexet Cr( 2,2'-bipyridin ) 3 är ett derivat av Cr(III) bundet till tre bipyridin 1− ligander. Å andra sidan är en-elektronoxidation av [Ru(2,2'-bipyridin) 3 ] 2+ lokaliserad på Ru och bipyridinen beter sig som en normal, oskyldig ligand i detta fall.
- ligander som innehåller ferrocen kan ha oxidationshändelser centrerade på ferrocenjärncentret snarare än det katalytiskt aktiva metallcentret.
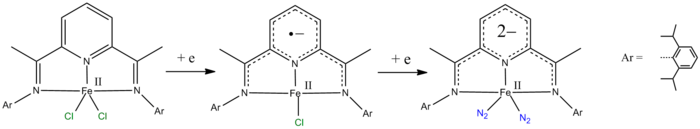
- pyridin-2,6-diiminligander kan reduceras med en och två elektroner.
Redoxa icke-oskyldiga ligander i biologi och homogen katalys
I vissa enzymatiska processer tillhandahåller icke-oskyldiga redoxkofaktorer redoxekvivalenter för att komplettera redoxegenskaperna hos metalloenzymer. Naturligtvis involverar de flesta redoxreaktioner i naturen oskyldiga system, t.ex. [ 4Fe-4S]-kluster . De ytterligare redoxekvivalenterna som tillhandahålls av icke-oskyldiga redoxligander används också som styrande faktorer för att styra homogen katalys.
Hemes

Porfyrinligander kan vara oskyldiga (2-) eller oskyldiga (1-). I enzymerna klorperoxidas och cytokrom P450 upprätthåller porfyrinliganden oxidation under den katalytiska cykeln, särskilt i bildningen av förening I. I andra hemproteiner , såsom myoglobin , förekommer inte ligandcentrerad redox och porfyrinet är oskyldigt.
Galaktosoxidas
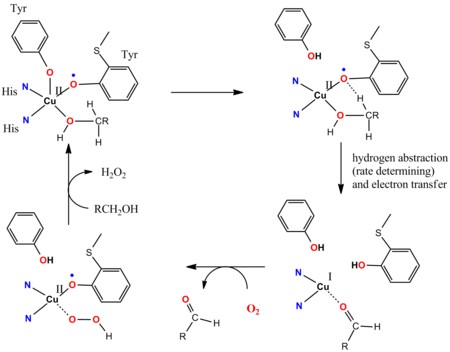
Den katalytiska cykeln av galaktosoxidas (GOas) illustrerar involveringen av icke-oskyldiga ligander. GOase oxiderar primära alkoholer till aldehyder med O 2 och frigör H 2 O 2 . Det aktiva stället för enzymet GOas har en tyrosyl som är koordinerad till en Cu II -jon. I nyckelstegen i den katalytiska cykeln deprotonerar en samverkande Brønsted-baslig ligandplats alkoholen, och därefter tar syreatomen i tyrosinylradikalen bort en väteatom från alfa-CH-funktionaliteten hos det koordinerade alkoxidsubstratet. Tyrosinylradikalen deltar i den katalytiska cykeln: 1e-oxidation utförs av Cu(II/I)-paret och 1e-oxidationen utförs av tyrosylradikalen, vilket ger en total 2e-ändring. Den radikala abstraktionen är snabb. Antiferromagnetisk koppling mellan de oparade spinnen av tyrosinradikalliganden och d9 CuII - centret ger upphov till det diamagnetiska grundtillståndet, i överensstämmelse med syntetiska modeller.
Se även
- ^ Ganguly, Sumit; Ghosh, Abhik (2019-07-16). "Sju ledtrådar till Ligand Noninnocence: The Metallocorrole Paradigm". Redovisningar för kemisk forskning . 52 (7): 2003–2014. doi : 10.1021/acs.accounts.9b00115 . ISSN 0001-4842 . PMID 31243969 .
- ^ Jørgensen CK (1966). "Skillnader mellan de fyra halogenidliganderna och diskussionsanmärkningar om trigonala-bipyramidala komplex, om oxidationstillstånd och om diagonala element av enelektronenergi". Koordinationskemi recensioner . 1 (1–2): 164–178. doi : 10.1016/S0010-8545(00)80170-8 .
- ^ Även om en mer noggrann undersökning av redoxpartnernas elektroniska struktur visar att oxidliganderna påverkas av redoxförändringen, är denna effekt mindre och det formella oxidationstillståndet för syre förblir detsamma.
- ^ Aragoni, M. Carla; Caltagirone, Claudia; Lippolis, Vito; Podda, Enrico; Slawin, Alexandra MZ; Woollins, J. Derek; Pintus, Anna; Arca, Massimiliano (2020-12-07). "Diradikal karaktär av neutrala heteroleptiska bis(1,2-ditiolen) metallkomplex: fallstudie av [Pd(Me2timdt)(mnt)] (Me2timdt = 1,3-dimetyl-2,4,5-tritioxoimidazolidin; mnt2– = 1 ,2-Dicyano-1,2-etylenditiolat)" . Oorganisk kemi . 59 (23): 17385–17401. doi : 10.1021/acs.inorgchem.0c02696 . ISSN 0020-1669 . PMC 7735710 . PMID 33185438 .
- ^ Rajabimoghadam, Khashayar; Darwish, Yousef; Bashir, Umyeena; Pitman, Dylan; Eichelberger, Sidney; Siegler, Maxime A.; Swart, Marcel; Garcia-Bosch, Isaac (2018). "Katalytisk aerob oxidation av alkoholer av kopparkomplex som bär redoxaktiva ligander med avstämbara H-bindningsgrupper" . Journal of the American Chemical Society . 140 (48): 16625–16634. doi : 10.1021/jacs.8b08748 . PMC 6645702 . PMID 30400740 .
- ^ Kaim W, Schwederski B (2010). "Icke-oskyldiga ligander i biooorganisk kemi - en översikt". Koordinationskemi recensioner . 254. (13-14) (13–14): 1580–1588. doi : 10.1016/j.ccr.2010.01.009 .
- ^ Ghosh, Abhik (2017-02-22). "Elektronisk struktur av korrolderivat: Insikter från molekylära strukturer, spektroskopi, elektrokemi och kvantkemiska beräkningar". Kemiska recensioner . 117 (4): 3798–3881. doi : 10.1021/acs.chemrev.6b00590 . ISSN 0009-2665 .
- ^ Zanello P, Corsini M (2006). "Homoleptiska, mononukleära övergångsmetallkomplex av 1,2-dioxolener: Uppdatering av deras elektrokemiska-till-strukturella (röntgen) egenskaper". Koordinationskemi recensioner . 250 (15–16): 2000–2022. doi : 10.1016/j.ccr.2005.12.017 .
- ^ Wang X, Thevenon A, Brosmer JL, Yu I, Khan SI, Mehrkhodavandi P, Diaconescu PL (augusti 2014). "Redoxkontroll av grupp 4 metallringöppnande polymerisationsaktivitet mot L-laktid och e-kaprolakton" . J. Am. Chem. Soc . 136 (32): 11264–7. doi : 10.1021/ja505883u . PMID 25062499 .
- ^ de Bruin B, Bill E, Bothe E, Weyhermüller T, Wieghardt K (juni 2000). "Molekylära och elektroniska strukturer av bis(pyridin-2,6-diimin)metallkomplex [ML2](PF6)n (n = 0, 1, 2, 3; M = Mn, Fe, Co, Ni, Cu, Zn)". Inorg Chem . 39 (13): 2936–47. doi : 10.1021/ic000113j . PMID 11232835 .
- ^ Chirik PJ, Wieghardt K (februari 2010). "Kemi. Radikala ligander ger adel på basmetallkatalysatorer". Vetenskap . 327 (5967): 794–5. doi : 10.1126/science.1183281 . PMID 20150476 .
- ^ Lyaskovskyy V, de Bruin B (2012). "Redox icke-oskyldiga ligander: mångsidiga nya verktyg för att kontrollera katalytiska reaktioner". ACS-katalys . 2 (2): 270–279. doi : 10.1021/cs200660v .
- ^ Luca OR, Crabtree RH (februari 2013). "Redoxaktiva ligander i katalys". Soc Rev. 42 (4): 1440–59. doi : 10.1039/c2cs35228a . PMID 22975722 .
- ^ Chirila, Andrei; Das, Braja Gopal; Kuijpers, Petrus F.; Sinha, Vivek; Bruin, Bas de (2018), "Application of Stimuli-Responsive and "Non-innocent" Ligands in Base Metal Catalysis", Non-Noble Metal Catalysis , John Wiley & Sons, Ltd, s. 1–31, doi : 10.1002/ 9783527699087.ch1 , ISBN 9783527699087
- ^ Whittaker MM, Whittaker JW (mars 1993). "Ligandinteraktioner med galaktosoxidas: mekanistiska insikter" . Biophys. J . 64 (3): 762–72. Bibcode : 1993BpJ....64..762W . doi : 10.1016/S0006-3495(93)81437-1 . PMC 1262390 . PMID 8386015 .
- ^ Wang Y, DuBois JL, Hedman B, Hodgson KO, Stack TD (januari 1998). "Katalytiska galaktosoxidasmodeller: biomimetisk Cu(II)-fenoxyl-radikalreaktivitet". Vetenskap . 279 (5350): 537–40. Bibcode : 1998Sci...279..537W . doi : 10.1126/science.279.5350.537 . PMID 9438841 .
- ^ Müller J, Weyhermüller T, Bill E, Hildebrandt P, Ould-Moussa L, Glaser T, Wieghardt K (mars 1998). "Varför har den aktiva formen av galaktosoxidas ett diamagnetiskt grundtillstånd?". Angew. Chem. Int. Ed. Engl . 37 (5): 616–619. doi : 10.1002/(SICI)1521-3773(19980316)37:5<616::AID-ANIE616>3.0.CO;2-4 . PMID 29711069 .
Vidare läsning
- Dzik, WI; Zhang, XP; de Bruin, B. (2011). "Redox Noninoence of Carbene Ligander: Carbene Radicals in (Katalytic) CC Bond Formation". Oorganisk kemi . 50 (20): 9896–9903. doi : 10.1021/ic200043a . PMID 21520926 .
- Büttner, T.; Geier, J.; Frison, G.; Harmer, J.; Calle, C.; Schweiger, A.; Schönberg, H.; Grützmacher, H. (2005). "Ett stabilt aminylradikalt metallkomplex". Vetenskap . 307. 307 (5707): 235–238. Bibcode : 2005Sci...307..235B . doi : 10.1126/science.1106070 . PMID 15653498 .
- Hetterscheid, DGH; Kaiser, J.; Reijerse, E.; Peters, TPJ; Thewissen, S.; Blok, ANJ; Smits, JMM; de Gelder, R.; de Bruin, B. (2005). "Ir II (eten): Metal eller Carbon Radical?". Journal of the American Chemical Society . 127 (6): 1895–1905. doi : 10.1021/ja0439470 . PMID 15701024 .
- Blanchard, S.; Derat, E.; Desage-El Murr, M.; Fensterbank, L. ; Malacria, M; Mouriès-Mansuy, V. (2012). "Icke-oskyldiga ligander: Nya möjligheter i järnkatalys". European Journal of Inorganic Chemistry . 2012 (3): 376–389. doi : 10.1002/ejic.201100985 .
- Kaim, W. (2012). "Den krympande världen av oskyldiga ligander: konventionella och icke-konventionella redoxaktiva ligander". European Journal of Inorganic Chemistry . 2012 (3): 343–348. doi : 10.1002/ejic.201101359 .