Flytande mosaikmodell
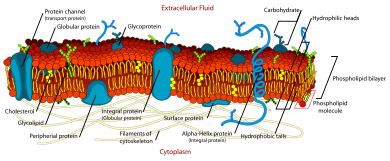
Vätskemosaikmodellen förklarar olika observationer angående strukturen hos funktionella cellmembran . Enligt denna biologiska modell finns det ett lipiddubbelskikt (två molekyler tjockt skikt bestående huvudsakligen av amfipatiska fosfolipider) i vilket proteinmolekyler är inbäddade . Fosfolipiddubbelskiktet ger fluiditet och elasticitet till membranet . Små mängder kolhydrater finns också i cellmembranet. Den biologiska modellen, som utarbetades av Seymour Jonathan Singer och Garth L. Nicolson 1972, beskriver cellmembranet som en tvådimensionell vätska som begränsar den laterala diffusionen av membrankomponenter. Sådana domäner definieras av förekomsten av regioner inom membranet med speciell lipid- och proteinkokong som främjar bildningen av lipidflottor eller protein- och glykoproteinkomplex . Ett annat sätt att definiera membrandomäner är associationen av lipidmembranet med cytoskelettfilamenten och den extracellulära matrisen genom membranproteiner. Den nuvarande modellen beskriver viktiga egenskaper som är relevanta för många cellulära processer, inklusive: cell-cell-signalering , apoptos , celldelning , membranknoppning och cellfusion. Den flytande mosaikmodellen är den mest acceptabla modellen av plasmamembranet. Dess huvudsakliga funktion är att separera innehållet i cellen från det yttre.
Kemisk smink
| Komponenter | Plats | Funktioner |
|---|---|---|
| Fosfolipid | Det huvudsakliga tyget av plasmamembran | Det ger selektiv permeabilitet för cellmembranet. |
| Kolhydrater | Fäst till proteiner på yttre membranskikt | Det hjälper till med cell-till-cell-igenkänning. |
| Kolesterol | Mellan fosfolipider och fosfolipiddubbelskikt | Det hjälper plasmamembranet att behålla sin flytbarhet. |
| Proteiner | Inbäddad i eller på ytan av fosfolipidskikt | Dessa bildar kanaler för att tillåta förflyttning av molekyler. |
Experimentella bevis
Vätskeegenskapen hos funktionella biologiska membran hade bestämts genom märkningsexperiment , röntgendiffraktion och kalorimetri. Dessa studier visade att integrala membranproteiner diffunderar med hastigheter som påverkas av viskositeten hos lipiddubbelskiktet i vilket de var inbäddade, och visade att molekylerna i cellmembranet är dynamiska snarare än statiska.
Tidigare modeller av biologiska membran inkluderade Robertson Unit Membrane Model och Davson-Danielli Tri-Layer-modellen. Dessa modeller hade proteiner närvarande som ark som gränsar till ett lipidskikt, snarare än inkorporerade i fosfolipiddubbelskiktet. Andra modeller beskrev upprepande, regelbundna enheter av protein och lipid. Dessa modeller stöddes inte väl av mikroskopi och termodynamiska data och rymde inte bevis för dynamiska membranegenskaper.
Ett viktigt experiment som gav bevis för att stödja flytande och dynamiska biologiska utfördes av Frye och Edidin. De använde Sendai-virus för att tvinga mänskliga och musceller att smälta samman och bilda ett heterokaryon . Genom att använda antikroppsfärgning kunde de visa att mus- och humanproteinerna förblev segregerade för att separera halvorna av heterokaryon en kort tid efter cellfusion. Proteinerna diffunderade dock så småningom och med tiden gick gränsen mellan de två halvorna förlorad. Sänkning av temperaturen saktade hastigheten för denna diffusion genom att få membranfosfolipiderna att övergå från en vätska till en gelfas. Singer och Nicolson rationaliserade resultaten av dessa experiment med deras flytande mosaikmodell.
Vätskemosaikmodellen förklarar förändringar i struktur och beteende hos cellmembran under olika temperaturer, såväl som associeringen av membranproteiner med membranen. Medan Singer och Nicolson hade betydande bevis från flera delfält för att stödja sin modell, har de senaste framstegen inom fluorescensmikroskopi och strukturbiologi validerat cellmembranens flytande mosaik.
Senare utveckling
Membranasymmetri
Dessutom är de två broschyrerna av biologiska membran asymmetriska och uppdelade i underdomäner sammansatta av specifika proteiner eller lipider, vilket möjliggör rumslig segregering av biologiska processer associerade med membran. Kolesterol och kolesterol-interagerande proteiner kan koncentreras till lipidflottar och begränsa cellsignaleringsprocesser till endast dessa flottar. En annan form av asymmetri visades av Mouritsen och Blooms arbete 1984, där de föreslog en madrassmodell av lipid-proteininteraktioner för att ta itu med de biofysiska bevisen på att membranet kan variera i tjocklek och hydrofobicitet hos proteiner.
Icke-dubbelskiktsmembran
Förekomsten av icke-dubbelskiktiga lipidformationer med viktiga biologiska funktioner bekräftades efter publiceringen av vätskemosaikmodellen. Dessa membranstrukturer kan vara användbara när cellen behöver föröka sig en icke-dubbelskiktsform, vilket inträffar under celldelning och bildandet av en gap junction .
Membrankrökning
Membrandubbelskiktet är inte alltid platt. Lokal krökning av membranet kan orsakas av asymmetri och icke-dubbelskiktsorganisation av lipider som diskuterats ovan. Mer dramatisk och funktionell krökning uppnås genom BAR-domäner , som binder till fosfatidylinositol på membranytan, vilket hjälper till med vesikelbildning , organellbildning och celldelning. Kurvaturutvecklingen är i konstant förändring och bidrar till den dynamiska naturen hos biologiska membran.
Lipidrörelser i membranet
Under decenniet 1970 erkändes det att individuella lipidmolekyler genomgår fri lateral diffusion inom vart och ett av lagren i lipidmembranet. Diffusion sker med hög hastighet, med en genomsnittlig lipidmolekyl som diffunderar ~2 µm, ungefär längden på en stor bakteriecell , på cirka 1 sekund. Det har också observerats att enskilda lipidmolekyler roterar snabbt runt sin egen axel. Dessutom kan fosfolipidmolekyler, även om de sällan gör det, migrera från ena sidan av lipidbiskiktet till den andra (en process som kallas flip-flop). Flip-flop kan dock förstärkas av flippasenzymer. Processerna som beskrivs ovan påverkar den oordnade naturen hos lipidmolekyler och interagerande proteiner i lipidmembranen, med konsekvenser för membranfluiditet, signalering, trafficking och funktion.
Restriktioner för dubbelskiktsfluiditet
Det finns restriktioner för den laterala rörligheten för lipid- och proteinkomponenterna i vätskemembranet som ålagts av bildandet av subdomäner inom lipiddubbelskiktet. Dessa subdomäner uppstår genom flera processer, t.ex. bindning av membrankomponenter till den extracellulära matrisen, nanometriska membranregioner med en speciell biokemisk sammansättning som främjar bildningen av lipidflottor och proteinkomplex medierade av protein-proteininteraktioner. Dessutom förmedlar protein-cytoskelett-associationer bildandet av "cytoskelettstängsel", korraler där lipid- och membranproteiner kan diffundera fritt, men som de sällan kan lämna. Begränsning av lateral diffusionshastighet av membrankomponenter är mycket viktig eftersom det tillåter funktionell specialisering av särskilda regioner inom cellmembranen.
Lipidflottar
Lipidflottar är nanometriska membranplattformar med en speciell lipid- och proteinsammansättning som diffunderar i sidled och navigerar på det flytande bilipidlagret. Sfingolipider och kolesterol är viktiga byggstenar i lipidflotterna.
Proteinkomplex
Cellmembranproteiner och glykoproteiner existerar inte som enskilda element i lipidmembranet, som först föreslogs av Singer och Nicolson 1972. Snarare förekommer de som diffuserande komplex i membranet. Sammansättningen av enstaka molekyler till dessa makromolekylära komplex har viktiga funktionella konsekvenser för cellen; såsom jon- och metabolittransport , signalering, cellvidhäftning och migration .
Cytoskelettstängsel (korraler) och bindning till den extracellulära matrisen
Vissa proteiner inbäddade i bilipidskiktet interagerar med den extracellulära matrisen utanför cellen, cytoskelettfilament inuti cellen och septinringliknande strukturer. Dessa interaktioner har ett starkt inflytande på form och struktur, såväl som på uppdelning . Dessutom inför de fysiska begränsningar som begränsar den fria laterala diffusionen av proteiner och åtminstone några lipider i bilipidskiktet.
När integrala proteiner i lipiddubbelskiktet är bundna till den extracellulära matrisen kan de inte diffundera fritt. Proteiner med en lång intracellulär domän kan kollidera med ett staket som bildas av cytoskelettfilament. Båda processerna begränsar diffusionen av proteiner och lipider som är direkt involverade, såväl som av andra interagerande komponenter i cellmembranen.
Septiner är en familj av GTP-bindande proteiner som är mycket konserverade bland eukaryoter. Prokaryoter har liknande proteiner som kallas paraseptiner. De bildar kompartmentaliserande ringliknande strukturer starkt associerade med cellmembranen. Septiner är involverade i bildandet av strukturer som flimmerhår och flageller, dendritiska ryggar och jästknoppar.
Historisk tidslinje
- 1895 - Ernest Overton antog att cellmembran är gjorda av lipider.
- 1925 – Evert Gorter och François Grendel fann att röda blodkroppsmembran bildas av ett fettlager två molekyler tjockt, dvs de beskrev cellmembranets bilipida natur.
- 1935 – Hugh Davson och James Danielli föreslog att lipidmembran är skikt sammansatta av proteiner och lipider med porliknande strukturer som tillåter specifik permeabilitet för vissa molekyler. Sedan föreslog de en modell för cellmembranet, bestående av ett lipidlager omgivet av proteinlager på båda sidor av det.
- 1957 – J. David Robertson, baserat på elektronmikroskopistudier, etablerar "Unit Membrane Hypothesis". Detta säger att alla membran i cellen, dvs plasma- och organellmembran, har samma struktur: ett dubbelskikt av fosfolipider med monolager av proteiner på båda sidor om det.
- 1972 – SJ Singer och GL Nicolson föreslog vätskemosaikmodellen som en förklaring till data och senaste bevis om cellmembrans struktur och termodynamik.

