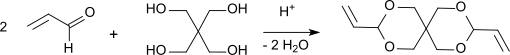3,9-Divinyl-2,4,8,10-tetraoxaspiro(5.5)undekan

|
|
| Namn | |
|---|---|
|
Föredraget IUPAC-namn
3,9-dietenyl-2,4,8,10-tetraoxaspiro[5.5]undekan |
|
| Identifierare | |
|
3D-modell ( JSmol )
|
|
| ECHA InfoCard | 100 000 994 |
| EG-nummer |
|
|
PubChem CID
|
|
| UNII | |
|
|
|
|
| Egenskaper | |
| C11H16O4 _ _ _ _ _ | |
| Molar massa | 212,24 g· mol -1 |
| Utseende | kristallint fast ämne |
| Smältpunkt | 43–46°C |
|
Om inte annat anges ges data för material i standardtillstånd (vid 25 °C [77 °F], 100 kPa).
|
|
3,9-Divinyl-2,4,8,10-tetraoxaspiro[5.5]undekan ( DVTOSU ) är en bicyklisk organisk molekyl med en central kvartär kolatom (en spiroatom ) med vilken två alicykliska ringar är kopplade, var och en bestående av fem atomer . DVTOSU är en diallylacetal och prekursorn för den isomera ketenacetalmonomeren 3,9-dietyliden-2,4,8,10-tetraoxaspiro[5.5]undekan ( DETOSU) som är en byggsten för polyortoestrar .
Nomenklatur
Enligt nomenklaturen som föreslagits av Adolf von Baeyer är spiroföreningen en spiro [5.5]undekan eller, på grund av dess fyra syreatomer, en 2,4,8,10-tetraoxaspiro[5.5]undekan som bär en allylgrupp i varje av positionerna 3 och 9.
Produktion
Kondensationsprodukter från propenal och pentaerytritol beskrevs första gången 1950. Syntesen genomförs med en allmän syntesmetod för acetaler vid surt pH (pH 3-5) genom att en alkohol reagerar med ett överskott av aldehyd, som stabiliseras med hydrokinon i höljet propenal, som tenderar att polymerisera vid förhöjd temperatur.
Efter 19 timmars upphettning under återflöde, neutralisering av oxalsyran , avlägsnande av överskott av aldehyd och reaktionsvattnet, fraktioneras återstoden under vakuum och diallylidenpentaerytritol erhålls i 87 % utbyte. Efter omkristallisation från 60 % metanol erhålls ren DVTOSU i 79 % utbyte med en kokpunkt på 108-110 °C vid 2 Torr och en smältpunkt på 42-42 °C. Graden av omvandling till acetal bestäms av reaktionens jämviktskonstant:
Den vanligaste tekniken för att fullborda acetalbildningen är att avlägsna reaktionsvattnet genom azeotropisk destillation med organiska lösningsmedel som inte är blandbara med vatten, såsom bensen eller toluen . Tendensen hos propenal att polymerisera vid förhöjda temperaturer är problematisk, liksom dess höga flyktighet vid förhöjda temperaturer (som dock krävs för att avlägsna reaktionsvattnet). Det låga rum-tidsutbytet av acetalbildningsreaktionen kräver långa reaktionstider vid förhöjda temperaturer, vid vilka den nukleofila tillsatsen av vatten och alkohol till dubbelbindningen av den omättade aldehyden också leder till oönskade biprodukter. Anpassningen av reaktionsbetingelserna till dessa krav möjliggör produktion av DVTOSU i 80 % utbyte efter 50 min reaktionstid vid 80 °C reaktionstemperatur och 20 % överskott av aldehyd. Avlägsnandet av reaktionsvattnet genom azeotropisk destillation med bensen (som bärare) förkortar reaktionstiden till 10 timmar, varvid efter fraktionerad destillation DVTOSU erhålls i 75 % utbyte med en kokpunkt på 138-141 °C vid 12 Torr. Cykliska acetaler kan även framställas av 1,3-dioler med propenal under mycket skonsamma (rumstemperatur) och kontinuerliga processbetingelser följt av kontinuerlig extraktion med t.ex. n-hexan i utbyten upp till 90 %.
Egenskaper
3,9-Divinyl-2,4,8,10-tetraoxaspiro[5.5]undekan är utan föroreningar ett vitt kristallint pulver. DVTOSU säljs dock ofta som en vätska, på grund av dess låga kristallisationstendens. De mycket varierande data om utbyten och kokpunkter under den första fraktionerade destillationen indikerar biprodukter, t.ex. genom omarrangering av dubbelbindningarna eller nukleofil addition. Framställningen av ren DVTOSU som ett fast ämne kräver upprepad omkristallisering från kolväten som pentan eller n-hexan eller vattenhaltig metanol.
Använda sig av
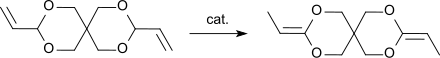
Alkoholer, såsom metanol, och syror, såsom etansyra , kan tillsättas i en nukleofil additionsreaktion till de allyliska dubbelbindningarna av 3,9-divinyl-2,4,8,10-tetraoxaspiro[5.5]undekan till motsvarande 3,9-dimetoxietyl- eller 3,9-diacetoxietyl-2,4,8,10-tetraoxaspiro[5.5]undekan. På liknande sätt kan väteklorid tillsättas i 80 % utbyte eller vätecyanid i 50 % utbyte till motsvarande 3,9-bis(2-kloretyl)- eller 3,9-bis(2-cyanoetyl)-2,4,8, 10-tetraoxaspiro[5.5]undekan. I närvaro av starka syror, såsom bortrifluorid-dietyleterat , reagerar 3,9-divinyl-2,4,8,10-tetraoxaspiro[5.5]undekan med dioler eller disyror för att bilda gummiliknande polymerer som kan tvärbindas till hårda hartser genom ytterligare syratillsats och förhöjda temperaturer. Enligt författarna är de terminala C-atomerna i allylgrupperna i DVTOSU kopplade till di- eller polyolen via eterbindningar. Diallylacetalen 3,9-divinyl-2,4,8,10-tetraoxaspiro[5.5]undekan, DVTOSU, är utgångsföreningen för ketendiacetalen 3,9-dietyliden-2,4,8,10-tetraoxaspiro[5.5] undecan , DETOSU, som bildas genom att dubbelbindningarna flyttas från allylpositionen till vinylpositionen.
DETOSU är i sin tur viktig som en reaktiv monomer för bildandet av polyortoestrar.
- ^ a b c Bidrag från 3,9-Divinyl-2,4,8,10-tetraoxaspiro[5.5 undecane] från TCI Europe, hämtat den {{{Date}}}
- ^ Wolfgang Holland: Die Nomenklatur in der organischen Chemie . VEB Deutscher Verlag für Grundstoffindustrie, Leipzig 1969, S. 81.
- ^ J. Heller; KJ Himmelstein (1985), "[31] Poly(orto ester) biodegradable polymer systems", Methods in enzymology (på tyska), vol. 112, s. 422–436, doi : 10.1016/S0076-6879(85)12033-1 , PMID 3930918
- ^ a b H. Schulz; H. Wagner (1950), "Synthese und Umwandlungsprodukte des Acroleins", Angewandte Chemie (på tyska), vol. 62, nr. 5, s. 105–118, doi : 10.1002/ange.19500620502
- ^ DE 858406 , H. Wagner, "Verfahren zur Herstellung von ungesättigten cyclischen Acetalen", utfärdad 1952-12-08, tilldelad Deutsche Gold- und Silber-Scheideanstalt vormals Roessler
- ^ a b R. F. Fischer; CW Smith (1960), "Cyclic Acrolein Acetals", The Journal of Organic Chemistry (på tyska), vol. 25, nr. 3, s. 319–324, doi : 10.1021/jo01073a002
- ^ a b J. V. Crivello; R. Malik; Y.-L. Lai (1996), "Keteneacetalmonomerer: Synthesis and characterization", Journal of Polymer Science Part A: Polymer Chemistry (på tyska), vol. 34, nr. 15, s. 3091–3102, doi : 10.1002/(SICI)1099-0518(19961115)34:15<3091::AID-POLA1>3.0.CO;2-0
- ^ US 4108869 , HB Copelin, "Beredning av en acetal från en diol och akrolein", utfärdad 1978-8-22, tilldelad EI Du Pont de Nemours och Co.
- ^ Sigma-Aldrich Co. , produktnr. {{{id}}} .
- ^ Frank Brown; DE Hudgin; RJ Kray (1959), "Polymers from the Unsaturated Bisacetals of Pentaerythritol" (PDF) , Journal of Chemical & Engineering Data (på tyska), vol. 4, nr. 2, s. 182–187, doi : 10.1021/je60002a020 , arkiverad från originalet (PDF) 2015-09-24 , hämtad 2019-04-29