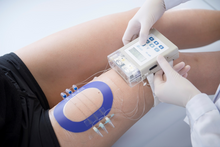
Öppet flöde mikroperfusion
Open flow mikroperfusion ( OFM ) är en provtagningsmetod för kliniska och prekliniska läkemedelsutvecklingsstudier och biomarkörforskning . OFM är designad för kontinuerlig provtagning av analyter från interstitiell vätska (ISF) i olika vävnader. Den ger direkt åtkomst till ISF genom införande av en liten, minimalt invasiv, membranfri sond med makroskopiska öppningar. Således blir hela den biokemiska informationen från ISF tillgänglig oavsett analytens molekylstorlek, proteinbindande egenskap eller lipofilicitet .
OFM kan ta prover på lipofila och hydrofila föreningar, proteinbundna och obundna läkemedel, neurotransmittorer , peptider och proteiner , antikroppar , nanopartiklar och nanobärare , enzymer och vesiklar .
Metod
OFM-sonderna perfunderas med en fysiologisk lösning (perfusatet) som balanserar med ISF för den omgivande vävnaden. Driftflödeshastigheter varierar från 0,1 till 10 μL/min. OFM tillåter obegränsat utbyte av föreningar via en öppen struktur över sondens öppna utbytesområde. Detta utbyte av föreningar mellan probens perfusat och den omgivande ISF drivs av konvektion och diffusion och sker icke-selektivt i endera riktningen (Figur 1).
Den direkta vätskebanan mellan sondens perfusat och den omgivande vätskan resulterar i insamling av ISF-prover. Dessa prover kan samlas in ofta och utsätts sedan för bioanalytisk analys för att möjliggöra övervakning av ämneskoncentrationer med tidsmässig upplösning under hela provtagningsperioden.
Den koncentriska OFM-sonden (Figur 2) fungerar enligt samma princip. Perfusatet pumpas till spetsen av OFM-sonden genom den inre, tunna lumen och kommer ut utanför det öppna utbytesområdet, där det sedan blandas med exogena ämnen som finns i ISF innan det dras ut genom det yttre, tjocka lumen.
Historia
Den första OFM-provtagningssonden som skulle användas som ett alternativ till mikrodialys beskrevs i en österrikisk patentansökan inlämnad av Falko Skrabal 1987, där OFM beskrevs som en anordning som kan implanteras i levande organismers vävnad. 1992 lämnades ett amerikanskt patent in som gör anspråk på en anordning för att bestämma åtminstone en medicinsk variabel i vävnaden hos levande organismer. I ett senare patent av Helmut Masoner, Falko Skrabal och Helmut List avslöjades också en linjär typ av provtagningssonden med makroskopiska cirkulära hål. Alternativa och nuvarande OFM-versioner för dermal och fettvävnad utvecklades av Joanneum Research och patenterades av Manfred Bodenlenz et al. Alternativa material med låg absorption användes för att möjliggöra tillverkning av sonder med diametrar på 0,55 mm och utbytesytor på 15 mm långa. För cerebral applikation patenterades speciella OFM-sonder av Birngruber et al. Dessutom har ett patent lämnats in för att hantera vätskehanteringen av ISF genom att använda en portabel peristaltisk pump med ett flödesområde på 0,1 till 10 µL/min som möjliggör drift av upp till tre sonder per pump.
OFM-system
Två typer av OFM-sonder finns för närvarande tillgängliga: linjära OFM-sonder för implantation i ytliga vävnader som hud (dermal OFM, dOFM) och subkutan fettvävnad (adipose OFM, aOFM) samt koncentriska prober för implantation i olika delar av hjärnan ( cerebral OFM, cOFM).
Användningsområden
OFM används rutinmässigt i farmaceutisk forskning i preklinisk (t.ex. möss, råttor, grisar, primater) och i kliniska studier på människor (Figur 3). OFM-relaterade procedurer såsom sondinsättningar eller förlängd provtagning med många sonder tolereras väl av försökspersonerna.
Dermal OFM (dOFM)
dOFM (Figur 4) möjliggör undersökning av transport av läkemedel i dermis och deras penetration i dermis efter lokal, topisk eller systemisk applicering, och dOFM nämns av US Food and Drug Administration som en ny metod för bedömning av bioekvivalens av topikal läkemedel.
dOFM används för:
- genomföra vävnadsspecifika farmakokinetiska (PK) och farmakodynamiska (PD) studier av läkemedel.
- utföra en direkt jämförelse av nya aktuella läkemedelsformuleringar
- bedöma dermal biotillgänglighet .
- undersöka föreningar med hög molekylvikt, t.ex. antikroppar
Head-to-head-inställningar med OFM har visat sig vara särskilt användbara för utvärdering av aktuella generiska produkter, som måste visa bioekvivalens till den referenslistade läkemedelsprodukten för att få marknadsgodkännande.
Tillämpningar av dOFM inkluderar ex vivo -studier med vävnadsexplantat och prekliniska och kliniska in vivo- studier.
Adipose OFM (aOFM)
aOFM (Figur 4) tillåter kontinuerlig on-line övervakning av metaboliska processer i den subkutana fettvävnaden, t.ex. glukos och laktat , såväl som större analyter såsom insulin (5,9 kDa). Polypeptidernas roll för metabolisk signalering ( leptin , cytokin IL-6, TNFa) har också studerats med aOFM. aOFM möjliggör kvantifiering av proteiner (t.ex. albuminstorlek: 68 kDa) i fettvävnad och öppnar därmed för möjligheten att undersöka proteinbundna läkemedel direkt i perifera målvävnader, såsom högproteinbundna insulinanaloger utformade för ett förlängt, retarderat insulin handling. Senast har aOFM använts för att prova agonister för att studera fetma , lipidmetabolism och immuninflammation. Tillämpningar av aOFM inkluderar ex vivo -studier med vävnadsexplantat och prekliniska och kliniska in vivo- studier.
Cerebral OFM (cOFM)
cOFM (Figur 5) används för att utföra PK/PD prekliniska studier i djurhjärnan. Tillgång till hjärnan inkluderar övervakning av blod-hjärnbarriärens funktion och läkemedelstransport över den intakta blod-hjärnbarriären. cOFM gör det möjligt att ta en titt bakom blod-hjärnbarriären och bedöma koncentrationer och effekter av neuroaktiva ämnen direkt i den riktade hjärnvävnaden.
Blod-hjärnbarriären är en naturlig sköld som skyddar hjärnan och begränsar utbytet av näringsämnen , metaboliter och kemiska budbärare mellan blod och hjärna. Blod-hjärnbarriären förhindrar också potentiella skadliga ämnen från att komma in och skada hjärnan. Men denna mycket effektiva barriär förhindrar också neuroaktiva substanser från att nå lämpliga mål. För forskare som utvecklar neuroaktiva läkemedel är det därför av stort intresse att veta om och i vilken utsträckning en aktiv läkemedelskomponent kan passera blod-hjärnbarriären. Experiment har visat att blod-hjärnbarriären har återupprättats helt 15 dagar efter implantation av cOFM-sonden i hjärnan på råttor. cOFM-sonden har utformats speciellt för att undvika att blod-hjärnbarriären öppnas igen eller orsaka ytterligare trauma på hjärnan efter implantation. cOFM möjliggör kontinuerlig provtagning av cerebral ISF med intakt blod-hjärnbarriär cOFM och möjliggör därmed kontinuerlig PK-övervakning i hjärnvävnad.
Kvantifiering av ISF-föreningar
ISF-föreningar kan kvantifieras antingen indirekt från endast utspädda ISF-prover genom att använda OFM och ytterligare kalibreringstekniker, eller direkt från outspädda ISF-prover som kan samlas in med ytterligare OFM-metoder. Kvantifiering av föreningar från utspädda ISF-prover kräver ytterligare tillämpning av kalibreringsmetoder, såsom nollflödeshastighet, inget nettoflöde eller jonisk referens. Zero Flow Rate har använts i kombination med dOFM av Schaupp et al. för att kvantifiera kalium , natrium och glukos i fett ISF-prover. Inget Net Flux har använts för att kvantifiera flera analyter i OFM-studier i subkutan fett-, muskel- och dermal ISF: de absoluta laktatkoncentrationerna och de absoluta glukoskoncentrationerna i Adipose ISF, den absoluta albuminkoncentrationen i muskel ISF och den absoluta insulinkoncentrationen i fett och muskel-ISF har framgångsrikt bestämts. Dragatin et al. använde No Net Flux i kombination med dOFM för att bedöma den absoluta ISF-koncentrationen av en helt human terapeutisk antikropp. Ionic Reference har använts i kombination med OFM för att bedöma den absoluta glukoskoncentrationen och den absoluta laktatkoncentrationen i fett ISF. Dermal OFM har också använts för att kvantifiera koncentrationerna av humant insulin och en insulinanalog i ISF med inulin som exogen markör.
Ytterligare OFM-metoder, såsom OFM-recirkulation och OFM-sug kan samla outspädda ISF-prover från vilka direkt och absolut kvantifiering av föreningar är möjlig. OFM-recirkulation för att samla outspädda ISF-prover recirkulerar perfusatet i en sluten slinga tills jämviktskoncentrationer mellan perfusat och ISF har etablerats. Med albumin som analyt har 20 recirkulationscykler varit tillräckligt för att nå jämviktskoncentrationer av ISF. OFM-sug utförs genom att applicera ett milt vakuum, som drar ISF från vävnaden in i OFM-sonden.
- ^ a b c Bodenlenz, M.; Aigner, B.; Dragatin, C.; Liebenberger, L.; Zahiragic, S.; Höfferer, C.; Birngruber, T.; Priedl, J.; Feichtner, F.; Schaupp, L.; Korsatko, S.; Ratzer, M.; Magnes, C.; Pieber, TR ; Sinner, F. (april 2013). "Klinisk tillämplighet av dOFM-enheter för hudprovtagning". Hudforskning och -teknik . 19 (4): 474–483. doi : 10.1111/srt.12071 . PMID 23581539 . S2CID 24530499 .
- ^ Altendorfer-Kroath, Thomas; Schimek, Denise; Eberl, Anita; Rauter, Günther; Ratzer, Maria; Raml, Reingard; Sinner, Frank; Birngruber, Thomas (januari 2019). "Jämförelse av cerebral Open Flow mikroperfusion och mikrodialys vid provtagning av små lipofila och små hydrofila substanser". Journal of Neuroscience Methods . 311 : 394-401. doi : 10.1016/j.jneumeth.2018.09.024 . PMID 30266621 . S2CID 52883354 .
- ^ a b c d Schaupp, L.; Ellmerer, M.; Brunner, GA; Wutte, A.; Sendlhofer, G.; Trajanoski, Z.; Skrabal, F.; Pieber, TR; Wach, P. (1 februari 1999). "Direkt tillgång till interstitiell vätska i fettvävnad hos människor genom användning av mikroperfusion med öppet flöde". American Journal of Physiology. Endokrinologi och metabolism . 276 (2): E401–E408. doi : 10.1152/ajpendo.1999.276.2.E401 . PMID 9950802 .
- ^ a b c Ellmerer, Martin; Schaupp, Lukas; Brunner, Gernot A.; Sendlhofer, Gerald; Wutte, Andrea; Wach, Paul; Pieber, Thomas R. (1 februari 2000). "Mätning av interstitiellt albumin i mänsklig skelettmuskel och fettvävnad genom mikroperfusion med öppet flöde". American Journal of Physiology. Endokrinologi och metabolism . 278 (2): E352–E356. doi : 10.1152/ajpendo.2000.278.2.E352 . PMID 10662720 . S2CID 11616153 .
- ^ a b c Dragatin, Christian; Polus, Florine; Bodenlenz, Manfred; Calonder, Claudio; Aigner, Birgit; Tiffner, Katrin Irene; Mader, Julia Katharina; Ratzer, Maria; Woessner, Ralph; Pieber, Thomas Rudolf; Cheng, Yi; Loesche, Christian; Sinner, Frank; Bruin, Gerard (februari 2016). "Secukinumab distribueras till dermal interstitiell vätska hos psoriasispatienter, vilket framgår av mikroperfusion med öppet flöde" . Experimentell dermatologi . 25 (2): 157–159. doi : 10.1111/exd.12863 . PMID 26439798 . S2CID 34556907 .
- ^ Kolbinger, Frank; Loesche, Christian; Valentin, Marie-Anne; Jiang, Xiaoyu; Cheng, Yi; Jarvis, Philip; Peters, Thomas; Calonder, Claudio; Bruin, Gerard; Polus, Florine; Aigner, Birgit; Lee, David M.; Bodenlenz, Manfred; Sinner, Frank; Pieber, Thomas Rudolf; Patel, Dhavalkumar D. (mars 2017). "β-Defensin 2 är en lyhörd biomarkör för IL-17A-driven hudpatologi hos patienter med psoriasis. " Journal of Allergy and Clinical Immunology . 139 (3): 923–932.e8. doi : 10.1016/j.jaci.2016.06.038 . PMID 27502297 . S2CID 30272491 .
- ^ Kleinert, Maximilian; Kotzbeck, Petra; Altendorfer-Kroath, Thomas; Birngruber, Thomas; Tschöp, Matthias H.; Clemmensen, Christoffer (juli 2018). "Tidsupplöst hypotalamisk mikroperfusion med öppet flöde avslöjar normal leptintransport över blod-hjärnbarriären hos leptinresistenta möss. " Molekylär metabolism . 13 : 77–82. doi : 10.1016/j.molmet.2018.04.008 . PMC 6026321 . PMID 29748097 .
- ^ Bodenlenz, Manfred; Dragatin, Christian; Liebenberger, Lisa; Tschapeller, Bernd; Boulgaropoulos, Beate; Augustin, Thomas; Raml, Reingard; Gatschelhofer, Christina; Wagner, Nathalie; Benkali, Khaled; Rony, Francois; Pieber, Thomas; Sinner, Frank (september 2016). "Kinetik av klobetasol-17-propionat i psoriatisk lesional och icke-lesional hud bedömd av dermal Open Flow Microperfusion med tids- och rumsupplösning" . Farmaceutisk forskning . 33 (9): 2229–2238. doi : 10.1007/s11095-016-1960-y . PMC 4967091 . PMID 27271272 .
- ^ a b c Bodenlenz, Manfred; Tiffner, Katrin I.; Raml, Reingard; Augustin, Thomas; Dragatin, Christian; Birngruber, Thomas; Schimek, Denise; Schwagerle, Gerd; Pieber, Thomas R.; Raney, Sam G.; Kanfer, Isadore; Sinner, Frank (januari 2017). "Open Flow Microperfusion som en dermal farmakokinetisk metod för att utvärdera aktuell bioekvivalens" . Klinisk farmakokinetik . 56 (1): 91–98. doi : 10.1007/s40262-016-0442-z . PMC 5222896 . PMID 27539717 . Se även: Bodenlenz, Manfred; Tiffner, Katrin I.; Raml, Reingard; Augustin, Thomas; Dragatin, Christian; Birngruber, Thomas; Schimek, Denise; Schwagerle, Gerd; Pieber, Thomas R.; Raney, Sam G.; Kanfer, Isadore; Sinner, Frank (januari 2017). "Erratum till: mikroperfusion med öppet flöde som en dermal farmakokinetisk metod för att utvärdera aktuell bioekvivalens" . Klinisk farmakokinetik . 56 (1): 99. doi : 10.1007/s40262-016-0487-z . PMC 6828129 . PMID 27873172 .
- ^ F. Skrabal, Vorrichtung zur Bestimmung zumindestens einer medizinischen Substanz in lebenden Organismen, AT391998B, 1987
- ^ F. Skrabal, Process för att bestämma parametrar av intresse i levande organismer, 5 097 834, 1992.
- ^ H. Marsoner, F. Skrabal, H. List, Enhet för att bestämma minst en medicinsk variabel, 5 193 545, 1993.
- ^ M. Bodenlenz, L. Schaupp, Catheter having an oblong slit, WO 2007/131780 A1, 2007.
- ^ M. Bodenlenz, C. Hoefferer, T. Birngruber, L. Schaupp, Filament-baserad kateter, WO 2010/031515, 2010
- ^ WO2012156478A1
- ^ M. Bodenlenz, C. Hoefferer, T. Birngruber, R. Schaller, J. Priedl, F. Feichtner, S. Schock, P. Tkaczyk och L. Schaupp, "Pump för medicinska tillämpningar" DE102011090210A1, 2011. EP; USA;CA; 2011. Patentsökt.
- ^ Ett nytt möjligt långt att utvärdera bioekvivalensen av aktuella droger . US Food and Drug Administration. 25 juni 2019.
- ^ Centrum för drogutvärdering och forskning (22 september 2017). "Impact Story: Utveckling av nya sätt att utvärdera bioekvivalens för aktuella droger" . US Food and Drug Administration.
- ^ Centrum för drogutvärdering och forskning (14 maj 2021). "Topiska dermatologiska produkter" . FY2020 GDUFA Science and Research Report . s. 122–126.
- ^ Bodenlenz, Manfred; Höfferer, Christian; Magnes, Christoph; Schaller-Ammann, Roland; Schaupp, Lukas; Feichtner, Franz; Ratzer, Maria; Pickl, Karin; Sinner, Frank; Wutte, Andrea; Korsatko, Stefan; Köhler, Gerd; Legat, Franz J.; Benfeldt, Eva M.; Wright, Andrew M.; Neddermann, Daniel; Jung, Thomas; Pieber, Thomas R. (augusti 2012). "Dermal PK/PD av ett lipofilt topiskt läkemedel hos psoriasispatienter genom kontinuerlig intradermal membranfri provtagning". European Journal of Pharmaceutics and Biopharmaceutics . 81 (3): 635–641. doi : 10.1016/j.ejpb.2012.04.009 . PMID 22554768 .
- ^ Skrabal, F.; Trajanoski, Z.; Kontscheider, H.; Kotanko, P.; Wach, P. (1 januari 1995). "Bärbart system för on-line kontinuerlig ex vivo-övervakning av subkutan vävnadsglukos med öppen vävnadsperfusion". Medicinsk och biologisk teknik och databehandling . 33 (1): 116–118. doi : 10.1007/BF02522959 . PMID 7616773 . S2CID 6602540 .
- ^ Ellmerer, M; Schaupp, L; Trajanoski, Z; Jobst, G; Moser, I; Urban, G; Skrabal, F; Wach, P (oktober 1998). "Kontinuerlig mätning av subkutan laktatkoncentration under träning genom att kombinera mikroperfusion med öppet flöde och tunnfilmslaktatsensorer". Biosensorer och bioelektronik . 13 (9): 1007–1013. doi : 10.1016/S0956-5663(98)00002-5 . PMID 9839389 .
- ^ a b Cline, Gary W.; Petersen, Kitt Falk; Krssak, Martin; Shen, Jun; Hundal, Ripudaman S.; Trajanoski, Zlatko; Inzucchi, Silvio; Dresner, Alan; Rothman, Douglas L.; Shulman, Gerald I. (22 juli 1999). "Försämrad glukostransport som en orsak till minskad insulinstimulerad muskelglykogensyntes vid typ 2-diabetes". New England Journal of Medicine . 341 (4): 240–246. doi : 10.1056/NEJM199907223410404 . PMID 10413736 .
- ^ Cline, Gary W.; Jucker, Beat M.; Trajanoski, Zlatko; Rennings, Alexander JM; Shulman, Gerald I. (1 februari 1998). "En ny 13 C NMR-metod för att bedöma intracellulär glukoskoncentration i muskler, in vivo". American Journal of Physiology. Endokrinologi och metabolism . 274 (2): E381–E389. doi : 10.1152/ajpendo.1998.274.2.E381 . PMID 9486172 .
- ^ Orban, Zsolt; Remaley, Alan T.; Sampson, Maureen; Trajanoski, Zlatko; Chrousos, George P. (juni 1999). "Den differentiella effekten av matintag och β-adrenerg stimulering på fetthärledda hormoner och cytokiner hos människan" . Journal of Clinical Endocrinology & Metabolism . 84 (6): 2126–2133. doi : 10.1210/jcem.84.6.5747 . PMID 10372721 .
- ^ Bodenlenz, M.; Ellmerer, M.; Schaupp, L.; Jacobsen, LV; Plank, J.; Brunner, GA; Wutte, A.; Aigner, B.; Mautner, SI; Pieber, TR (december 2015). "Biotillgänglighet av insulin detemir och humant insulin på nivån av perifer interstitiell vätska hos människor, bedömd genom mikroperfusion med öppet flöde". Diabetes, fetma och metabolism . 17 (12): 1166–1172. doi : 10.1111/dom.12551 . PMID 26260082 . S2CID 36352136 .
- ^ Birngruber, Thomas; Sinner, Frank (juni 2016). "Cerebral open flow microperfusion (cOFM) ett innovativt gränssnitt till hjärnvävnad". Drug Discovery Today: Teknologier . 20 :19–25. doi : 10.1016/j.ddtec.2016.07.003 . PMID 27986219 .
- ^ Birngruber, Thomas; Raml, Reingard; Gladdines, Werner; Gatschelhofer, Christina; Gander, Edgar; Ghosh, Arijit; Kroath, Thomas; Gaillard, Pieter J.; Pieber, Thomas R.; Sinner, Frank (juli 2014). "Förbättrad doxorubicintillförsel till hjärnan administrerad genom glutation-pegylerat liposomalt doxorubicin (2B3-101) jämfört med generisk Caelyx,®/Doxil®—A Cerebral Open Flow Microperfusion Pilot Study". Journal of Pharmaceutical Sciences . 103 (7): 1945–1948. doi : 10.1002/jps.23994 . PMID 24801480 .
- ^ Birngruber, Thomas; Ghosh, Arijit; Perez-Yarza, Veronica; Kroath, Thomas; Ratzer, Maria; Pieber, Thomas R; Sinner, Frank (december 2013). "Cerebral open flow microperfusion: En ny in vivo-teknik för kontinuerlig mätning av substanstransport över den intakta blod-hjärnbarriären" . Klinisk och experimentell farmakologi och fysiologi . 40 (12): 864–871. doi : 10.1111/1440-1681.12174 . PMID 24256164 . S2CID 29933240 .
- ^ Jacobson, I.; Sandberg, M.; Hamberger, A. (november 1985). "Massöverföring i hjärndialysanordningar - en ny metod för uppskattning av extracellulära aminosyrorkoncentration". Journal of Neuroscience Methods . 15 (3): 263–268. doi : 10.1016/0165-0270(85)90107-4 . PMID 4094481 . S2CID 8495995 .
- ^ Lonnroth, P.; Jansson, PA; Smith, U. (1 augusti 1987). "En mikrodialysmetod som tillåter karakterisering av intercellulärt vattenutrymme hos människor". American Journal of Physiology. Endokrinologi och metabolism . 253 (2): E228–E231. doi : 10.1152/ajpendo.1987.253.2.E228 . PMID 3618773 . S2CID 5766876 .
- ^ Trajanoski, Z.; Brunner, GA; Schaupp, L.; Ellmerer, M.; Wach, P.; Pieber, TR; Kotanko, P.; Skrabal, F. (1 juli 1997). "Open-Flow mikroperfusion av subkutan fettvävnad för on-line kontinuerlig ex vivo mätning av glukoskoncentration". Diabetesvård . 20 (7): 1114–1121. doi : 10.2337/diacare.20.7.1114 . PMID 9203447 . S2CID 27877616 .
- ^ a b Ellmerer, M.; Schaupp, L.; Sendlhofer, G.; Wutte, A.; Brunner, GA; Trajanoski, Z.; Skrabal, F.; Wach, P.; Pieber, TR (december 1998). "Laktatmetabolism av subkutan fettvävnad studerad av Open Flow Microperfusion" . Journal of Clinical Endocrinology & Metabolism . 83 (12): 4394–4401. doi : 10.1210/jcem.83.12.5303 . PMID 9851784 .
- ^ Bodenlenz, Manfred; Schaupp, Lukas A.; Druml, Tatjana; Sommer, Romana; Wutte, Andrea; Schaller, Helga C.; Sinner, Frank; Wach, Paul; Pieber, Thomas R. (augusti 2005). "Mätning av interstitiellt insulin i human fett- och muskelvävnad under måttlig hyperinsulinemi med hjälp av direkt interstitiell tillgång". American Journal of Physiology. Endokrinologi och metabolism . 289 (2): E296–E300. doi : 10.1152/ajpendo.00431.2004 . PMID 15769794 .
- ^ Hummer, Joanna; Schwingenschuh, Simon; Raml, Reingard; Boulgaropoulos, Beate; Schwagerle, Gerd; Augustin, Thomas; Sinner, Frank; Birngruber, Thomas (1 november 2020). "OFM-recirkulation och OFM-sug: avancerade in vivo öppna flödesmikroperfusionsmetoder (OFM) för direkt och absolut kvantifiering av albumin i interstitiell vätska" . Biomedicinsk fysik & teknik Express . 6 (6): 065031. doi : 10.1088/2057-1976/abc3a7 . PMID 33843658 . S2CID 226336167 .