Spike-and-wave
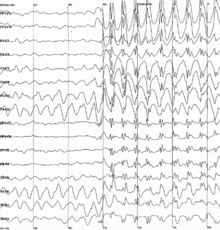
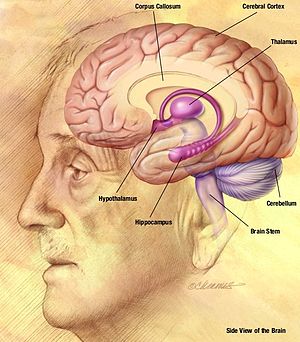
Spike-and-wave är ett mönster av elektroencefalogrammet (EEG) som vanligtvis observeras under epileptiska anfall . En spik-and-wave urladdning är ett regelbundet, symmetriskt, generaliserat EEG-mönster som ses särskilt under frånvaroepilepsi , även känd som "petit mal"-epilepsi. De grundläggande mekanismerna bakom dessa mönster är komplexa och involverar en del av hjärnbarken , det thalamokortikala nätverket och inneboende neuronala mekanismer.
Det första spik-and-wave-mönstret registrerades i början av nittonhundratalet av Hans Berger . Många aspekter av mönstret forskas fortfarande och upptäcks, och fortfarande är många aspekter osäkra. Spike-and-wave-mönstret är vanligast undersökt vid frånvaroepilepsi, men är vanligt vid flera epilepsier som Lennox-Gastaut syndrom (LGS) och Ohtahara syndrom . Antiepileptiska läkemedel (AED) ordineras vanligtvis för att behandla epileptiska anfall, och nya upptäcks med färre biverkningar. Idag är det mesta av forskningen inriktad på ursprunget till den generaliserade bilaterala spik-and-wave-urladdningen. Ett förslag föreslår att en thalamokortikal (TC) loop är involverad i initieringen av spik-och-vågsvängningar. Även om det finns flera teorier, har användningen av djurmodeller gett ny insikt om spik-and-wave urladdning hos människor.
Historia
Historik om generaliserad epilepsi med frånvaroanfall är daterad till 1700-talet, men uppfinnaren av elektroencefalogrammet (EEG), Hans Berger , registrerade det första EEGet av ett frånvaroanfall på 1920-talet, vilket ledde vägen för den allmänna uppfattningen om spike- och vågelektrofysiologi. Hans första inspelning av ett mänskligt EEG gjordes 1924 med en galvanometer, men hans resultat var mycket grova och visade små, odefinierade svängningar. Han fortsatte att förfina sin teknik och öka känsligheten för galvanometern, där han samlade många EEG från individer med och utan hjärnfel eller störning. Bland de som testades fanns patienter med epilepsi, demens och hjärntumörer. Hans Berger publicerade sina fynd 1933, men hans resultat gav inte en definitiv karakterisering av det allmänna EEG-mönstret som ses under ett epileptiskt anfall. 1935 gav FA Gibbs, H. Davis och WG Lennox en tydlig beskrivning av EEG-spets-och-vågmönster under ett petit mal epileptiskt anfall. En intracellulär inspelning utförd av DA Pollen 1964 avslöjade att "spike"-aspekten av fenomenet var associerad med neuronal avfyring och "våg"-aspekten var associerad med hyperpolarisering.
Patofysiologi
Spik-and-wave-mönstret som ses under ett frånvaroanfall är resultatet av en bilateral synkron avfyring av neuroner som sträcker sig från neocortex (en del av hjärnbarken ) till thalamus , längs det talamokortikala nätverket. EEG-"spiken" för spik-and-wave-komplexet motsvarar depolariseringen av den neuronala membranpotentialen, även kallad ett paroxysmalt depolariserande skift (PDS). Den initiala förståelsen bakom mekanismen för PDS var att den orsakades av en mycket stor EPSP ( excitatorisk postsynaptisk potential ) i frånvaro av synaptisk hämning, vilket förmedlade aktionspotentialerna i neuronerna genom att utlösa aktivering av spänningsstyrda kanaler. De spänningsstyrda natriumkanalerna orsakar övergående natriumström in i cellen, vilket genererar aktionspotentialen . De spänningsstyrda kalciumkanalerna har också viss effekt på cellens depolarisering, men effekten är minimal jämfört med natriumkanalerna. Den ökande koncentrationen av intracellulärt kalcium leder dock till större aktivering av kalciumaktiverade kaliumkanaler . Dessa kalciumaktiverade kaliumkanaler, tillsammans med de spänningsstyrda kaliumkanalerna , bidrar till repolarisering och hyperpolarisering av membranet. I ett epileptiskt anfall finns det perioder av en ihållande depolarisering, som orsakar en serie aktionspotentialer följt av en repolariserings- och hyperpolariseringsfas. Tåget av aktionspotentialer utgör "spik"-fasen, och repolariseringen och hyperpolariseringen utgör "våg"-fasen.
Även om det finns bevis för genereringen av en stor EPSP, har många studier visat att synaptisk hämning förblir funktionell under genereringen av dessa typer av paroxysmala depolariserande skift. Det har också visats att en minskning av den hämmande aktiviteten inte påverkar neokortikal tändning. accepteras inte teorin att spik-and-wave-aktivitet orsakas av en gigantisk EPSP på grund av minskningen eller frånvaron av IPSPs ( hämmande postsynaptiska potentialer) som en allmän mekanism för epileptisk aktivitet. Många studier har visat att den hämmande postsynaptiska signaleringen faktiskt ökar under dessa epileptiska attacker. Aktiveringen av postsynaptiska GABAA- receptorer leder till en ökning av den intracellulära kloridkoncentrationen, vilket i icke-epileptiska situationer skulle leda till en IPSP. I anfallsrelaterade depolariserande skift sker emellertid en betydande aktivering av postsynaptiska GABAA- receptorer , vilket leder till en ännu högre koncentration av intracellulär kloridkoncentration. Denna förändring i jonkoncentrationsgradient gör att den GABAA- hämmande strömmen överstiger reverseringspotentialen, vilket leder till ett utflöde av kloridjonerna. Detta leder till en minskad amplitud eller till och med omvänd polaritet hos IPSP:erna.
Metabotropa glutamatreceptorer ( mGluRs ) i det talamokortikala nätverket har också visat sig spela en viss roll i genereringen av spik-and-wave urladdningar (SWDs) associerade med frånvaroepilepsi. De olika subtyperna av mGlu-receptorer har en modulerande roll på antingen excitatorisk eller hämmande synaptisk transmission. Det finns motstridiga hypoteser för funktionen av de många mGlu-receptorerna med avseende på epileptiska anfall, men rollen för mGlu4-receptorn är obestridd i genereringen av SWD, som visas i djurmodeller. I en studie visade knockoutmöss som saknade mGlu4-receptorer en störning av frisättningen av glutamat och GABA i det talamokortikala nätverket och var resistenta mot frånvaroanfall inducerade av låga doser pentylentetrazol . En annan studie visade att bilateral injektion av en mGlu4-receptorantagonist i nRT ( thalamic reticular nucleus ) hos normala möss skyddade mot pentylenetetrazol inducerade anfall. Dessutom visar WAG/Rij-råttor ett ökat uttryck av mGlu4-receptorer i nRT jämfört med en kontrollgrupp av normala råttor. Dessa studier visar att en ökning av uttrycket och/eller aktiviteten av mGlu4-receptorer är associerad med spike-and-wave-urladdningar som ses i frånvaro av anfall. Denna koppling mellan mGlur4-receptorer och SWDs har lett till sökandet efter en selektiv mGlu4-receptorantagonist ( som kommer att blockera dessa receptorer) som ett potentiellt nytt läkemedel för behandling av frånvaroepilepsi.
Initieringsfaktorer
Användningen av djurmodeller, såsom katter, för att studera spik-och-våg-urladdningar, har gett användbara data för att studera epilepsi hos människor. En metod för att framkalla ett anfall hos en katt är att injicera penicillin i den kortikala delen av hjärnan. De spik-and-wave-urladdningar som ses vid felin generaliserad penicillin-epilepsi (FGPE) är mycket lika spik-and-wave-urladdningarna från ett mänskligt frånvaroanfall. Användningen av råttor har också varit en vanlig metod för att studera spik-and-wave-fenomenet. Genetic Absence Epilepsy Rats från Strasbourg (GAERS) och inavlade Wistar Albino Glaxo-råttor från Rijswijk (WAG/Rij) är de två huvudstammarna av råttor som har använts i studier. Råttorna från dessa två stammar visar spontant förekommande frånvaroanfall som består av typisk spik-och-våg-aktivitet som ses på ett EEG. Genetiska råttmodeller har gett data som visar att uttrycket av absenceanfall involverar både thalamus- och kortikala nätverk. I båda modellerna visade elektrofysiologiska data att spike-and-waves initieras i den somatosensoriska cortex och sprids sedan snabbt till den motoriska cortex och talamuskärnor. Genom att använda in vivo intracellulära inspelningar, fann man i GAERS att spik-and-wave initieras i lager 5/6 neuroner i den somatosensoriska cortex. Dessa neuroner visar en distinkt hyperaktivitet associerad med en membrandepolarisering. De föreslås leda avfyrningen av avlägsna kortikala celler under den epileptiska flytningen.
Ett annat möjligt initieringsmönster som testats på råttor antydde att den talamokortikala (TC) slingan är involverad i initieringen av spik-och-vågsvängningar under vissa förhållanden. I denna studie registrerades relä- och retikulära talamusneuroner från epileptiska och icke-epileptiska råttor dubbelt extracellulärt och märkta juxtacellulärt. Mediumoscillationer (5–9 Hz) i båda typerna av råttor noterades att inträffa slumpmässigt i ett osynkroniserat mönster i relä- och retikulära neuroner. Emellertid observerades spontana spike-and-wave-urladdningar hos epileptiska råttor när mediumoscillationerna blev synkroniserade, vilket tyder på ett beroende av de två. Men eftersom medeldistanssvängningar endast utvecklades till spik-och-våg-urladdningar spontant, verkar genetiska faktorer också bidra till initieringen av synkroniserade oscillationer. Dessa genetiska faktorer kan bidra till spik-och-vågsvängningar genom att minska aktionspotentialtröskeln i retikulära celler, vilket gör dem mer exciterade och potentiellt lättare att initiera synkroniserad avfyring. En annan studie har visat att dessa medelstora svängningar har lett till spik-och-våg-urladdningar. Aktiviteten hos de primära och sekundära kortikala regionerna, såväl som den intilliggande insulära cortexen, registrerades med hjälp av ett EEG och applicerades med elektrisk stimulering. Fynden här visade att början av spik-and-wave-urladdning följdes av 5–9 Hz svängningar även i dessa kortikala regioner.
Genetiska/utvecklingsfaktorer
Elongator Protein Complex 4 ( ELP4 ) har identifierats som en nyckelkomponent i transkriptionen av gener som är kända för att reglera aktincytoskelettet, cellmotilitet och migration av neuroner. Forskning på ELP4 har kopplat genen till en centrotemporal fenotyp med skarp spik . Hypoteser har gjorts om att en mutation i den icke-kodande regionen av ELP4- genen kan interferera med elongo-medierad geninteraktion, specifikt under utvecklingsstadierna av den kortikala regionen. Denna mutation kan vara ansvarig för en predisposition för spik-and-wave urladdningar, såväl som andra neuroutvecklingsstörningar.
En annan studie visade att glukos också kan vara relevant för spike-and-wave-förekomst hos möss som innehöll en knock-in av den mänskliga GABA(A) γ2(R43Q)-mutationen, som har varit känd för att vara en genetisk faktor som är involverad i orsakssambandet av frånvaro epilepsi. Dessa möss som är utsatta för frånvaro anfall injicerades med insulin för att sänka blodsockernivåerna med 40 %. Denna minskning av blodsocker ledde till att dubbla förekomsten av spike-and-wave-aktivitet. I likhet med insulineffekten visade fasta över natten, där blodsockernivåerna sänktes med 35 %, också denna dubbla förekomst. Denna modell drar slutsatsen att låga glukosnivåer kan vara en potentiell utlösare för frånvaroanfall och kan vara en miljöriskfaktor för människor.
Spike-and-wave vid epilepsi
Frånvaro epilepsi
Utbrott av generaliserade spik-and-wave-urladdningar som varar i två sekunder eller längre anses vara ett frånvaroanfall . Frånvaroanfall är generaliserade epileptiska anfall som kan delas in i två typer, typiska och atypiska. Typiska och atypiska frånvaroanfall visar två olika typer av spik-och-vågmönster. Typiska frånvaroanfall beskrivs av generaliserade spik-och-vågmönster på ett EEG med en urladdning på 2,5 Hz eller mer. De kan kännetecknas av en ökning av synkroniseringen av urladdningar i thalamokortikala kretsar. De kan också kännetecknas av akut uppkomst och upphörande av anfallet. Atypiska absenceanfall har en högre frekvens hos barn med svår epilepsi som lider av flera typer av anfall. Det spik-och-vågmönster som ses här är mer oregelbundet än det generaliserade mönstret och verkar också vara långsammare. Detta oregelbundna mönster beror på icke-synkrona urladdningar av thalamokortikala kretsar. Debuten och upphörandet av dessa atypiska absenceanfall verkar vara mindre akuta än de typiska absenceanfallen.
Lennox-Gastaut syndrom
Epileptiska encefalopatier är en grupp tillstånd som resulterar i försämring av sensoriska, kognitiva och motoriska funktioner på grund av konsekvent epileptisk aktivitet. Lennox-Gastauts syndrom ( LGS) är en epileptisk encefalopati hos barn som kännetecknas av generaliserade anfall och långsam spikvågsaktivitet när du är vaken. LGS är en kombination av atonisk frånvaro, toniska anfall, kognitiv försämring och långsam spikvågsaktivitet i EEG. Detta syndrom beror vanligtvis på fokal, multifokal eller diffus hjärnskada och kan delas in i symtomatiska och kryptogena typer. Kognitiv försämring med högfrekvent spikvågsaktivitet drabbar de flesta patienter 2–9 år gamla med generaliserade anfall. Debutåldern för LGS är mellan 1 och 10 år, mellan 2 och 6 år för symtomatiska fall och 5 och 8 år för kryptogena fall. Episoder kan utlösas av modifieringar av behandlingen, som vanligtvis involverar bensodiazepiner, eller förändringar i livsvillkoren.
Ohtaharas syndrom
Ohtaharas syndrom (OS), även känt som tidig infantil epileptisk encefalopati (EIEE) med suppression-burst (SB), är den allvarligaste och tidigast utvecklande epileptiska encefalopati hos barn. Detta syndrom kännetecknas på ett EEG av högspänningsskurar och långsamma vågor blandade med multifokala spikar omväxlande med nästan platta undertryckningsfaser. SB kommer gradvis att börja avta vid 3 månader och försvinna efter 6 månader. OS kommer att övergå till West syndrom eller LGS med åldern. Toniska spasmer är de viktigaste anfallen som observeras i OS. Till skillnad från LGS är spik-and-wave-mönstret konsekvent under både vaket och sovande tillstånd. Symtom på OS inkluderar:
- Genetiska defekter
- Mitokondriell sjukdom
- Mitokondriella andningskedjadefekter
- Medfödda metabolismfel
- Glycinencefalopati
- Kortikala missbildningar
- Cerebral asymmetri
- Posterior fossa anomalier
- Agenesis av mammillära kroppar
- Frekventa mindre generaliserade anfall
- Allvarlig och kontinuerlig epileptisk EEG-avvikelse
- Svår psykomotorisk prognos
Spike-and-wave-mönster under sömnen
Vid kontinuerligt spik-and-wave-syndrom (CSWS), en sällsynt form av åldersrelaterad epilepsi, uppvisar barn mellan tre och sju år kontinuerliga spike-and-wave-urladdningar under långsam sömn. Denna störning finns i 0,2–0,5 % av alla barnepilepsifall. Denna sjukdoms flytningar resulterar sällan i absenceanfall, men motorisk funktionsnedsättning och neurofysiologisk regression har hittats i CSWS. Spike-and-wave-aktivitet upptar cirka 85 % av den icke-snabba ögonrörelsesömnen . Detta kontinuerliga mönster under sömnen, liksom andra aspekter av spik-and-wave-aktivitet, är inte heller helt förstått. Det som dock antas är att det kortikotalamiska neuronala nätverket som är involverat i oscillerande sömnmönster kan börja fungera som en patologisk urladdningskälla.
Klinisk relevans
Återkommande efter ett ensamt oprovocerat anfall hos barn är cirka 50 %, så användningen av antiepileptika ( AED) är mycket utbredd. AED:er syftar till att bromsa överskottsavfyrningen, associerad med spik-och-våg-urladdningar, i början av anfall. De kan orsaka allvarliga biverkningar, så läkare måste vara medvetna om säkerheten och tillåtligheten för varje läkemedel. Dessa negativa effekter är en viktig källa till funktionshinder, sjuklighet och dödlighet. Vissa av de negativa effekterna, såsom allvarliga kutana, hematologiska och leverhändelser, kräver vanligtvis abstinens hos barn och lägger en stor börda på kostnaderna för sjukvården.
Bromid introducerades som det första antiepileptiska läkemedlet för 150 år sedan. På grund av de ovan nämnda negativa effekterna används bromid för närvarande inte som AED. Tidig behandlingsavbrott förekom alldeles för ofta och resulterade så småningom i negativa effekter på flera patienter. Nuvarande behandlingsalternativ inkluderar fenytoin , valproinsyra , etosuximid och de nya antiepileptika. Under de senaste 20 åren har 15 nya antiepileptika med positiva resultat introducerats till allmänheten. Dessa nya AED:er syftar till att förbättra kostnads-nyttobalansen i AED-terapi, förbättra tolerabilitetsprofiler och minska potentialen för läkemedelsinteraktion. Trots dessa stora framsteg finns det alltid utrymme för förbättringar, särskilt när det gäller den skräddarsydda behandlingen av individer som har drabbats av biverkningar av äldre AED.