Nasala kondrocyter
Nasala kondrocyter (NC) finns i det hyalina brosket i nässkiljeväggen och är faktiskt den enda celltypen i vävnaden . I likhet med kondrocyter som finns i ledbrosk , uttrycker NC extracellulära matrisproteiner såsom glykosaminoglykaner och kollagen.
I sin naturliga miljö
Vid födseln är nässkiljeväggen , förutom vomer ''anlage', fullständigt broskaktig. Under andra halvan av det första levnadsåret förbenar septumet progressivt i posterior-anterior riktning genom en process av endokondral förbening. Den återstående broskdelen (karakteriserad som hyalint brosk ) av den mänskliga nässkiljeväggen har en specifik tredimensionell organisation med avseende på lokala skillnader i cellstorlek och mängden extracellulär matris. I det yttre området av brosket är NC många, små, platta och orienterade parallellt med ytan. I de mellanliggande och centrala områdena är NC sfäroida i form, mindre täta och är inriktade vinkelrätt mot broskytan. Broskmatrisen består huvudsakligen av kollagen typ II (90-95%), även om små mängder kollagen typ IX och XI också finns. Näsbrosk är tätt anslutet till perichondrium , bestående av flera lager av bindvävsfibrer (huvudsakligen baserade på typ I-kollagen) som löper parallellt med brosket.
Tillämpningar för vävnadsteknik
Artikulära kondrocyter har typiskt varit den celltyp som använts för broskvävnadsteknikstrategier för ledbroskreparation. Eftersom NC också kan uttrycka hyalint broskspecifika extracellulära matrisproteiner såsom glykosaminoglykaner och kollagen, har NC nyligen också använts för in vitro- konstruktion av broskvävnader.
Cellisolering
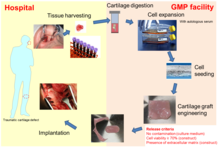
Skörd av näsbrosk är minimalt invasiv , kan utföras i ett polikliniskt förfarande under lokalbedövning och är förknippat med minimal sjuklighet. NC kan isoleras från nässeptala broskbiopsier genom enzymatisk nedbrytning med användning av kollagenas typ I, II eller IV (vid olika kombinationer och koncentrationer – varierande från 0,15 % till 0,6 %) enbart eller efter en initial kort pre-inkubationsfas med pronas (0,2 % - 1 %). Cellutbytet efter enzymatisk nedbrytning av näsbrosket uppskattades till 2 100 - 3 700 celler/mg vävnad. Alternativt kan NC isoleras genom utväxtodling av näsbroskfragment.
Cellexpansion
Efter isolering från septalbroskbiopsier kan NC utökas i stort antal genom konventionella in vitro-cellodlingsmetoder (monolagerodling i kolvar eller petriskålar). Proliferationshastigheten för NC rapporterades öka i närvaro av specifika tillväxtfaktorer såsom TGF-beta och FGF-2 eller kulturtillskott som insulin-transferrin-selen . NC odlat i medium innehållande autologt serum uppvisar liknande proliferationshastigheter som NC odlat med medium kompletterat med fetalt bovint serum . Även om artikulära kondrocyter härrörande från äldre individer har visat sig ha en lägre spridningskapacitet än från yngre donatorer, har NC visat sig ha betydligt mindre åldersberoende.
Differentiering
I likhet med andra kondrocyter från hyalina broskvävnader på andra platser i människokroppen genomgår NC en process av cellavdifferentiering under monolagerodling. NC -de-differentiering kan karakteriseras av ett gradvis förvärv av en fibroblastisk morfologi, uttrycket av proteiner associerade med en odifferentierad mesenkymal cellfenotyp (t.ex. typ I kollagen och versikan) och minskat uttryck av hyalina broskproteiner (t.ex. typ II kollagen och aggrecan). Emellertid kan NC omdifferentiera när den överförs tillbaka till en mer fysiologisk tredimensionell miljö. Riklig produktion av broskspecifik matris har rapporterats av expanderad NC när den induceras att omdifferentiera i mikromassapellets, alginatpärlor, hydrogeler eller till porösa ställningar baserade på polyglykolsyra, polyetylenglykoltereftalat/polybutylenterefalat, kollagen eller hyaluronsyra. Komplettering med specifika tillväxtfaktorer (t.ex. TGF-beta, IGF-1 och GDF-5) under omdifferentiering har visat sig öka ackumuleringen av glykosaminoglykaner (GAG) och typ II-kollagen samt de biomekaniska egenskaperna hos den genererade konstruktioner.
Autologt serum har också använts under NC-omdifferentiering i stället för fetalt bovint serum med liknande effekt. Studier som direkt jämförde omdifferentieringen av artikulära kondrocyter med NC har visat att den broskbildande kapaciteten hos NC var högre och mer reproducerbar än den för artikulära kondrocyter med lägre donatorrelaterat beroende. Dessutom har NC nyligen visat sig uppvisa egenskaper av självförnyelseförmåga, att kunna bilda broskvävnad efter seriekloning, möjligen på grund av deras neuro-ektodermala ursprung.
Djurstudier
Prekliniska undersökningar har utförts med hjälp av olika djurmodeller för att ge principbevis för den kliniska potentialen hos NC-baserade vävnadskonstruerade konstruktioner för broskrekonstruktion. Mognaden av humana NC-konstruerade transplantat har ofta bedömts i den subkutana fickan hos nakna möss , dvs en miljö som är mycket vaskulariserad och tillåtande för, men inte induktiv för, kondrogenes. Omfattningen av broskmatrisproduktion och de mekaniska egenskaperna hos NC-baserade konstruktioner har rapporterats öka i sådana ektopiska in vivo- modeller. En ektopisk musmodell användes också för att testa effekterna av olika produktionsmetoder för att generera stora kliniskt relevanta NC-baserade vävnadstransplantat.
Även om dessa modeller kan ge insiktsfulla resultat, är nakna möss inte kapabla att framkalla ett signifikant immunsvar, och därför kan dessa studier inte förutsäga prognosen för implanterat manipulerat septalbrosk i en immunkompetent värd. Som ett alternativ har en ortotopisk råttmodell etablerats för att studera reparation av nässkiljeväggen. I denna modell perforerades septumbrosk först för att skapa en defekt, och därefter implanterades ett konstruerat brosktransplantat i defekten under samma kirurgiska ingrepp
Med hjälp av en ortotopisk stordjursmodell för att studera reparation av ledbroskdefekter, implanterades konstruerade NC-baserade brosktransplantat i getternas kondyl. I denna studie fastställdes det att NC direkt bidrog till reparationen av ledbroskdefekterna och resulterade i ett överlägset resultat jämfört med konstruerade artikulära kondrocytbaserade transplantat.
Kliniska tillämpningar
Konstruerad broskvävnad, baserad på autolog NC, har nyligen använts av plastikkirurger för rekonstruktion av näsbroskdefekter. Vävnadskonstruerade brosktransplantat baserade på NC som autologa transplantat för rekonstruktion av alarloben i näsan efter hudtumörresektion i en första-i-människ klinisk prövning (ClinicalTrials.gov, nummer NCT01242618) (se figuren till höger). Deras resultat visade att de konstruerade transplantaten kunde leda till fullständig strukturell, funktionell och estetisk tillfredsställelse. Dessutom, eftersom skörd av näsbroskbiopsi var minimalt invasiv, kunde den utföras i ett polikliniskt förfarande under lokalbedövning och var därför associerat med minimal sjuklighet.
Flera studier har visat att NC är kompatibla med de miljöegenskaper som är typiska för det skadade knäet (t.ex. när det gäller svar på inflammatoriska molekyler, mekanisk belastning och genetisk molekylär signatur). Sålunda har nasala kondrocyter föreslagits som en alternativ cellkälla för reparation av ledbroskdefekter. En klinisk fas I-studie (ClinicalTrials.gov, nummer NCT 01605201) genomfördes för att testa säkerheten och genomförbarheten av att implantera ett vävnadskonstruerat brosktransplantat baserat på autologa nasala kondrocyter för regenerering av knäbroskdefekter . De kliniska observationerna av de första 10 patienterna i denna studie indikerade inte bara säkerheten och genomförbarheten av proceduren, utan visade tillsammans med magnetisk resonanstomografi (MRI) och fördröjd gadoliniumförstärkt magnetisk resonanstomografi av broskdata (dGEMRIC) också lovande resultat för effektiviteten av behandlingen som indikeras av signifikant förbättring av kliniska poäng och regenerering av hyalinreparationsvävnad efter 24 månader. Baserat på denna studie inleddes en klinisk fas II-studie med flera centrum och pågår för närvarande för att utvärdera effektiviteten av de NC-baserade brosktransplantaten för reparation av traumatiska knäbroskdefekter (BIO-CHIP; finansierat av Europeiska Unionen genom Horisont 2020- programmet, anslagsnummer 681103).