Demetylering
Demetylering är den kemiska process som resulterar i att en metylgrupp (CH 3 ) avlägsnas från en molekyl. Ett vanligt sätt för demetylering är att ersätta en metylgrupp med en väteatom, vilket resulterar i en nettoförlust av en kol- och två väteatomer.
Motsvarigheten till demetylering är metylering .
I biokemi
I biokemiska system katalyseras demetyleringsprocessen av demetylaser . Dessa enzymer oxiderar N-metylgrupper, som förekommer i histoner och vissa former av DNA:
- R2N -CH3 + O → R2N - H + CH2O
En sådan oxidativ enzymfamilj är cytokrom P450 . Alfa-ketoglutarat-beroende hydroxylaser är aktiva för demetylering av DNA och fungerar på en liknande väg. Dessa reaktioner utnyttjar den svaga CH-bindningen intill aminer .
I synnerhet kan 5-metylcytosiner i DNA demetyleras med TET-enzymer som illustreras i figuren. TET-enzymer är dioxygenaser i familjen av alfa-ketoglutarat-beroende hydroxylaser . Ett TET-enzym är ett alfa-ketoglutarat (α-KG)-beroende dioxygenas som katalyserar en oxidationsreaktion genom att införliva en enda syreatom från molekylärt syre (O 2 ) i dess substrat , 5-metylcytosin i DNA (5mC), för att producera produkten 5-hydroximetylcytosin i DNA. Denna omvandling är kopplad till oxidationen av samsubstratet α-KG till succinat och koldioxid (se figur).
Det första steget involverar bindningen av α-KG och 5-metylcytosin till TET-enzymets aktiva plats . TET-enzymerna har var och en en katalytisk kärndomän med en dubbelsträngad β-helixveck som innehåller de avgörande metallbindande resterna som finns i familjen Fe(II)/α-KG-beroende oxygenaser . α-KG koordinerar som en bidentat ligand (ansluten vid två punkter) till Fe(II) (se figur), medan 5mC hålls av en icke-kovalent kraft i omedelbar närhet. Det aktiva TET-stället innehåller ett mycket konserverat triadmotiv, i vilket den katalytiskt essentiella Fe(II) hålls av två histidinrester och en asparaginsyrarest (se figur). Triaden binder till en sida av Fe-centret och lämnar tre labila platser tillgängliga för bindning av α-KG och O 2 (se figur). TET verkar sedan för att omvandla 5-metylcytosin till 5-hydroximetylcytosin, medan a-ketoglutarat omvandlas till succinat och CO 2 .
Demetylering av vissa steroler är steg i biosyntesen av testosteron och kolesterol . Metylgrupper går förlorade som formiat . Under embryogenesen hos musen demetyleras cirka 20 miljoner 5-metylcytosiner under en sextimmarsperiod strax efter befruktning av ett ägg av en spermie för att bilda en zygot. [ citat behövs ]
Oorganisk kemi
Demetylering hänvisar ofta till klyvning av etrar , särskilt aryletrar, även om det finns några undantag, såsom N -demetylering av aminer (t.ex. imipramin till desipramin ).
Spjälkande metyletrar
Arylmetyletrar är genomgående i lignin och många härledda föreningar. Demetyleringen av dessa material har varit föremål för mycket ansträngning. Reaktionen kräver vanligtvis hårda förhållanden eller hårda reagens. Till exempel kan metyletern i vanillin avlägsnas genom uppvärmning nära 250 °C (482 °F) med stark bas. Starkare nukleofiler såsom diorganofosfider (LiPPh 2 ) klyver också aryletrar under mildare förhållanden. Andra starka nukleofiler som har använts inkluderar tiolatsalter som EtSNa.
Sura betingelser kan också användas. Historiskt har arylmetyletrar, inklusive naturprodukter som kodein ( O -metylmorfin), demetylerats genom att värma ämnet i smält pyridinhydroklorid ( smältpunkt 144 °C (291 °F)) vid 180 till 220 °C (356 till 428 ° F), ibland med överskott av väteklorid , i en process som kallas Zeisel-Prey-eterklyvningen . Kvantitativ analys för aromatiska metyletrar kan utföras genom argentometrisk bestämning av den bildade N -metylpyridiniumkloriden . Mekanismen för denna reaktion börjar med protonöverföring från pyridiniumjon till arylmetyleter, ett mycket ogynnsamt steg ( p Ka K < 10 –11 ) som står för de svåra förhållanden som krävs, givet den mycket svagare surheten hos pyridinium ( = 5,2) ) jämfört med den protonerade arylmetyletern (en arylmetyloxoniumjon, p Ka = –6,7 för aryl = Ph). Detta följs av S N 2-angrepp av arylmetyloxoniumjonen vid metylgruppen av antingen pyridin- eller kloridjon (beroende på substratet) för att ge den fria fenolen och, slutligen, N -metylpyridiniumklorid, antingen direkt eller genom efterföljande metylöverföring från metylklorid till pyridin.
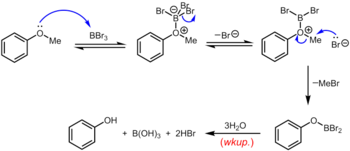
En annan klassisk (men, återigen, hård) metod för att avlägsna metylgruppen i en arylmetyleter är att värma etern till återflöde i en lösning av vätebromid eller vätejodid i ättiksyra (kokpunkt 118 °C (244 °C) F)) eller koncentrerad bromvätesyra eller jodvätesyra . Klyvningen av etrar med bromväte eller jodvätesyra fortskrider med en mycket liknande mekanism, i vilken den mycket sura HBr eller HI tjänar till att protonera etern, följt av ersättning av bromid eller jodid , som båda är utmärkta nukleofiler. En något mildare uppsättning förhållanden använder cyklohexyljodid (CyI, 10,0 ekv.) i N , N -dimetylformamid för att generera en liten mängd vätejodid in situ . Bortribromid , som kan användas vid rumstemperatur eller lägre, är ett mer specialiserat reagens för demetylering av arylmetyletrar. Mekanismen för eter-dealkylering fortskrider via den initiala reversibla bildningen av en Lewis-syra-basaddukt mellan den starkt Lewis sura BBr 3 och Lewis basiska etern. Denna Lewis-addukt kan dissociera reversibelt för att ge en dibromoboryloxoniumkatjon och Br – . Bruttning av eterbindningen sker genom den efterföljande nukleofila attacken på oxoniumarten av Br - för att ge en aryloxidibromoboran och metylbromid. Efter fullbordad reaktion frigörs fenolen tillsammans med borsyra (H3B03 ) och bromvätesyra (vattenhaltig HBr) vid hydrolys av dibromboranderivatet under vattenhaltig upparbetning .
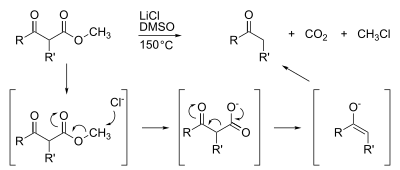
Metylestrar är också mottagliga för demetylering, vilket vanligtvis uppnås genom förtvålning . Mycket specialiserade demetyleringar är rikliga, såsom Krapcho-dekarboxyleringen :
En blandning av anetol , KOH och alkohol upphettades i en autoklav. Även om produkten av denna reaktion var den förväntade anolen , upptäcktes också en mycket reaktiv dimeriseringsprodukt i moderlutarna som kallas dianol av Charles Dodds .
N -demetylering
N -demetylering av 3°-aminer sker genom von Braun-reaktionen , som använder BrCN som reagens för att ge motsvarande nor- derivat. En modern variant av von Braun-reaktionen utvecklades, där BrCN ersattes av etylkloroformiat . Beredningen av Paxil från arecoline är en tillämpning av denna reaktion, såväl som syntesen av till exempel GSK-372,475 .
Se även
- Metylering , tillsats av en metylgrupp till ett substrat