Kaptativ effekt
Den kaptodativa effekten är stabiliseringen av radikaler genom en synergistisk effekt av en elektronbortdragande substituent och en elektrondonerande substituent. Namnet härstammar från att den elektronbortdragande gruppen (EWG) ibland kallas "fångare"-gruppen, medan den elektrondonerande gruppen (EDG) är "dativ"-substituenten. Olefiner med detta substituentmönster beskrivs ibland som kaptodativa. Radikala reaktioner spelar en integrerad roll i flera kemiska reaktioner och är också viktiga inom polymervetenskapen .
När EDG och EWG är nära det radikala centret ökar stabiliteten i det radikala centret. Substituenterna kan kinetiskt stabilisera radikalcentra genom att förhindra molekyler och andra radikalcentra från att reagera med centrum. Substituenterna stabiliserar termodynamiskt centrum genom att delokalisera radikaljonen via resonans . Dessa stabiliseringsmekanismer leder till en ökad hastighet för fria radikalreaktioner. I figuren till höger är radikalen delokaliserad mellan captornitril ( -CN) och dativ sekundär amin (-N(CH3 ) 2 ) , vilket stabiliserar radikalens centrum.
Substituteffekt på reaktionshastigheter
Vissa substituenter är bättre på att stabilisera radikala centra än andra. Detta påverkas av substituentens förmåga att delokalisera den radikala jonen i övergångstillståndsstrukturen . Delokalisering av radikaljonen stabiliserar övergångstillståndsstrukturen. Som ett resultat minskar aktiveringsenergin, vilket ökar hastigheten för den totala reaktionen. Enligt den kaptodativa effekten är reaktionshastigheten störst när både EDG och EWG kan delokalisera den radikala jonen i övergångstillståndsstrukturen.
Ito och medarbetare observerade hastigheten för additionsreaktioner av aryltiylradikal till disubstituerade olefiner. Olefinerna innehöll en EWG- nitrilgrupp och varierande EDG och effekten av varierande EDG på hastigheten för additionsreaktionerna observerades. Processen som studerades var:
Hastigheten för additionsreaktionen accelererades av följande EDGs i ökande ordning: H < CH3 < OCH2CH3 . När R = OCH 2 CH 3 är reaktionshastigheten den snabbaste eftersom reaktionen har den minsta aktiveringsenergin (ΔG ‡ ). Etoxi- och cyanogrupperna kan delokalisera radikaljonen i övergångstillståndet, vilket stabiliserar radikalcentret. Hastighetsökningen beror på den kaptodativa effekten. När R = H har reaktionen den största aktiveringsenergin eftersom radikalcentret inte stabiliseras av den kaptodativa effekten. Väteatomen kan inte delokalisera radikaljonen. Således är reaktionen långsam i förhållande till R = OCH2CH3 - fallet . När R = CH 3 är reaktionshastigheten snabbare i förhållande till när R = H eftersom metylgrupper har mer elektrondonerande förmåga. Reaktionshastigheten är dock långsammare i förhållande till när R = OCH 2 CH 3 eftersom radikaljonen inte delokaliseras över metylgruppen. Sålunda påverkar inte kaptodativ reaktionshastigheten om radikaljonen inte delokaliseras till både EWG- och EDG-substituenterna. Vart och ett av dessa fall illustreras nedan:
Används i syntes
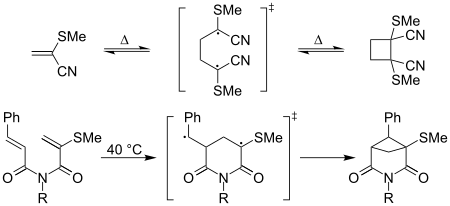
Termen "kaptodativa etener" har använts i samband med cykloadditionsreaktioner som involverar kaptodativa radikalintermediärer – till exempel sker den termiska [2+2] head-to-head dimeriseringen av 2-metyltioakrylnitril lätt vid rumstemperatur; bildningen av det ekvivalenta cyklobutanderivatet av akrylnitril är "trögt". Intramolekylära [2+2] cykliseringar har också rapporterats förstärkas av kaptodativa effekter, som visas nedan:
Liknande effekter har diskuterats för andra cykloadditioner såsom [3+2], [4+2] och [3+4] för kaptodativa etener. Effekter har också rapporterats i fall som Diels-Alder- och Friedel-Crafts- reaktioner i fall där nukleofila olefiner reagerar ineffektivt, vilket beror på att övergångstillståndet är nära en biradikal och därmed stabiliserats. Dessa studier har avslöjat ett direkt beroende av Δω, skillnad i elektrofilicitet och reaktionens polära natur. De har använts på grund av deras mycket reaktiva, stereoselektiva, regioselektiva natur inom dessa reaktioner.
Kaptodativa olefiner i reaktioner visar också störande effekter med den typiska kinetiska isotopeffekten , vilket tillåter atypiska reaktioner att inträffa med isotopmärkta molekyler och visar att mekanismerna och övergångstillstånden för dessa reaktioner har påverkats.
Polymervetenskaplig tillämpning
Friradikalpolymerisation , där radikaler är kedjebärare i processens fortplantning, stod för 40 miljarder av de 110 miljarder pund av polymerer som producerades i USA 2001. Kaptodativa olefiner har en specifik fördel av att vara känsliga för lösningsmedelseffekter utan effekten av att destabilisera radikalen. De har också visat sig genomgå sin radikala transformation spontant vilket gör att de kan vara användbara i polymerisationsmekanismer och bättre förstås genom NMR-studier . Dessutom är kaptodativa etaner initiatorer med unika egenskaper som ger högre molekylviktsfördelning och bildar segmentsampolymerer genom de kända radikalmekanismerna. Polymererna erhållna från kaptodativt substituerade utgångsmaterial uppvisar "önskvärda" egenskaper såsom optisk aktivitet, skillnader i polaritet, lösningsmedelsaffinitet, termiska och mekaniska stabiliteter.
- Polymerer med polära substituenter är kända för att ha intressanta tillämpningar inklusive inom elektriska och optiska material .
- Dessa polymerer är vanligtvis transparenta.
- Tdi (initial sönderdelning) för dessa polymerer är relativt låga jämfört med deras analoger, men har relativt sett högre Tdm ( maximal hastighet för viktändringstemperaturer). Men även om de kommer att börja smälta snabbare, kommer de att ta längre tid att helt ändra faser.
- Polymerer med utgångsmaterial med stora kaptodativa stabiliseringar kan snabbt "packa upp" till sin startmonomer vid upphettning.
-
Bifunktionella polymerer, med två olika funktionella grupper vid varje monomerenhet, bildas vanligtvis av de kaptodativa monomererna.
- Dativgrupper förändrar väsentligt lösligheten genom vätebindning i specifika bifunktionella polymerer (se figuren ovan). Emellertid har ingen tydlig korrelation utvecklats vid denna tidpunkt, eftersom inte alla kombinationer av substituenter och lösligheter har undersökts.
- Kaptodativ polymer är mycket funktionell i kelater med vissa metaller.