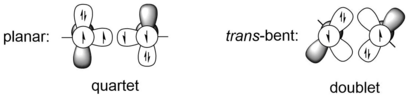Digermyne
Digermyner är en klass av föreningar som anses vara de tyngre digermaniumanalogerna av alkyner . Föräldermedlemmen i hela den här klassen är HGeGeH, som endast har karakteriserats beräkningsmässigt, men har avslöjat nyckeldrag för hela klassen. På grund av den stora interatomära repulsionen mellan två Ge-atomer kan endast kinetiskt stabiliserade digermyne-molekyler syntetiseras och karakteriseras genom att använda skrymmande skyddsgrupper och lämpliga syntetiska metoder, till exempel reduktiv koppling av germanium(II)halider.
Bindningen mellan två Ge-atomer i digermyne skiljer sig från C≡C-bindning i alkyner, vilket resulterar i digermynes trans -böjda struktur. Trans -böjd struktur är ganska vanlig i tyngre grupp 14 elementanaloger av alkyner. Den andra ordningens Jahn-Teller (SOJT) effekten av digermynes ger upphov till glidande π-bindning och stor molekylär geometrisk distorsion.
På grund av den multibundna egenskapen hos digermynes och den stora interatomära avstötningen av två Ge-atomer, vilket därför leder till det långa avståndet germanium-germanium, är digermyner mycket reaktiva och kan genomgå olika typer av reaktioner, såsom [2+1] och [2 +2] cykloadditionsreaktion med olika typer av omättade molekyler, [4+1] cykloaddition med 1,3-dimetyl-1,3-butadien, additionsreaktion av alkoholer och vatten, och fungera som π-elektrondonator för att genomgå koordinationsreaktion med silverjon.
Förberedelse
Även om många beräkningsstudier har beräknat strukturerna och energierna hos modermolekylen HGeGeH och digermynes med organiska substitut, kan de endast syntetiseras och isoleras vid skydd av skrymmande R-grupper. Det har bevisats att den syntetiska strategin att reducera korrekt prekursor, vanligtvis germanium(II)halogenider med skrymmande skyddsgrupper, med starka reduktionsmedel är kraftfull för att syntetisera digermynes.
Reduktiv koppling av germanium(II)halogenider
Den första stabila digermyne 2,6-Dipp 2 H 3 C 6 GeGeC 6 H 3 -2,6-Dipp 2 (Ar 1 GeGeAr 1 , Dipp = 2,6-diisopropylphenyl) syntetiserades och karakteriserades av Philip P. Power and co -arbetare 2002. Reduktiv koppling av skrymmande 2,6-Dipp 2 -C 6 H 3 (Ar 1 ) gruppskyddad Ge(II) monoklorid (Ge(Cl)Ar 1 ) under behandling av kalium i tetrahydrofuran (THF) eller bensen gav bildningen av Ar 1 GeGeAr 1 . Kärnstrukturen C1-Ge1-Ge2-C2 har en centrosymmetrisk trans -böjd egenskap, med C1-Ge1-Ge2-vinkeln på 128,67(8)° och ett avsevärt kort avstånd på 2,2850(6) Å mellan två Ge-atomer. Den har en bra konjugation mellan två terfenylringar och C1-Ge1-Ge2-C2 vanlig på grund av den presenterade nästan noll vridningsvinkeln (0,4°). Liknande molekyl, betecknad Ar 2 GeGeAr 2 har beräknats före karakteriseringen av Ar 1 GeGeAr 1 , med den optimerade trans -böjda kärnstrukturen skyddad av ännu mer trångt 2,6-Trip 2 C 6 H 2 (Ar 2 , Trip = 2 ,4,6-triisopropylfenyl)-grupper. Transböjningen i Ar 2 GeGeAr 2 (123,2°) är jämförbar med Ar 1 GeGeAr 1 , och Ge-Ge-avståndet på 2,277 Å skiljer sig också lite från det för Ar 1 GeGeAr 1 . Ar 2 GeGeAr 2 erhölls med användning av samma reduktionsmetod och gav en struktur liknande den beräknade och Ar 1 GeGeAr 1 .
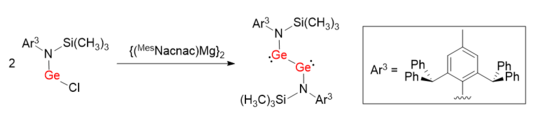
Liknande syntetisk metod användes för att underlätta syntesen av en digermyne LGeGeL med en Ge-Ge enkelbindning. Istället för att dra fördel av skrymmande ligander med kol som koordinerande atom, användes kvävebaserad skyddsgrupp L (L = N(Si(CH3) 3 ) ( Ar3 ) ) . Bindningsvinklarna för N-Ge-Ge är 100,09(6)°, vilka är mycket mer förvrängda än Ar 1 GeGeAr 1 och Ar 2 GeGeAr 2 .
Reduktion av digermylen
Steriskt trångt trans -dibromodigermylen, som skyddas av 2,6-bis[bis(trimetylsilyl)metyl]-4-[tris(trimetylsilyl)metyl]fenyl (Bbt)-grupper, kan reduceras med två ekvivalenter kaliumgrafit (KC 8 ) ) i bensen vid rumstemperatur för att föda motsvarande digermyne BbtGe≡GeBbt.
Bindning
Valensobligationsmodeller
Den mest uppenbara skillnaden mellan alkyner och digermyner, och även andra tyngre alkynanaloger, är molekylgeometrin, som är linjär i alkyner, men trans -böjd i alla tyngre alkynanaloger. Denna enorma skillnad i molekylär geometri beror på skillnaden mellan kol-kol trippelbindning och bindningen av två grupp 14 tyngre atomer, till exempel germaniumatomer. Tyngre element i grupp 14 har mycket större kovalenta radier än kol. Till exempel är enkel- och trippelbindningsradier för kol 75 Å respektive 60 Å, medan enkel- och trippelbindningsradier för germanium är 121 Å respektive 114 Å, vilka är ungefär 50 % längre. Trippelbindningssystemet REER av grupp 14-element kan ses som interaktionen mellan antingen två kvartett-ER-fragment eller två dublett-ER-fragment. Det förra fallet motsvarar den plana strukturen, medan det senare representerar den trans -böjda strukturen. Kvartettens ER-fragment har lägre energi än dubblett ett endast när E är kol, vilket vill säga för tyngre grupp 14-element, är den trans -böjda strukturen mer energiskt gynnad än plan struktur. Till exempel är HGe- och PhGe-fragment av HGeGeH och PhGeGePh 44,2 och 44,1 kcal/mol mer stabila i energi än kvartettens respektive, under beräkningsnivån B3PW91/6-311+G(2df) (för Ge), 6- 31G(d) (för C, H). Kriteriet för en trans -böjd struktur kan ges av CGMT-modellen. Därför kan bindningen mellan två Ge-atomer i digermynes beskrivas som donator-acceptor-interaktioner med valensbindningsmodeller.
Det kan ses från bindningsrepresentationerna att Ge-atomer antingen är länkade med en σ-bindning och två donator-acceptorbindningar (från en fylld sp-hybridorbital till en tom p-orbital) eller en σ-bindning och en π-bindning med en resonerande ensamma par eller två radikaler på varje Ge-atom. Enligt resonansstrukturerna har en av de två Ge-atomerna partiell positiv laddning och är elektronbrist, den andra Ge-atomen har ett ensamt elektronpar och kan donera en viss elektrontäthet.
De onormala bindningsvinklarna och enkelbindningsfunktionen hos LGeGeL kan rationaliseras av den elektrondonerande karaktären hos N-atomen, vilket leder till bildandet av N p(π)→Ge (tom p-orbital) interaktion. Därför är donator-acceptorbindningarna mellan två Ge-atomer försvagade och är mer som icke-bindande ensamma elektronpar. Det har föreslagits att bindningsordningen för Ge-Ge-bindning till viss del påverkas av de elektroniska egenskaperna hos skrymmande skyddsgrupper.
Molecular orbital (MO) behandling
I en beskrivning av molekylär orbital (MO) är den geometriska distorsionen (trans-böjda strukturen) av digermynes konsekvensen av andra ordningens Jahn-Teller (SOJT) effekt, som är den symmetri som tillåts interaktion mellan fylld bindning MO (vanligtvis HOMO i digermynes) och tomma icke-bindande eller antibindande MOs (vanligtvis den senare) som är nära i energi och kan leda till stor molekylär distorsion. Om du begränsar digermyne-molekylen i D ∞h -punktgruppen kommer två Ge-atomer att bilda en lågt liggande σ-bindande orbital, två degenererade π-bindande orbitaler och π-antibindande orbitaler, och en högt liggande σ-antibindande orbitaler, som är samma som alkyner. SOJT-blandning av in-plain π-bindande orbital (π x , HOMO) och σ-antibonding orbital, som har samma b u- symmetri i den trans -böjda C 2h -punktgruppen, ger upphov till en glidande π-bindning med signifikant icke -bundna elektronparkaraktär som har lägre energi, samt en σ-antibindande orbital med högre energi. Denna andra ordningens blandning av MO leder till den molekylära distorsionen i geometrin från linjär D ∞h till trans -böjd C 2h . Blandningen av σ-bindande orbital och in-plain π-antibindande orbital (π x * , LUMO) är också symmetriskt (båda är i b g -symmetri) och energimässigt tillåten. När man märker att stor SOJT-effekt uppstår mellan två orbitaler med en energiskillnad på 2 eV eller ännu större, till exempel 4 eV, är omfattningen av blandning av orbitaler försumbar i alkyner, men maximeras i tyngre grundämnen, som Ge-atomer i digermynes.
Reaktivitet
Cykelladdning
På grund av den multibundna egenskapen hos digermynes och den stora interatomära avstötningen av två Ge-atomer, kan digermyner genomgå cykloadditionsreaktioner med alkener och alkyner, såsom eten och acetylen.
[2+1] och [2+2] Cycladdition
Digermyner kan reagera med en mängd olika omättade små molekyler, inklusive alkyner, alkener, PhN=NPh, isocyanider och azider, på grund av deras relativt svaga Ge-Ge-bindningar. Det har bevisats att det finns två typer av reaktionssätt när BbtGeGeBbt behandlas med eten, som båda genomgår en [1+2] cykloadditionsreaktion till en början för att ge en germiransubstituerad germylenintermediär. Ge-atomen i germiran-substituenten infogas sedan lätt i en av Ge-C-bindningarna av germylen för att generera 1,2-digermacyklobuten, vilket har illustrerats både experimentellt och beräkningsmässigt. I det fall etentrycket är ca 1 atm reagerar 1,2-digermacyklobutenen vidare med en ekvivalent eten genom samma cykloadditionsreaktion för att ge en digerman med två fyrledade Ge 2 C 2-ringar , medan digermanen med två treledade GeC2- ringar erhålls med högre etentryck. Det har föreslagits att den förra är termodynamiskt stabil produkt, medan den senare endast är kinetiskt stabil.
På liknande sätt äger [2+2] cykloadditionsreaktioner rum mellan digermyner och alkyner, till exempel PhC≡CPh, vilket leder till bildningen av 1,2-digermacyklobutadien.
[4+1] Cycladdition: digermynes diradisk karaktär
Till skillnad från alkyner som genomgår [4+2] cykloadditionsreaktion med 2,3-dimetyl-1,3-butadien för att ge 1,4-cyklohexadienderivat, genomgår digermyner [4+1] cykloadditionsreaktion på grund av närvaron av det ytterst reaktiva diradikal karaktär, vilket kan ses i valensorbitalmodeller. I fallet med Ar 2 GeGeAr 2 reagerar den med 2,3-dimetyl-1,3-butadien för att ge ett ovanligt germant derivat. Reaktionen börjar mellan varje radikalcentrum och 2,3-dimetyl-1,3-butadien först, vilket ger upphov till bildandet av digerman med två germacyklopent-3-enringar genom [4+1] cykloaddition. Den ökade steriska repulsionen av två GeC 4 -ringar leder till homolytisk klyvning av Ge-Ge-singelbindningen som sedan producerar den slutliga germanen genom 1,4-additionsreaktion med ytterligare ekvivalent av 2,3-dimetyl-1,3-butadien . Brytningen av Ge-Ge-bindningen ses inte när BbtGeGeBbt reagerar med 2,3-dimetyl-1,3-butadien, vilket endast ger upphov till digerman.
Additionsreaktion av alkoholer och vatten: multipelbindningskaraktär hos digermynes
BbtGeGeBbt har visat sig kunna genomgå additionsreaktion med alkoholer som metanol och vatten för att generera 1,1-dimethoxydigermane respektive 1,1-dihydroxydigermane, som visar digermynes multipelbindningskaraktär.
Koordinationsreaktion
Genom att notera att den a u (π) bindande orbitalen i digermynes har förmågan att fungera som π-elektrondonator, kan Ar 1 GeGeAr 1 reagera med AgSbF 6 för att bilda [AgAr 1 GeGeAr 1 ] + SbF 6 − vid -40 °C . [AgAr 1 GeGeAr 1 ] + har en C 2 -axel genom silveratomen som är vinkelrät mot CGeGeC-slätten och Ge-Ge-bindningens mittpunkt. Silveratomen koordineras av två Ge-atomer och två arener från Dipp-grupper i de skrymmande skyddsgrupperna. Bindningen mellan GeGe-delen och Ag + domineras av interaktionen mellan HOMO för Ar 1 GeGeAr 1 och 5s och 5p-orbitaler för Ag + , som gör anspråk på σ-karaktären för interaktionen, medan π-karaktären kan förklaras av relativ svag interaktion av Ag 4d xz orbital med π* orbital (LUMO+1). Därför har det föreslagits att [AgAr 1 GeGeAr 1 ] + är en hybrid av π-komplex och ett metallacyklopropenliknande σ-komplex.
Se även
- ^ Power, Philip P. (2010-01-14). "Huvudgruppselement som övergångsmetaller". Naturen . 463 (7278): 171–177. doi : 10.1038/nature08634 . ISSN 1476-4687 . PMID 20075912 . S2CID 205219269 .
- ^ Grev, Roger S.; Deleeuw, Bradley J.; Schaefer, Henry F. (1990-01-12). "Germanium-germanium multipelbindningar: Singlet elektroniska jordtillståndet för Ge2H2". Bokstäver i kemisk fysik . 165 (2): 257–264. doi : 10.1016/0009-2614(90)85439-J .
- ^ Grev, Roger S. (1991-01-01). Sten, FGA; West, Robert (red.). Framsteg inom metallorganisk kemi . Vol. 33. Akademisk press. s. 125–170. doi : 10.1016/S0065-3055(08)60695-4 . ISBN 9780120311330 .
- ^ a b Takagi, Nozomi; Nagase, Shigeru (2001-12-01). "Substituenteffekter på Germanium-Germanium och Tin-Tin Trippelbindningar". Organometalliska ämnen . 20 (26): 5498–5500. doi : 10.1021/om010669u . ISSN 0276-7333 .
- ^ Stender, Matthias; Phillips, Andrew D.; Wright, Robert J.; Power, Philip P. (2002-05-17). "Syntes och karakterisering av en digermaniumanalog av en alkyn". Angewandte Chemie International Edition . 41 (10): 1785–1787. doi : 10.1002/1521-3773(20020517)41:10<1785::AID-ANIE1785>3.0.CO;2-6 . PMID 19750717 .
- ^ a b Stender, Matthias; Phillips, Andrew D.; Power, Philip P. (2002-05-30). "Bildning av [Ar*Ge{CH2C(Me)C(Me)CH2}CH2C(Me)]2 (Ar* = C6H3-2,6-Trip2; Trip = C6H2-2,4,6-i-Pr3) via reaktion av Ar*GeGeAr* med 2,3-dimetyl-1,3-butadien: bevis för existensen av en germaniumanalog av en alkyn". Chemical Communications (12): 1312–1313. doi : 10.1039/B203403D . ISSN 1364-548X . PMID 12116985 .
- ^ Li, Jiaye; Schenk, Christian; Goedecke, Catharina; Frenking, Gernot; Jones, Cameron (2011-11-23). "En Digermyne med en Ge-Ge Single Bond som aktiverar dihydrogen i fast tillstånd". Journal of the American Chemical Society . 133 (46): 18622–18625. doi : 10.1021/ja209215a . ISSN 0002-7863 . PMID 22026634 .
- ^ a b c d Sugiyama, Yusuke; Sasamori, Takahiro; Hosoi, Yoshinobu; Furukawa, Yukio; Takagi, Nozomi; Nagase, Shigeru; Tokitoh, Norihiro (2006-01-01). "Syntes och egenskaper hos en ny kinetiskt stabiliserad Digermyne: Nya insikter för en Germaniumanalog av en alkyn". Journal of the American Chemical Society . 128 (3): 1023–1031. doi : 10.1021/ja057205y . ISSN 0002-7863 . PMID 16417395 .
- ^ Pyykkö, Pekka; Atsumi, Michiko (2009-11-23). "Molekylära dubbelbindande kovalenta radier för element Li–E112". Kemi – En europeisk tidskrift . 15 (46): 12770–12779. doi : 10.1002/chem.200901472 . ISSN 1521-3765 . PMID 19856342 .
- ^ Kobayashi, Kaoru; Nagase, Shigeru (1997-06-01). "Silicon−Silicon Triple Bonds: Gör substituenter Disilynes syntetiskt tillgängliga?". Organometallics . 16 (12): 2489–2491. doi : 10.1021/om970232f . ISSN 0276-7333 .
- ^ Driess, Matthias; Grützmacher, Hansjörg (1996-05-03). "Huvudgruppselementanaloger av karbener, olefiner och små ringar". Angewandte Chemie International Edition på engelska . 35 (8): 828–856. doi : 10.1002/anie.199608281 . ISSN 1521-3773 .
- ^ Pearson, Ralph G. (1975-06-01). "Angående Jahn-Teller-effekter" . Proceedings of the National Academy of Sciences . 72 (6): 2104–2106. doi : 10.1073/pnas.72.6.2104 . ISSN 0027-8424 . PMC 432704 . PMID 16592247 .
- ^ a b Sasamori, Takahiro; Sugahara, Tomohiro; Agou, Tomohiro; Sugamata, Koh; Guo, Jing-Dong; Nagase, Shigeru; Tokitoh, Norihiro (2015-09-14). "Reaktion av en diaryldigermyne med etylen" . Kemisk vetenskap . 6 (10): 5526–5530. doi : 10.1039/c5sc01266j . ISSN 2041-6539 . PMC 5510527 . PMID 28757948 .
- ^ Huo, Suhong; Li, Xiaoyan; Zeng, Yanli; Zheng, Shijun; Meng, Lingpeng (2013-09-01). "Reaktionsmekanism för CH3M≡MCH3 (M=C, Si, Ge) med C2H4: [2+1] eller [2+2] cykloaddition?". Journal of Molecular Modeling . 19 (9): 3501–3506. doi : 10.1007/s00894-013-1882-0 . ISSN 1610-2940 . PMID 23708650 . S2CID 43101037 .
- ^ a b Power, Philip P. (2005-04-01). "Syntes och några reaktivitetsstudier av germanium, tenn och blyanaloger av alkyner". Tillämpad organometallisk kemi . 19 (4): 488–493. doi : 10.1002/aoc.824 . ISSN 1099-0739 .
- ^ Wang, Xinping; Peng, Yang; Olmstead, Marilyn M.; Hope, Håkon; Power, Philip P. (2010-09-29). "En Ditetrylyne som en π-elektrondonator: syntes och karakterisering av [AgAr′GeGeAr′]+SbF6− och [Ag2Ar′GeGe(F)Ar′]+SbF6− (Ar′ = C6H3-2,6(C6H3-2) ,6-Pri2)2)". Journal of the American Chemical Society . 132 (38): 13150–13151. doi : 10.1021/ja1051236 . ISSN 0002-7863 . PMID 20809567 .