Dekarboxylativ korskoppling
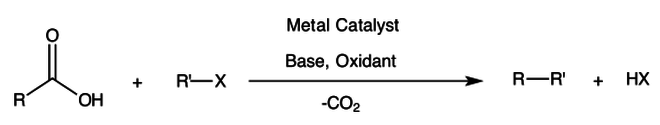
Dekarboxylativa korskopplingsreaktioner är kemiska reaktioner där en karboxylsyra reageras med en organisk halogenid för att bilda en ny kol-kolbindning, samtidigt med förlust av CO 2 . Aryl- och alkylhalider deltar. Metallkatalysator , bas och oxidationsmedel krävs .
En betydande fördel med denna reaktion är att den använder relativt billiga karboxylsyror (eller deras salter) och är mycket mindre luft- och fuktkänsliga i jämförelse med typiska korskopplingsorganometalliska reagenser . Dessutom karboxylsyradelen ett vanligt inslag i naturliga produkter och kan också framställas genom relativt godartade luftoxidationer . Ytterligare fördelar inkluderar den breda toleransen av funktionella grupper , såväl som förmågan att undvika användningen av starka baser . Ett viktigt elementärt steg i denna reaktion är protodekarboxylering eller metallering för att först omvandla C-COOH-bindningen till en C-H- respektive C-M-bindning.
Historia och katalysatorutveckling
Kopparmonometalliska system
Den första rapporterade dekarboxylativa korskopplingsreaktionen var en Ullmann-reaktion , 1966 av Nilsson et al. Termisk dekarboxylering av kopparbensoater, i närvaro av en arylhalogenid , visade sig producera (både symmetriska och osymmetriska) biaryler genom aryl-Cu-mellanprodukter.
Detta monometalliska kopparsystem krävde drastiska förhållanden för fullständig korskoppling och hade olika inneboende begränsningar, som båda förhindrade utvecklingen av en katalytisk , förberedande version av denna reaktion. Det var inte förrän 2009 som Liu och Shang et al. fann att dekarboxylativ korskoppling av arylbromider och jodider med kaliumpolyfluorbensoater kunde uppnås med användning av monometallisk kopparjodid som katalysator. Det oxidativa tillsatssteget bestämdes vara det hastighetsbegränsande steget i katalysatorcykeln med endast koppar (en kontrast till Pd-katalyserad dekarboxylativ korskoppling) .
Cu(I)-system har också visat sig främja koppling av alkynylkarboxylsyror med arylhalider (se arylalkyner nedan), såväl som dekarboxylativ dehydrogenativ korskoppling av aminosyror med alkyner (eller liknande nukleofiler ).
Katalysatorer för dekarboxylativ korskoppling är av den allmänna formen ML2, med en mängd olika ligandtyper optimerade för olika substrat. Koppar (och silver ) centra är ofta komplexbundna med fenantroliner , och aktiviteten rapporteras öka med elektronrika substituenter på liganderna.
Palladium monometalliska system
År 2000, Steglich et al. rapporterade en intramolekylär Pd(II)-medierad dekarboxylativ korskopplingsreaktion i deras syntes av lamellarin L. Myers et al. rapporterade dekarboxylativ olefinering av orto -substituerade arenkarboxylater i närvaro av en oxidant (Ag2CO3) 2002.
Efterföljande studier visade att homogena Pd-katalysatorer kunde dekarboxylera syror vid lägre temperaturer än deras Cu- och Ag-motsvarigheter, men var begränsade till elektronrika orto -substituerade aromatiska karboxylsyror. Trots detta kan palladiumkatalysatorer främja en mängd olika korskopplingsreaktioner inklusive biarylbildning och arylalkynbildning, tillsammans med en mängd korskopplingsreaktioner där karboxylsyran inte är bunden till en aromatisk förening. Andra Pd-katalyserade dekarboxylerings-korskopplingsreaktioner inkluderar konjugerad dienberedning (se diener och triener nedan) och dehydrogenativa reaktioner (med en mängd olika substrat- och katalysatorkombinationer ).
I motsats till Cu-only- system är dekarboxylativ palladering det hastighetsbegränsande steget i den katalytiska palladiumcykeln.
Palladium-–koppar bimetallsystem
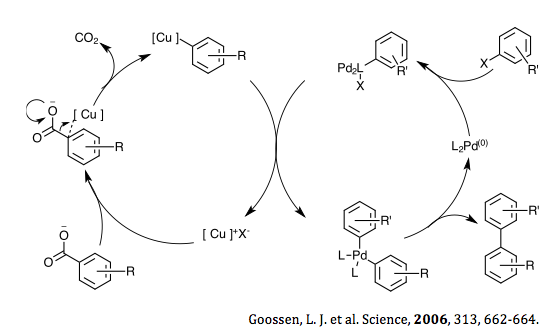
Ett Pd-Cu bimetallsystem upptäcktes inte förrän 2006 när Goossen et al. rapporterade en dekarboxylativ korskoppling av arylhalider med orto -substituerade aromatiska karboxylsyror. Genom efterföljande studier visade det sig att användningen av aryltriflater gjorde det möjligt att utöka substratets utrymme för korskoppling till vissa aromatiska karboxylater som saknade orto -substitution (mindre reaktiva). Detta var ett resultat av det faktum att eventuell halidanjon som genererades i reaktionen hämmade den Cu-katalyserade dekarboxyleringsprocessen. Ytterligare optimering av systemet och katalysatorförhållandena har gjort dekarboxylativ korskoppling med hjälp av bimetalliska Pd-Cu-system tillämpliga på organisk syntes, mest övervägande vid bildning av biaryler. Variabiliteten hos detta kombinerade katalytiska system möjliggör också främjande av ett stort spektrum av reaktioner, inklusive arylketonbildning, c-heteroatom-korskoppling och många andra.
Palladium-silver bimetallsystem
Silver är i samma grupp som koppar, Pd-Ag(I) bimetalliska system liknar till sin natur Pd-Cu katalytiska system. Silversalter är dock bättre lämpade för protodekarboxylering av karboxylsyror än deras kopparekvivalenter, vilket tillåter mildare reaktionsförhållanden i Pd-Ag-cykler i förhållande till Pd-Cu-cykler. Ag(I)-katalyserade monometalliska system har också rapporterats. Deras skicklighet (i förhållande till koppar ) tillskrivs sannolikt lägre elektronegativitet och större expansion av d-orbitaler , vilket främjar dekarboxylering av substratet. En begränsning av denna katalysatorkombination är att silversalterna kommer att bilda olösliga silverhalider, vilket tvingar reaktionen att kräva en stökiometrisk mängd Ag om halogenider är närvarande. Detta hinder övervanns av Goossen et al. 2010 genom att använda aryltriflater , och katalytisk reaktion med arylsulfonater har också rapporterats.
Produktomfattning via variation av substrat
Produktomfånget för denna reaktion är extremt brett med användning av olika substrat; emellertid har utvecklingen av olika funktionaliteter krävt åtföljande studier för att bestämma det rätta katalysatorsystemet. Den mest typiska klassen av reaktioner involverar koppling mellan C–COOH och C–X bindningar, men C–COOH och C–M korskoppling, homokoppling av karboxylsyror, heck koppling och dehydrogenativ korskoppling kan också inkluderas i denna klass när de släpper ut CO 2 . Heteroatomkorskopplingsreaktioner som involverar bildning av C-N-, C-S-, C-P- och C-X-bindningar har också visats.
Biarylbildning
Per IUPAC hänvisar termen biaryl till en sammansättning av två aromatiska ringar förenade med en enkelbindning, som börjar med den enklaste, bifenyl . Biaryler utgör ett viktigt strukturellt motiv av fysiskt organiskt, syntetiskt och katalytiskt intresse - till exempel bakom området för atropisomerer i enantioselektiv syntes - och de förekommer i många farmaceutiska, agrokemiska och materialtillämpningar (t.ex. LCD). omvandling ; Exemplet på en kopplingsreaktionsreaktion som används i deras framställning är ett alternativ till de traditionella Suzuki- och Stille-korskopplingsreaktionerna, och olika katalysatorer har använts för denna Goossen et al. rapporterade bildandet av biaryler från palladium- och kopparkatalyserade korskopplingsreaktioner av en aryl- eller heteroarylkarboxylsyra och en arylhalogenid (I, Br eller Cl) i närvaro av en bas.
Arylalkyner
Arylalkyner tillverkas vanligtvis med användning av Sonogashira-reaktionen som är den palladiumkatalyserade korskopplingsreaktionen av terminala alkyner och arylhalider. Istället för de terminala alkynerna har alkynkarboxylsyror fördelar, enkel hantering och lagring. Den första dekarboxylativa kopplingen av alkynkarboxylsyror rapporterades 2008 av S. Lee. De använde propiolsyra som en alkynkälla. Ett år senare tillämpade S. Lee de dekarboxylativa kopplingsreaktionerna mot 2-oktynsyra och fenylpropiolsyra. År 2010, Xue et al. rapporterade kopplingen av en arylhalogenid och alkynylkarboxylsyra under milda reaktionsförhållanden och en endast kopparkatalysator för att erhålla arylalkyner.
Arylketoner
Ytterligare arbete av Goossen et al. beskrev syntesen av ketoner från a-oxokarboxylsyror med aryl- eller heteroarylbromider genom en acylanjonmellanprodukt.
Arylestrar
Shang et al. upptäckte den dekarboxylativa kopplingen av kaliumoxalatmonoestrar med arylhalider för att erhålla aryl- eller alkenylestrar.
sp 3 C karboxylsyror
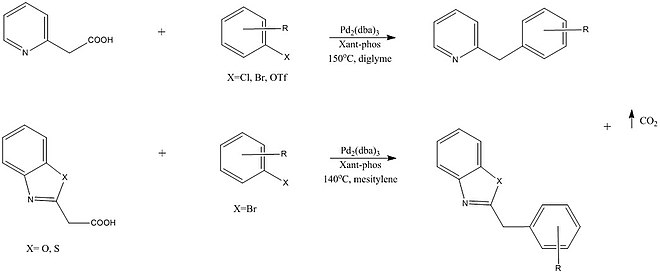
Många dekarboxylativa korskopplingsreaktioner involverar brytning av sp 2 C-COOH- och sp C-COOH-bindningar, därför har efterföljande studier försökt möjliggöra korskoppling med sp 3 C-karboxylsyror. En sådan reaktion av Shang et al. beskrev en palladiumkatalyserad korskoppling som möjliggör bildning av funktionaliserade pyridiner, pyraziner, kinoliner, bensotiazoler och bensoxazoler. Positionen för kväveatomen i "2"-positionen i förhållande till kopplingen har visat sig vara nödvändig, vilket innebär att dess bindning till Pd i ett övergångstillstånd.
Dienes och triener
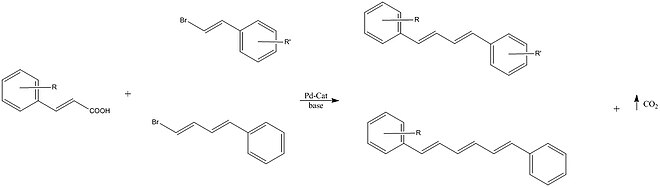
Miura et al. rapporterade korskopplingen av vinylbromider med en alkenylkarboxylsyra med användning av en palladiumkatalysator. Vissa av de framställda konjugerade dienerna rapporterades uppvisa fluorescens i fast tillstånd.
Olefiner via Heck-typ
En dekarboxylativ Heck-koppling av Su et al. kan användas för att erhålla en arylolefin med användning av bensokinon som oxidant.
Fenantrenderivat
Wang et al. föreslog en ny metod för [4+2] annullering via en palladiumkatalyserad intermolekylär väg. Derivat bildas i måttlig till god avkastning; akridin är avgörande för hög reaktionseffektivitet.
C–N-koppling
Jiao et al. möjliggjorde bildandet av en C-N-bindning via korskoppling med luft som oxidationsmedel och en kopparkatalysator. Inga förhållanden är kända för en C–N-korskoppling som bryter en sp 3 eller sp 2 C–COOH-bindning.
CS koppling
Liu et al. rapporterade CS-kopplingen av arylkarboxylsyror med disulfider eller tioler med användning av ett Pd/Cu-katalysatorsystem.
C–P-koppling
Använda antingen Pd-Cu eller Cu katalysatorer Yang et al. rapporterade det första exemplet på dekarboxylativ C–P-korskoppling.
C–X-koppling
Wu et al. rapporterade en C–X-korskoppling med CuX 2 (X= Br, Cl) och en silverkatalysator för att erhålla arylhalider.
Mekanistiska studier
Dekarboxylativ Heck typ
År 2005, Meyers et al. Föreslog följande mekanism för den dekarboxylativa korskopplingsreaktionen. Det initiala och hastighetsbestämmande steget är dekarboxyleringen. Ipso-kolet i arenringen tros koordinera till palladiumcentret initialt och följs av utdrivningen av koldioxid, vilket bildar en aryl-palladium-mellanprodukt. Olefinen sätts sedan in mellan aren och palladiumcentrum, som sedan genomgår beta-eliminering för att bilda den önskade vinylhalogeniden, såväl som en palladiumhydrid. Denna proton abstraheras av silverkarbonat, som fungerar som både en bas och en oxidant för att regenerera utgångspalladiumkomplexet som fullbordar den katalytiska cykeln.
Biarylsyntes via redoxneutral dekarboxylativ korskoppling
År 2006 gjorde Goossen et al. föreslog en reaktion för att syntetisera biarylföreningar via katalytisk dekarboxylativ korskoppling. Mekanismen involverar två överlappande cykler, en använder en kopparhalogenid och den andra använder palladium. Dekarboxyleringssteget sker mellan den substituerade bensoesyran och kopparhalogeniden för att bilda den intermediära arylkoppartypen. Palladiumet genomgår initialt oxidativ tillsats från arylhalogeniden för att bilda ett Pd(II)-arylkomplex. Efter båda dessa initiala steg genomgår den substituerade arylkopparn transmetallering med palladiumkomplexet. Detta steg bildar kopparhalogeniden, som sedan genomgår anjonutbyte med den substituerade bensoesyran för att reformera arylkopparmellanprodukten och fortsätta den katalytiska cykeln. Det andra komplexet som bildas i trans-metalleringssteget är ett bis-aryl-palladium(II), som sedan genomgår reduktiv eliminering för att bilda den önskade bis-aryl-arten såväl som utgångs-Pd(0)-komplexet, och därmed fullborda den katalytiska cykeln.
Heteroaromatisk syrakoppling
Forgione, P., Bilodeau, F. et al. rapporterade att heteroatomer innehållande en karboxylsyra också tolereras av palladiummonometalliska system och genomgår dekarboxylativ korskoppling med arylhalogenider. I den föreslagna mekanismen är det första steget oxidativ tillsats av arylhalogeniden som bildar en aryl-palladium-mellanprodukt. Elektrofil palladation sker sedan vid kol-3 i heteroatomen. Från denna intermediär finns det två möjliga vägar för cykeln att fortsätta på. Den första är palladiummigrering från kol-3 till kol-2 tillsammans med utdrivningen av koldioxid. Detta bildar aryl-palladium-heteroatom-mellanprodukten, som genomgår reduktiv eliminering för att bilda den slutliga heteroaromatiska föreningen. Den andra vägen uppstår endast när R är en proton. Om så är fallet sker deprotonering för att återvinna aromaticiteten hos heteroatomen. Denna mellanprodukt genomgår sedan reduktiv eliminering, vilket kopplar aryl till kol-3-positionen i heteroatomen. Eftersom denna förening fortfarande innehåller karboxylsyran är den sedan fri att återinträda i den katalytiska cykeln där den genomgår koppling vid kol 2-positionen, tillsammans med utdrivningen av koldioxid för att bilda en biarylheteroatom. Eftersom denna väg konkurrerar med dekarboxyleringssteget, bildas två produkter som gör denna reaktion mindre selektiv. Som ett resultat, heteroatomer, som är substituerade i kol 3-positionen och är mer gynnade på grund av den högre nivån av kontroll de ger.