Vattenklyvning
Vattenspjälkning är den kemiska reaktionen där vatten bryts ner till syre och väte :
- 2H2O → 2H2 + O2 _
Effektiv och ekonomisk vattenklyvning skulle vara ett tekniskt genombrott som skulle kunna underbygga en väteekonomi baserad på grönt väte . En version av vattenklyvning sker i fotosyntesen , men väte produceras inte. Det omvända till vattendelning är grunden för vätebränslecellen .
Elektrolys
Elektrolys av vatten är sönderdelning av vatten (H 2 O) till syre (O 2 ) och väte (H 2 ) på grund av att en elektrisk ström passerar genom vattnet.
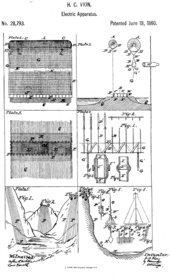 Atmosfäriskt elutnyttjande för den kemiska reaktionen där vatten separeras i syre och väte. (Bild via: Vion, US-patent 28793. juni 1860.)
Atmosfäriskt elutnyttjande för den kemiska reaktionen där vatten separeras i syre och väte. (Bild via: Vion, US-patent 28793. juni 1860.)
- Vion, US-patent 28 793 , "Förbättrad metod för att använda atmosfärisk elektricitet", juni 1860.
I kraft-till-gas- produktionsscheman används överskottseffekten eller lågeffekt som skapas av vindgeneratorer eller solpaneler för lastbalansering av energinätet genom att lagra och senare injicera vätgas i naturgasnätet.

Produktion av väte från vatten är energikrävande. Potentiella elektriska energiförsörjningar inkluderar vattenkraft, vindkraftverk eller solceller. Vanligtvis är den elektricitet som förbrukas mer värdefull än det väte som produceras, så denna metod har inte använts i stor utsträckning. I motsats till lågtemperaturelektrolys, högtemperaturelektrolys (HTE) av vatten mer av den initiala värmeenergin till kemisk energi (väte), vilket potentiellt fördubblar effektiviteten till cirka 50 %. Eftersom en del av energin i HTE tillförs i form av värme, måste mindre av energin omvandlas två gånger (från värme till elektricitet och sedan till kemisk form ), och så blir processen mer effektiv. [ citat behövs ]
För närvarande är energieffektiviteten för elektrolytisk vattendelning 60 % - 70 %.
Vatten spricker i fotosyntesen
En version av vattendelning sker i fotosyntesen , men elektronerna shuntas, inte till protoner, utan till elektrontransportkedjan i fotosystem II . Elektronerna används för att omvandla koldioxid till sockerarter.
När fotosystem I blir fotoexciterad, initieras elektronöverföringsreaktioner, vilket resulterar i reduktion av en serie elektronacceptorer, vilket så småningom reducerar NADP + till NADPH och PS I oxideras. Det oxiderade fotosystemet I fångar elektroner från fotosystem II genom en serie steg som involverar ämnen som plastokinon, cytokromer och plastocyanin. Fotosystemet II åstadkommer sedan vattenoxidation vilket resulterar i utveckling av syre, reaktionen katalyseras av CaMn 4 O 5 -kluster inbäddade i komplex proteinmiljö; komplexet är känt som oxygen evolving complex (OEC).

Vid biologisk väteproduktion shuntas elektronerna som produceras av fotosystemet inte till en kemisk syntesapparat utan till hydrogenaser , vilket resulterar i bildning av H 2 . Detta bioväte produceras i en bioreaktor .
Fotoelektrokemisk vattenklyvning
Att använda el som produceras av solcellssystem erbjuder potentiellt det renaste sättet att producera väte, annat än kärnkraft, vindkraft, geotermisk energi och vattenkraft. Återigen bryts vatten ner till väte och syre genom elektrolys, men den elektriska energin erhålls genom en fotoelektrokemisk cell (PEC) process. Systemet kallas också för artificiell fotosyntes .
Fotokatalytisk vattenklyvning
Omvandlingen av solenergi till väte med hjälp av vattenklyvningsprocess är ett sätt att uppnå ren och förnybar energi. Denna process kan bli effektivare om den assisteras av fotokatalysatorer suspenderade direkt i vatten snarare än ett solcells- eller elektrolytiskt system, så att reaktionen sker i ett steg.
Radiolys
Kärnstrålning bryter rutinmässigt vattenbindningar, i Mponeng -guldgruvan , Sydafrika , hittade forskare i en naturligt hög strålningszon , ett samhälle som domineras av en ny fylotyp av Desulfotomaculum , som livnär sig på i första hand radiolytiskt producerad H 2 . Använt kärnbränsle utreds också som en potentiell vätekälla. [ citat behövs ]
Nanogalvaniskt pulver av aluminiumlegering
Ett aluminiumlegeringspulver som uppfanns av US Army Research Laboratory 2017 visade sig kunna producera vätgas vid kontakt med vatten eller någon vätska som innehåller vatten på grund av dess unika galvaniska mikrostruktur i nanoskala. Den genererar enligt uppgift väte till 100 procent av det teoretiska utbytet utan behov av några katalysatorer, kemikalier eller externt tillförd kraft.

Termisk nedbrytning av vatten
Vid termolys splittras vattenmolekyler i sina atomkomponenter väte och syre . Till exempel, vid 2200 °C är cirka tre procent av all H2O dissocierad i olika kombinationer av väte- och syreatomer, mestadels H, H2, O , O2 och OH. Andra reaktionsprodukter som H 2 O 2 eller HO 2 förblir mindre. Vid den mycket höga temperaturen på 3000 °C bryts mer än hälften av vattenmolekylerna ned, men vid omgivningstemperaturer dissocierar bara en molekyl på 100 biljoner av värmeeffekten. De höga temperaturerna och materialbegränsningarna har begränsat tillämpningarna av detta tillvägagångssätt.
Nukleär-termisk
En sidofördel med en kärnreaktor som producerar både el och väte är att den kan flytta produktionen mellan de två. Till exempel kan anläggningen producera el på dagen och väte på natten, vilket matchar sin elproduktionsprofil med den dagliga variationen i efterfrågan. Om vätgas kan produceras ekonomiskt, skulle detta system konkurrera gynnsamt med befintliga system för energilagring i nätet . Dessutom finns det tillräcklig efterfrågan på väte i USA för att all daglig toppproduktion skulle kunna hanteras av sådana anläggningar.
Den termoelektriska hybridcykeln av koppar-klor är ett kraftvärmesystem som använder spillvärme från kärnreaktorer, närmare bestämt den superkritiska vattenreaktorn CANDU .
Solvärme
De höga temperaturer som krävs för att dela vatten kan uppnås genom användning av koncentrerad solenergi . Hydrosol-2 är en pilotanläggning på 100 kilowatt vid Plataforma Solar de Almería i Spanien som använder solljus för att erhålla de nödvändiga 800 till 1 200 °C för att klyva vatten. Hydrosol II har varit i drift sedan 2008. Designen av denna 100 kilowatts pilotanläggning är baserad på ett modulärt koncept. Som ett resultat kan det vara möjligt att denna teknik lätt kan skalas upp till megawatts räckvidd genom att multiplicera de tillgängliga reaktorenheterna och genom att ansluta anläggningen till heliostatfält ( fält med solföljande speglar) av lämplig storlek.
Materialbegränsningar på grund av de erforderliga höga temperaturerna reduceras genom utformningen av en membranreaktor med samtidig extraktion av väte och syre som utnyttjar en definierad termisk gradient och snabb diffusion av väte. Med koncentrerat solljus som värmekälla och endast vatten i reaktionskammaren är de producerade gaserna mycket rena och den enda möjliga föroreningen är vatten. En "Solar Water Cracker" med en koncentrator på cirka 100 m² kan producera nästan ett kilo väte per soltimme.
Forskning
Forskning bedrivs kring fotokatalys , accelerationen av en fotoreaktion i närvaro av en katalysator. Dess förståelse har gjorts möjlig ända sedan upptäckten av vattenelektrolys med hjälp av titandioxid. Artificiell fotosyntes är ett forskningsfält som försöker replikera den naturliga processen med fotosyntes och omvandla solljus, vatten och koldioxid till kolhydrater och syre. På senare tid har detta varit framgångsrikt i att dela upp vatten till väte och syre med hjälp av en konstgjord förening som heter Nafion .
Högtemperaturelektrolys (även HTE eller ångelektrolys ) är en metod som för närvarande undersöks för framställning av väte ur vatten med syre som biprodukt. Annan forskning inkluderar termolys på defekta kolsubstrat , vilket gör det möjligt att producera väte vid temperaturer strax under 1000 °C.
Järnoxidcykeln är en serie termokemiska processer som används för att producera väte . Järnoxidcykeln består av två kemiska reaktioner vars nettoreaktant är vatten och vars nettoprodukter är väte och syre . Alla andra kemikalier återvinns. Järnoxidprocessen kräver en effektiv värmekälla.
Svavel -jod-cykeln (SI-cykeln) är en serie termokemiska processer som används för att producera väte . SI-cykeln består av tre kemiska reaktioner vars nettoreaktant är vatten och vars nettoprodukter är väte och syre . Alla andra kemikalier återvinns. SI-processen kräver en effektiv värmekälla.
Mer än 352 termokemiska cykler har beskrivits för vattendelning eller termolys . Dessa cykler lovar att producera vätesyre från vatten och värme utan att använda elektricitet. Eftersom all ingående energi för sådana processer är värme, kan de vara effektivare än högtemperaturelektrolys. Det beror på att effektiviteten i elproduktionen i sig är begränsad. Termokemisk produktion av väte med kemisk energi från kol eller naturgas övervägs i allmänhet inte, eftersom den direkta kemiska vägen är mer effektiv.
För alla termokemiska processer är den sammanfattande reaktionen den för nedbrytning av vatten:
Alla andra reagenser återvinns. Ingen av de termokemiska väteproduktionsprocesserna har visats på produktionsnivåer, även om flera har visats i laboratorier.
Det finns också forskning om nanopartiklars och katalysatorers livsduglighet för att sänka temperaturen vid vilken vatten delar sig.
Nyligen har Metal-Organic Framework (MOF)-baserade material visat sig vara en mycket lovande kandidat för vattenklyvning med billiga, första radens övergångsmetaller .
Forskningen är koncentrerad till följande cykler:
| Termokemisk cykel | LHV Verkningsgrad | Temperatur (°C/F) |
|---|---|---|
| ( IV) oxid -cerium(III)oxidcykel ( CeO2 / Ce2O3 ) | ? % | 2 000 °C (3 630 °F) |
| Hybrid svavelcykel (HyS) | 43 % | 900 °C (1 650 °F) |
| Svaveljodcykel (SI-cykel) | 38 % | 900 °C (1 650 °F) |
| Kadmiumsulfatcykel | 46 % | 1 000 °C (1 830 °F) |
| Bariumsulfatcykel | 39 % | 1 000 °C (1 830 °F) |
| Mangansulfatcykel | 35 % | 1 100 °C (2 010 °F) |
| Zink-zinkoxidcykel (Zn/ZnO) | 44 % | 1 900 °C (3 450 °F) |
| Hybrid kadmiumcykel | 42 % | 1 600 °C (2 910 °F) |
| Kadmiumkarbonatcykel | 43 % | 1 600 °C (2 910 °F) |
| Järnoxidcykel ( ) | 42 % | 2 200 °C (3 990 °F) |
| Natrium mangan cykel | 49 % | 1 560 °C (2 840 °F) |
| Nickel mangan ferrit cykel | 43 % | 1 800 °C (3 270 °F) |
| Zink mangan ferrit cykel | 43 % | 1 800 °C (3 270 °F) |
| Koppar-klor cykel (Cu-Cl) | 41 % | 550 °C (1 022 °F) |



![{\displaystyle {\ce {2H2O <=>[{\ce {Heat}}] 2H2{}+ O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f87596dad9be266529ce624d24d420a7c5529226)
