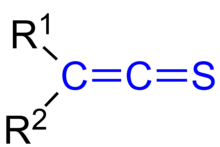Tioketen
Inom organisk kemi är tioketener organiska svavelföreningar analoga med ketener med den allmänna formeln R2C . C=S = , där R är alkyl eller aryl Modertioketenet (etention) har formeln CH2 = C=S . Det är det enklaste tioketenet. Tioketen är stabil som en gas, men som de flesta tioketener polymeriserar det vid kondensation.
Vissa tioketener produceras som övergående arter vid pyrolys av 1,2,3-tiadiazoler .
Isolerbara tioketener
Tioketener kan stabiliseras genom antingen steriskt skydd eller genom elektroniska effekter. Sålunda är di-tert-butyltioketen lätt isolerad och luftstabil. Flera exempel har karakteriserats av röntgenkristallografi . C=S-avståndet är 157 pm och C=C-avståndet är 124 pm, båda bindningarna är lämpliga för C=C=S-uppgiften. Den violetta färgen som är karakteristisk för tioketener indikerar det lilla HOMO-LUMO-gapet . Dessa föreningar framställs genom behandling av syrakloriden med fosforpentasulfid såsom beskrivs av följande idealiserade ekvation:
Bis(trifluormetyl)tioketen ( (CF3 ) 2C = C=S ) är ett exempel på en elektroniskt stabiliserad tioketen.
Reaktioner
Tioketener är elektrofila. De tillsätter aminer för att ge tioamider:
- R2C =C=S + HNR'2 → R2CH - C (S) -NR'2
Med peroxisyror producerar de tioketen-S-oxider:
- R2C =C=S + R'CO3H → R2CH = C =S=O + R'CO2H
Tioketener binder till metallkarbonyler och ger addukter.
Besläktade föreningar
- kolsubsulfid ( S=C=C=C=S ).
Det har föreslagits att tioketen kan vara involverat i cellskadaprocesser.
-
^
Noslash;rkjær, Kim; Senning, Aexander (1992). "Thio-, Seleno- och Telluroketenes". Svavelrapporter . 11 (2): 361–384. doi : 10.1080/01961779208046190 .
{{ citera tidskrift }}: CS1 underhåll: flera namn: lista över författare ( länk ) - ^ Otto-Albrecht Neuman (redaktör). Rompps Encyclopedia of Chemistry, Frank'sche Publishing House, Stuttgart, 1983, 8. Edition, sid. 4242, ISBN 3-440-04513-7 .
- ^ a b Elam, EU; Utslag, FH; Dougherty, JT; Goodlett, VW; Brannock, KC (1968). "Di- tert -Butyltioketen". The Journal of Organic Chemistry . 33 (7): 2738–2741. doi : 10.1021/jo01271a027 .
- ^ a b Schaumann, Ernst; Harto, Surya; Adiwidjaja, Gunadi (1979). "Kristall‐ och Molekülstruktur eines Ketens, eines Thioketens och eines Thioketen‐S‐oxids". Chemische Berichte . 112 (7): 2698–2708. doi : 10.1002/cber.19791120738 .
- ^ Raasch, Maynard S. (1970). "Bis(trifluorometyl)tioketen. I. Syntes och cykloladdningsreaktioner". J. Org. Chem . 35 (10): 3470–3483. doi : 10.1021/jo00835a064 .
- ^ Seitz, Karsten; Benecke, Jörg; Behrens, Ulrich (1989). "Öbergangsmetall-heteroallen-komplexe". Journal of Organometallic Chemistry . 371 (2): 247–256. doi : 10.1016/0022-328x(89)88030-1 .
- ^ Dekant, Wolfgang; Urban, Gudrun; Goersmann, Claus; Anders, MW (1991). "Tioketenbildning från a-haloalkenyl-2-nitrofenyldisulfider: modeller för biologiska reaktiva mellanprodukter av cytotoxiska S-konjugat". J. Am. Chem. Soc . 113 (13): 5120–5122. doi : 10.1021/ja00013a090 .