Stoppat-flöde
Stopped-flow är en experimentell teknik för att studera kemiska reaktioner med en halvtid i storleksordningen 1 ms, introducerad av Britton Chance och utökad av Quentin Gibson (Andra tekniker, såsom temperaturhoppningsmetoden, är tillgängliga för mycket snabbare processer. )
Beskrivning av metoden
Sammanfattning
Stoppad-flow spektrometri tillåter kemisk kinetik för snabba reaktioner (med halva gånger i storleksordningen millisekunder) att studeras i lösning. Det användes först speciellt för enzymkatalyserade reaktioner. Sedan hittade det stoppade flödet snabbt sin plats i nästan alla biokemi-, biofysik- och kemilaboratorier med ett behov av att följa kemiska reaktioner i millisekunders tidsskalan. I sin enklaste form blandar ett stoppat flöde två lösningar. Små volymer av lösningar drivs snabbt och kontinuerligt in i en högeffektiv blandare. Denna blandningsprocess initierar sedan en extremt snabb reaktion. Den nyligen blandade lösningen går till observationscellen och trycker ut innehållet i cellen (lösningen som återstår från det föregående experimentet eller från nödvändiga tvättsteg). Den tid som krävs för att denna lösning ska passera från blandningspunkten till observationspunkten kallas dödtid. Minsta injektionsvolym kommer att bero på blandningscellens volym. När tillräckligt med lösning har injicerats för att helt avlägsna den föregående lösningen, når instrumentet ett stationärt tillstånd och flödet kan stoppas. Beroende på sprutdrivningstekniken uppnås flödesstoppet genom att använda en stoppventil som kallas hårdstopp eller genom att använda en stoppspruta. Det stoppade flödet skickar också en "startsignal" till detektorn som kallas triggern så att reaktionen kan observeras. Tidpunkten för triggern är vanligtvis mjukvarustyrd så att användaren kan trigga samtidigt som flödet stannar eller några millisekunder innan stoppet för att kontrollera det stationära tillståndet har uppnåtts.
Så detta är en mycket ekonomisk teknik.
Reaktantsprutor
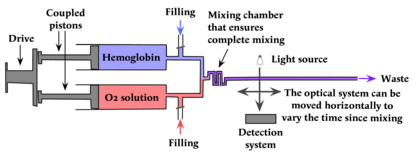
Två sprutor är fyllda med lösningar som inte genomgår en kemisk reaktion förrän de blandas ihop. Dessa har kolvar som drivs av en enda drivkolv eller av oberoende stegmotorer, så att de kopplas ihop och deras innehåll pressas ut samtidigt i en blandningsanordning.
Blandningskammare
När de två lösningarna väl har tvingats ut ur sina sprutor kommer de in i ett blandningssystem som har bafflar för att säkerställa fullständig blandning, med turbulent flöde snarare än laminärt flöde, vilket skulle tillåta de två lösningarna att flyta sida vid sida med ofullständig blandning.
Död tid
Dödtiden är tiden för lösningarna att gå från blandningspunkten till observationspunkten, det är den del av kinetiken som inte kan observeras. Så ju lägre dödtid, desto mer information kan användaren få. I äldre instrument kan detta vara i storleksordningen 1 ms, men förbättringar tillåter nu en dödtid på cirka 0,3 ms.
Observationscell
De blandade reaktanterna passerar en observationscell som gör att reaktionen kan följas spektrofotometriskt, typiskt med ultraviolett spektroskopi , fluorescensspektroskopi , cirkulär dikroism eller ljusspridning , och det är nu vanligt att kombinera flera av dessa. Observationskyvetter med kort ljusväg (0,75 till 1,5 mm) är vanligtvis att föredra för fluorescensmätningar för att minska självabsorptionseffekter. Observationskyvett med längre ljusväg (0,5 cm till 1 cm) är att föredra för absorbansmätningar. Modernt stoppat flöde kan rymma olika modeller av celler och det är möjligt att byta kyvett mellan två experiment. För röntgenmätningar med stoppat flöde används en kvartskapillär med tunn vägg för att minimera kvartsabsorptionen. Samtidiga röntgen- och absorbansmätningar är möjliga i samma kapillär.
Stoppar
Väl genom observationscellen kommer blandningen in i en tredje spruta som innehåller en kolv som drivs av flödet för att aktivera en omkopplare för att stoppa flödet och aktivera observationen.
Kontinuerligt flöde
Stoppad-flow-metoden är en utveckling av den kontinuerliga-flow-metod som användes av Hamilton Hartridge och Francis Roughton för att studera bindningen av O 2 till hemoglobin. I avsaknad av något stoppsystem passerade reaktionsblandningen till ett långt rör förbi ett observationssystem (som 1923 bestod av en enkel kolorimeter) för att gå till spillo. Genom att flytta kolorimetern längs röret och känna till flödeshastigheten kunde Hartridge och Roughton mäta processen efter en känd tid.
På sin tid var detta ett revolutionerande framsteg som visade att ett till synes svårlöst problem (att studera en process som tog millisekunder med utrustning som krävde sekunder för varje mätning) kunde lösas med enkel utrustning. Men i praktiken var det begränsat till reaktanter tillgängliga i stora mängder: för proteiner begränsade detta det effektivt till reaktioner av hemoglobin. För praktiska ändamål är detta tillvägagångssätt föråldrat.
Släckt flöde
Stoppad-flow-metoden beror på förekomsten av spektroskopiska egenskaper som kan användas för att följa reaktionen. När så inte är fallet ger släckt flöde ett alternativ som använder konventionella kemiska metoder för analys. Istället för ett mekaniskt stoppsystem stoppas reaktionen genom släckning , varvid produkterna levereras till en mottagare som stoppar reaktionen omedelbart, antingen genom momentan frysning eller genom att denaturera enzymet med ett kemiskt denatureringsmedel eller genom att exponera provet för en denaturerande ljuskälla. Liksom i kontinuerligt flödesmetoden kan tiden mellan blandning och kylning varieras genom att variera längden på röret.
Den pulserade kylda flödesmetoden introducerad av Alan Fersht och Ross Jakes övervinner behovet av ett långt rör. Reaktionen initieras precis som i ett experiment med stoppat flöde, men det finns en tredje spruta som åstadkommer släckning av en bestämd och förinställd tid efter initieringen.
Släckt flöde har både fördelar och nackdelar med avseende på stoppat flöde. Å ena sidan gör kemisk analys det tydligt vilken process som mäts, medan det kanske inte alltid är uppenbart vilken process en spektroskopisk signal representerar. Å andra sidan är släckt flöde mycket mer mödosamt, eftersom varje punkt längs tidsförloppet måste bestämmas separat. Bilden till vänster för katalys av nitrogenas från Klebsiella pneumoniae illustrerar båda dessa punkter: överensstämmelsen i halvtid indikerar att absorbansen vid 420 nm mätte frisättningen av Pi , men experimentet med släckt flöde krävde 11 datapunkter.
Vidare läsning
- Alan Fersht (1998). Structure and Mechanism in Protein Science: Guide to Enzyme Catalysis and Protein Folding . New York: WH Freeman. s. 132–168. ISBN 9780716732686 .
- Athel Cornish-Bowden (2012). Fundamentals of Enzyme Kinetics (4:e upplagan). Weinheim: Wiley-Blackwell. s. 391–396. ISBN 978-3527330744 .