Stannylene
Stannylener (R 2 Sn:) är en klass av organotenn(II)-föreningar som är analoger till karben . Till skillnad från karben, som vanligtvis har ett triplettgrundtillstånd, har stannylener ett singlettgrundtillstånd eftersom valensorbitaler av tenn (Sn) har mindre tendens att bilda hybridorbitaler och därmed är elektronerna i 5s orbitaler fortfarande ihopparade. Fria stannylener stabiliseras av steriskt skydd. Addukter med Lewis-baser är också kända.
Historia
Den första persistenta stannylenen, [(Me3Si ) 2CH ] 2Sn , rapporterades av Michael F. Lappert 1973. Lappert använde samma syntetiska tillvägagångssätt för att syntetisera den första diamidostannylen [(Me3Si ) 2N ] 2Sn in 1974.
Det kortlivade, övergående stannylenet Me2Sn har genererats genom termolys av cyklo- (Me2Sn ) 6 .
Syntes och karaktärisering
Ihållande stannylen
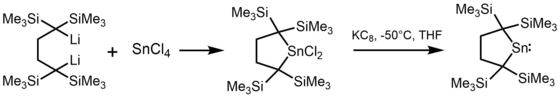
De flesta alkylstannylener har syntetiserats genom alkylering av tenn(II)dihalogenider med organolitiumreagens . Till exempel syntetiserades den första stannylenen, [(Me3Si ) 2CH ] 2Sn med användning av ( Me3Si ) 2CHLi och SnCl2 . 
I vissa fall har stannylener framställts genom reduktion av en tenn(IV)-förening med KC 8
Amidostannylen kan också syntetiseras genom att använda en tenn(II)dihalogenid och litiumamiden.
Kortlivad stannylen
Isoleringen av en övergående alkylstannylen är svårare. Den första isoleringen av dimetylstannylen antogs göras genom att termolysera cyklostannan (Me2Sn ) 6 , som var produkten av kondensationen av Me2Sn ( NEt2 ) 2 och Me2SnH2 . Bevisen kom från vibrationsfrekvenserna för dimetylstannylen som identifierats med infraröd spektroskopi, vilket överensstämmer med det beräknade värdet. Förekomsten av denna svårfångade SnMe 2 bekräftades ytterligare av upptäckten av absorption av synligt ljus som matchar den beräknade elektroniska övergången av SnMe 2 i gasfas.
En annan metod för att framställa kortlivad stannylen är laserblixtfotolys med användning av tetraalkyltenn(IV)-förening (t.ex. SnMe 4 ) som en prekursor. Genereringen av stannylen kan övervakas med transient UV-VIS-spektroskopi.
Struktur och bindning
Stannylener kan ses som sp 2 -hybridiserade med ledig 5p orbital och ett ensamt par. Detta ger upphov till deras röda färg från n till p övergång.
Med specifik typ av ligander reduceras elektronbristen hos monomert stannylen genom den agostiska interaktionen från BH-bindning. Detta koncept bevisades av Mark Kenyon och medarbetare 2006 när de syntetiserade den cykliska dialkylstannylenen [{n-Pr 2 P(BH 3 )}(Me 3 Si) CCH 2 ] 2 Sn. Kristallstrukturen för den syntetiserade föreningen visade arrangemanget av en BH-bindning mot Sn-atomen med B-H--Sn-bindningsavståndet på 2,03 Å. Minskning av Sn-elektronbrist bevisades av spektroskopiska data, speciellt 119Sn NMR-spektra som visade det drastiskt låga kemiska skiftet (587 och 787 ppm jämfört med 2323 ppm i analog dialkylstannylen) vilket indikerar mer elektrondensitet runt Sn i detta fall.
Reaktivitet
Oligomerisering
Små, instabila stannylener (t.ex. dimetylstannylen) genomgår självoligomerisering vilket ger cykliska oligostannaner, som kan användas som stannylenkällor.
Mer skrymmande stannylener (t.ex. Lapperts stannylen) tenderar å andra sidan att bilda en dimer. Naturen hos Sn-Sn-bindningen i stannylendimer skiljer sig ganska mycket från CC-bindning i karbendimer (dvs. alken). Eftersom alken utvecklar en typisk dubbelbindningskaraktär och molekylen har en plan geometri, har stannylendimer en trans-böjd geometri. Dubbelbindningen i stannylendimer kan betraktas som två donator-acceptor-interaktioner. Elektronlokaliseringsfunktionsanalysen (ELF) av stannylendimer visar en disynaptisk bassäng (elektroner i bindande orbitaler) på båda Sn-atomerna, vilket indikerar att interaktionen mellan två Sn-atomer är två ovanliga böjda dativbindningar . Bortsett från det påverkas stannylendimerens stabilitet också av den steriska repulsionen och dispersionsattraktionen mellan skrymmande substituenter.
Insättningsreaktion
Alkylstannylener kan reagera med olika reagens (t.ex. alkylhalider, enoner, diener) på ett oxidativt additions- (eller insättnings-) sätt. Reaktionen mellan stannylen och 9,10-fenantrolindion producerar en EPR-signal som identifierades vara 9,10-fenantrenedion-radikalanjon, vilket indikerar att denna reaktion fortsätter via radikalmekanism.
Cykelladdning
Även om stannylener är mer stabila än dess lättare karbenanaloger, genomgår de lätt [2+4] cykloadditionsreaktion med Z-alkener. Tillsatsen av (CH(SiMe3 ) 2 ) 2Sn till 2,7-difenylocta-2,3,5,6-tetraen fortskrider på ett keletropiskt sätt, som tillåts av Woodward-Hoffmann regler .
Metallcentrum för oxidativ tillsats och reduktiv eliminering
När det gäller Sn II /Sn IV -paret liknar vissa stannylener övergångsmetaller. Singlett-triplett-energiseparationen anses ha en stark effekt på oxidativ additionsreaktivitet, genom att använda en mycket stark σ-donatorboryl (-BX 2 ) ligand. Resultaten visade att inte bara molekylärt väte utan även EH-bindning (E = B, Si, O, N) kan tillsättas oxidativt på Sn. I ammoniak- och vattenfall kan den oxidativt tillsatta produkten också genomgå reduktiv eliminering, vilket ger O- eller NB-bindningar.