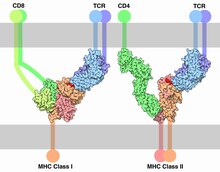
MHC-begränsning
MHC-begränsad antigenigenkänning , eller MHC-restriktion , hänvisar till det faktum att en T-cell kan interagera med en själv- stor histokompatibilitetskomplexmolekyl och en främmande peptid bunden till den, men kommer bara att svara på antigenet när den är bunden till en viss MHC molekyl.
När främmande proteiner kommer in i en cell bryts de i mindre bitar som kallas peptider. Dessa peptider, även kända som antigener, kan härröra från patogener såsom virus eller intracellulära bakterier. Främmande peptider förs till ytan av cellen och presenteras för T-celler av proteiner som kallas det stora histokompatibilitetskomplexet (MHC). Under utvecklingen av T-celler går T-celler igenom en selektionsprocess i tymus för att säkerställa att T-cellsreceptorn ( TCR ) inte känner igen MHC- molekylen som presenterar självantigener, dvs att dess affinitet inte är för hög. Hög affinitet betyder att den kommer att vara autoreaktiv, men ingen affinitet betyder att den inte kommer att binda tillräckligt starkt till MHC. Urvalsprocessen resulterar i utvecklade T-celler med specifika TCR som kanske bara svarar på vissa MHC- molekyler men inte andra. Det faktum att TCR bara känner igen vissa MHC-molekyler men inte andra bidrar till "MHC-restriktion". Den biologiska orsaken till MHC-begränsning är att förhindra generering av överflödiga vandrande lymfocyter, därav energibesparing och ekonomi för cellbyggande material.
T-celler är en typ av lymfocyter som är betydande i immunsystemet för att aktivera andra immunceller. T-celler känner igen främmande peptider genom T-cellsreceptorer (TCR) på ytan av T-cellerna och utför sedan olika roller beroende på vilken typ av T-cell de är för att försvara värden från den främmande peptiden, som kan har kommit från patogener som bakterier, virus eller parasiter. Genom att upprätthålla restriktionen att T-celler aktiveras av peptidantigener endast när antigenerna är bundna till själv-MHC-molekyler, lägger MHC-restriktionen ytterligare en dimension till specificiteten hos T-cellsreceptorer så att ett antigen endast känns igen som peptid-MHC-komplex.
MHC-restriktion i T-celler inträffar under deras utveckling i tymus, specifikt positiv selektion. Endast de tymocyter (utvecklande T-celler i tymus) som kan binda, med en lämplig affinitet, till MHC-molekylerna kan ta emot en överlevnadssignal och gå vidare till nästa nivå av selektion. MHC-restriktion är signifikant för att T-celler ska fungera korrekt när den lämnar tymus eftersom den tillåter T-cellsreceptorer att binda till MHC och upptäcka celler som är infekterade av intracellulära patogener, virala proteiner och med genetiska defekter. Två modeller som förklarar hur restriktion uppstod är könslinjemodellen och urvalsmodellen.
Könslinjemodellen antyder att MHC-restriktion är ett resultat av evolutionärt tryck som gynnar T-cellsreceptorer som kan binda till MHC. Selektionsmodellen antyder att inte alla T-cellsreceptorer visar MHC-restriktion, men endast T-cellsreceptorerna med MHC-restriktion uttrycks efter tymusselektion. Faktum är att båda hypoteserna återspeglas i bestämningen av TCR-restriktion, så att både könslinjekodade interaktioner mellan TCR och MHC och samreceptorinteraktioner med CD4 eller CD8 för att signalera T-cellmognad inträffar under selektion.
Introduktion
T-cellers TCR känner igen linjära peptidantigener endast om de är kopplade med en MHC-molekyl. Med andra ord är liganderna av TCR: er specifika peptid-MHC-komplex. MHC-restriktion är särskilt viktig för självtolerans, vilket säkerställer att immunsystemet inte riktar sig mot självantigener. När primära lymfocyter utvecklas och differentierar i tymus eller benmärg , dör T-celler genom apoptos om de uttrycker hög affinitet för självantigener som presenteras av en MHC-molekyl eller uttrycker för låg affinitet för egen MHC.
T-cellmognad involverar två distinkta utvecklingsstadier: positivt urval och negativt urval . Positiv selektion säkerställer att alla T-celler med tillräckligt hög affinitet för MHC-bunden peptid överlever och går vidare till negativ selektion, medan negativ selektion inducerar död i T-celler som binder själv-peptid-MHC-komplex för starkt. I slutändan differentierar T-cellerna och mognar till att bli antingen T-hjälparceller eller T-cytotoxiska celler. Vid denna tidpunkt lämnar T-cellerna det primära lymfoida organet och går in i blodomloppet.
Interaktionen mellan TCR och peptid-MHC-komplex är signifikant för att upprätthålla immunsystemet mot främmande antigener. MHC-restriktion tillåter TCR att detektera värdceller som är infekterade av patogener, innehåller icke-självproteiner eller bär främmande DNA. Men MHC-restriktion är också ansvarig för kroniska autoimmuna sjukdomar och överkänslighet.
Strukturell specificitet
Peptid-MHC-komplexet presenterar en yta som ser ut som ett förändrat jag till TCR. Ytan som består av två α-helixar från MHC och en bunden peptidsekvens projiceras bort från värdcellen till T-cellerna, vars TCR:er projiceras bort från T-cellerna mot värdcellerna. I motsats till T-cellsreceptorer som känner igen linjära peptidepitoper, känner B-cellsreceptorer igen en mängd olika konformationella epitoper (inklusive peptid, kolhydrat, lipid och DNA) med specifika tredimensionella strukturer.
Utskjutning
Införandet av MHC-restriktioner på den mycket varierande TCR har orsakat het debatt. Två modeller har föreslagits för att förklara införandet av MHC-restriktioner. Germline-modellen föreslår att MHC-restriktion är hårdkopplad i TCR Germline-sekvensen på grund av samutveckling av TCR och MHC för att interagera med varandra. Selektionsmodellen antyder att MHC-restriktion inte är en fast ansluten egenskap i Germline-sekvenserna av TCR, utan påtvingas dem av CD4- och CD8-co-receptorer under positiv selektion. Den relativa betydelsen av de två modellerna är ännu inte fastställd.
Germline modell
Germline-hypotesen antyder att förmågan att binda till MHC är inneboende och kodad inom det könslinje-DNA som kodar för TCR. Detta beror på evolutionära tryckselekter för TCR som kan binda till MHC och selekterar mot de som inte kan binda till MHC. Sedan uppkomsten av TCR och MHC för ~500 miljoner år sedan, finns det stora möjligheter för TCR och MHC att utvecklas samtidigt för att känna igen varandra. Därför föreslås det att evolutionärt tryck skulle leda till konserverade aminosyrasekvenser vid kontaktområden med MHC på TCR.
Bevis från röntgenkristallografi har visat jämförbara bindningstopologier mellan olika TCR- och MHC-peptidkomplex. Dessutom stöder konserverade interaktioner mellan TCR och specifika MHC hypotesen att MHC-restriktion är relaterad till samutvecklingen av TCR och MHC i viss utsträckning.
Urvalsmodell
Selektionshypotesen hävdar att istället för att vara en inneboende egenskap, åläggs MHC-restriktion på T-cellerna under positiv tymisk selektion efter att slumpmässiga TCR har producerats. Enligt denna modell är T-celler kapabla att känna igen en mängd olika peptidepitoper oberoende av MHC-molekyler innan de genomgår tymusselektion. Under tymisk selektion signaleras endast T-celler med affinitet till MHC att överleva efter att CD4- eller CD8 -koreceptorerna också binder till MHC-molekylen. Detta kallas positivt urval.
Under positiv selektion initierar co-receptorerna CD4 och CD8 en signalkaskad efter MHC-bindning. Detta involverar rekryteringen av Lck, ett tyrosinkinas som är nödvändigt för T-cellmognad som är associerat med den cytoplasmatiska svansen av CD4- eller CD8-koreceptorerna. Selektionsmodellen hävdar att Lck riktas till TCR av co-receptorer CD4 och CD8 när de känner igen MHC-molekyler. Eftersom TCR interagerar bättre med Lck när de binder till MHC-molekylerna som binder till co-receptorerna i ett ternärt komplex, kan T-celler som kan interagera med MHC som binds till av co-receptorerna aktivera Lck-kinaset och få en överlevnad signal.
Som stöd för detta argument uttrycker genetiskt modifierade T-celler utan CD4- och CD8-koreceptorer MHC-oberoende TCR. Det följer att MHC-restriktion påtvingas av CD4- och CD8-samreceptorer under positivt urval av T-cellselektion.
Försoning
En försoning av de två modellerna erbjöds senare, vilket tyder på att både co-receptor och könsceller predisposition för MHC-bindning spelar betydande roller för att införa MHC-restriktion. Eftersom endast de T-celler som är kapabla att binda till MHC selekteras under positiv selektion i tymus, väljer evolutionärt tryck till viss del för könslinje-TCR-sekvenser som binder MHC-molekyler. Å andra sidan, som föreslås av selektionsmodellen, kräver T-cellsmognad att TCR binder till samma MHC-molekyler som CD4- eller CD8-samreceptorn under T-cellselektion, vilket innebär att MHC-restriktioner införs.
externa länkar
-
 Media relaterade till MHC-begränsning på Wikimedia Commons
Media relaterade till MHC-begränsning på Wikimedia Commons