Alkalimetallnitrat
Alkalimetallnitrater är kemiska föreningar som består av en alkalimetall ( litium , natrium , kalium , rubidium och cesium ) och nitratjonen . Endast två är av stort kommersiellt värde, natrium- och kaliumsalterna. De är vita, vattenlösliga salter med smältpunkter från 255 °C ( LiNO
3 ) till 414 °C ( CsNO
3 ) på ett relativt smalt intervall på 159 °C
| Förening | Kemisk formel | Molar massa | Smältpunkt | Strukturera |
|---|---|---|---|---|
| Litiumnitrat | LiNO 3 | 68,946 g/mol | 255 °C (491 °F; 528 K) |

|
| Natriumnitrat | NaNO3 _ | 84,9947 g/mol | 308 °C (586 °F; 581 °K) |
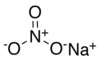
|
| Kaliumnitrat | VET 3 | 101,1032 g/mol | 334 °C (633 °F; 607 K) |

|
| Rubidiumnitrat | RbNO 3 | 147,473 g/mol | 310 °C (590 °F; 583 K) |

|
| Cesiumnitrat | CsNO 3 | 194,91 g/mol | 414 °C (777 °F; 687 K) |

|
Smältpunkten för alkalimetallnitraterna tenderar att öka från 255 °C till 414 °C (med en anomali för rubidium som inte är korrekt inriktat i serien) när atommassan och jonradien ( naken katjon ) för den alkaliska metallen ökar , går ner i kolumnen. På liknande sätt, men inte presenterat här i tabellen, minskar även lösligheten av dessa salter i vatten med metallens atommassa.
Ansökningar
Natrium- och kaliumnitrater används vanligtvis som gödningsmedel . Eftersom de också är starka oxidationsmedel kommer de in i pyrotekniska kompositioner och tillverkning av sprängämnen .
En mindre användning är för att färga ljuset som sänds ut av fyrverkerier :
- litiumnitrat ger en röd färg,
- natriumnitrat ger en gul/orange färg,
- kaliumnitrat och rubidiumnitrat ger violetta färger,
- cesiumnitrat ger en indigofärg.
På ett allmänt sätt växlar den utsända färgen progressivt från rött till violett i det synliga ljusspektrumet när det går ner i kolumnen av alkaliska metaller i Mendeleevs periodiska system . Det motsvarar en minskning av våglängden för det ljus som emitteras under elektronavexciteringssteget i atomerna som bringas till hög temperatur. De fotoner som emitteras av cesium är mer energiska än de av litium .
Se även
